TIOSIVAR 18 mcg inhilasyon tozu sert kaps�l (30 kaps�l) Klinik �zellikler
{ Tiotropium Bromur Monohidrat }
KL�N�K OZELL�KLER
4.1. Terap�tik endikasyonlar
Tiotropium brom�r, orta ve a��r KOAH (kronik obstruktif akci�er hastal���) olgular�nda d�zenli kullan�ld���nda atak s�kl���n� azaltmakta, semptomlar� ve ya�am kalitesini d�zeltebilmekte, ancak uzun d�nemdeki FEVd�����n� de�i�tirmemektedir.
4.2. Pozoloji ve uygulama �ekli
Eri�kinler4.2. Pozoloji ve uygulama �ekli
Eri�kinlerT�OS�VAR' �n �nerilen dozu, g�nde bir kez bir kaps�l i�eri�inin inhale edilmesidir. �nerilen dozdan daha fazla ila� kullan�lmamal�d�r.
Uygulama sekli:
Sadece inhalasyon yoluyla kullan�l�r. Kaps�ller a��zdan yutulmaz.
�lac�n uygun �ekilde uyguland���ndan emin olmak i�in, bir doktor veya ba�ka bir sa�l�k profesyoneli taraf�ndan inhalerin nas�l kullan�laca�� hastaya g�sterilmelidir. Kuru toz inhalerlerin (DPI) do�ru kullan�m� tedavinin ba�ar�s� i�in gereklidir. Hastaya kullanma talimat�n� dikkatlice okumalar� ve kullan�m talimatlar� ve talimattaki resimli �emalar� izlemeleri �nerilir.
Hastalar�n jelatin kaps�l�n par�alanabilece�ini ve k���k jelatin par�alar�n�n inhalasyondan sonra a��z veya bo�az b�lgesine ula�abilece�ini bilmesi �nemlidir. Hastaya jelatinin zarars�z oldu�u, a��zda yumu�ayaca�� ve yutulabildi�i s�ylenmelidir. Kaps�l� bir defadan fazla delmemek suretiyle par�alanma olas�l��� asgari d�zeye indirilebilir.
|
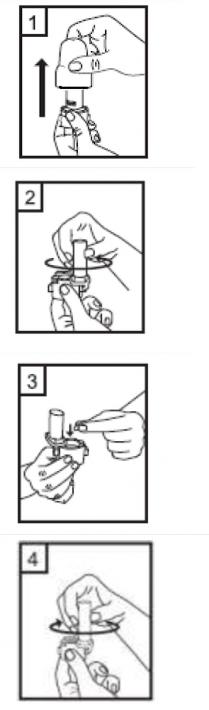
1-Kapa�� �ekip ��kar�n�z. |
| 2-Kaps�l b�lmesini a��n�z. Cihaz�n taban�n� s�k�ca tutup, a�mak i�in cihaz�n �st taraf�nda bulunan ok y�n�nde �eviriniz. |
| 3-Parmaklar�n�z�n tamamen kuru oldu�undan emin olunuz. Ambalaj�ndan bir kaps�l ��kar�n�z ve bu kaps�l� cihaz�n taban�ndaki kaps�l b�lmesine yat�k olarak yerle�tiriniz. Kaps�lleri, kullan�mdan hemen �nce ambalaj�ndan ��karman�z �nemlidir.
�NEML�: Kaps�l� a��zl���n i�erisine yerle�tirmeyiniz! |
| 4-A��zl��� “klik” sesi duyana kadar geri �evirerek kapal� duruma getiriniz.. |
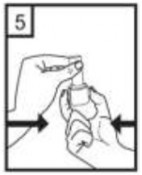
| 5-Tozu kaps�lden serbest b�rakmak i�in:
L�tfen dikkat: Bu a�amada jelatin kaps�l par�alanabilir ve soluma s�ras�nda k���k jelatin par�alar� a�z�n�za veya bo�az�n�za gelebilir. Fakat jelatin yenilebilir nitelikte oldu�undan zarars�zd�r. |
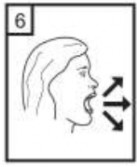
| 6-Nefesinizi kuvvetlice d��ar� verin. |
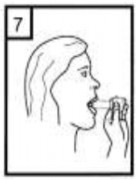
| 7-A��z par�as�n� a�z�n�za yerle�tirin ve ba��n�z� hafif�e geriye do�ru e�iniz. Dudaklar�n�z ile a��zl��� s�k�ca sar�n�z. Olabildi�ince h�zl�, duraksamadan ve alabildi�iniz kadar derin nefes al�n�z.
L�tfen dikkat: Nefes alma s�ras�nda, kaps�l, kaps�l haznesinde titre�ir ve bir ses (v�z�lt�) olu�ur. Bu sesi duymad�ysan�z kaps�l�n, kaps�l b�lmesinde s�k���p s�k��mad���n� kontrol ediniz. Bu durumda cihaz� a��n�z ve kaps�l� b�lmesinde oynatarak gev�etiniz. Daha sonra 7. basama�� tekrarlay�n�z. Kaps�l� s�k��t��� yerden kurtarmak i�in d��melere tekrar tekrar BASMAYINIZ. |
Cihaz� dik tutun (a��z par�as� yukar�da olacak �ekilde)
Kenarlardaki iki kulak���a (d��melere) AYNI ANDA ve SADECE B�R KEZ bas�p b�rak�n�z. B�ylelikle cihazdaki kaps�l� delmi� oldunuz.
| 8- Cihaz�n i�erisinden nefes ald�ktan sonra, nefesinizi olabildi�ince tutunuz ve cihaz� a�z�n�zdan ��kar�n�z. Sonra burnunuzdan nefes veriniz. Kaps�l b�lmesini a��n�z ve kaps�lde toz kal�p kalmad���n� kontrol ediniz. E�er kalm�� ise 6-8 basamaklar� tekrarlay�n�z. |
| 9-Kulland�ktan sonra bo� kaps�l� ��kart�n ve at�n�z. Doktorunuzun �nerisi do�rultusunda ayn� i�lemleri di�er kaps�l i�in de tekrarlay�n�z. |
Temizleme:
Temizleme talimatlar� i�in hastalara Kullanma Talimat�n� dikkatlice okumalar� �nerilmelidir. Toz kal�nt�lar�n� temizlemek i�in a��z par�as�n� ve kaps�l haznesini KURU ve temiz bir bez ile silin. Temiz yumu�ak bir f�r�a da bu ama�la kullan�labilir.
Cihaz� temizlemek i�in SU KULLANMAYIN.
�zel pop�lasyonlara ili�kin ek bilgiler:
B�brek yetmezli�i: B�brekleri bozuk olan hastalar T�OS�VAR'� �nerilen dozlarda kullanabilirler. Orta ila �iddetli b�brek yetmezli�i olan hastalarda (kreatinin klerensi ≤50 ml/dk) T�OS�VAR kullan�m� yak�ndan izlenmelidir (Bkz. 4.4 ve 5.2).
Karaci�er yetmezli�i:
Karaci�erleri bozuk olan hastalar T�OS�VAR'� �nerilen dozlarda kullanabilirler (Bkz.5.2).
Pediyatrik pop�lasyon:
18 ya��ndan k���k hasta grubunda KOAH durumunda T�OS�VAR' �n kullan�m alan� yoktur.
T�OS�VAR' �n kistik fibrozda, �ocuklar ve adolesanlardaki g�venli�i ve etkinlili�i belirlenmemi�tir. Bu konuda veri yoktur.
Geriyatrik pop�lasyon:
Ya�l� hastalar T�OS�VAR' � �nerilen dozlarda kullanabilirler.
4.3. Kontrendikasyonlar
T�OS�VAR, tiotropium brom�re, atropin veya t�revlerine, �rn. ipratropium ya da oksitropium veya bu ilac�n bile�enlerinden herhangi birine kar�� a��r� duyarl�l�k �yk�s� olan hastalarda kontrendikedir (Bkz. B�l�m 2 ve B�l�m 6.1; Yard�mc� maddeler).
4.4. �zel kullan�m uyar�lar� ve �nlemleri
T�OS�VAR, g�nde bir kez kullan�lan bir idame tedavisi bronkodilat�r�d�r, akut bronkospazm epizotlar�n�n ba�lang�� tedavisinde, yani kurtarma tedavisi �eklinde kullan�lmamal�d�r.
T�OS�VAR uygulamas�ndan sonra ani a��r� duyarl�l�k reaksiyonlar� olu�abilir.
Di�er antikolinerjik ila�larla oldu�u gibi, T�OS�VAR dar-a��l� glokomu k�t�le�tirebilece�inden, prostat hiperplazisi ya da mesane boynu obstr�ksiyonu bulunan hastalarda idrar g��l��� olu�turabilece�inden bu hastalarda dikkatle kullan�lmal�d�r.
�nhalasyon yoluyla al�nan ila�lar, inhalasyonun ind�kledi�i bronkospazma neden olabilirler.
Yeni (<6 ay) miyokard enfarkt�s� ge�iren hastalarda; stabil olmayan veya ya�am� tehdit edici veya
giri�im gerektiren veya son 1 y�l i�inde tedavisinde de�i�iklik yap�lm�� kardiyak aritmi durumlar�nda; son 1 y�l i�inde kalp yetmezli�i nedeniyle (NYHA S�n�f III veya IV) hastaneye yat�r�lan hastalarda dikkatli kullan�lmal�d�r. Bu hastalar klinik �al��malara dahil edilmemi�tir ve bu ko�ullar antikolinerjik etki mekanizmas�ndan etkilenebilir.
Renal fonksiyonlardaki azalmaya ba�l� olarak plazma konsantrasyonu artt��� i�in, orta ile �iddetli b�brek yetmezli�i olan hastalarda (kreatinin klerensi ≤ 50 mL/dk) T�OS�VAR, sadece beklenen yararlar potansiyel risklere g�re daha �st�nse kullan�lmal�d�r. �iddetli b�brek yetmezli�i olan hastalarda uzun s�reli deneyim yoktur (Bkz. 5.2).
Hastalara, T�OS�VAR'�n do�ru bir �ekilde nas�l kullan�laca�� ��retilmelidir. Hastalara tozun g�ze ka�mamas� i�in dikkatli olmalar� ���tlenmelidir. Bu ilac�n g�ze ka�mas� durumunda, dar- a��l� glokomunun ortaya ��kabilece�i veya k�t�ye gidebilece�i, konjonktivada konjesyon veya korneada �dem sonucunda geli�en g�z k�zarmas�yla birlikte g�zde a�r� veya rahats�zl�k hissi, ge�ici bulan�k g�rme, haleler veya renkli g�r�nt�ler g�rme, akut dar a��l� glokom belirtileri olabilece�i konusunda hasta bilgilendirilmelidir. Bu semptomlar herhangi bir kombinasyonu
geli�irse, hasta ilac� kesmeli ve hemen bir uzman hekime ba�vurmal�d�r. Miyotik g�z damlalar�n�n, etkili bir tedavi sa�lamad�klar� kabul edilmektedir.
Antikolinerjik ila�larla g�zlenen ag�z kurulu�u uzun d�nemde di� ��r�klerine yol a�abilir. T�OS�VAR g�nde bir defadan daha s�k kullan�lmamal�d�r (Bkz. 4.9).
T�O�M�T kaps�lleri yaln�zca inhaler cihaz� ile kullan�lmal�d�r.
T�OS�VAR laktoz i�ermektedir. Nadir kal�t�msal galaktoz intolerans�, Lapp laktaz yetmezli�i ya da glikoz-galaktoz malabsorpsiyon problemi olan hastalar�n bu ilac� kullanmamalar� gerekir.
4.5. Di�er t�bbi �r�nler ile etkile�imler ve di�er etkile�im �ekilleri
D�zenli ila� etkile�imi �al��malar� y�r�t�lmemi� olmakla birlikte, tiotropium brom�r inhalasyon tozu, KOAH tedavisinde yayg�n olarak kullan�lan di�er ilaclar ile beraber, ila� etkile�imine y�nelik klinik bulgular g�r�lmeksizin kullan�lm��t�r; sempatomimetik bronkodilatatorler, metilksantinler, oral ve inhale steroidler, bu ila�lar aras�ndad�r.
Uzun etkili beta agonistlerin veya inhale kortikosteroidlerin tiotropium maruziyetini de�i�tirmedi�i bulunmu�tur.
T�OS�VAR' �n di�er antikolinerjik i�eren ila�larla birlikte uygulanmas� hen�z �al���lmam��t�r ve bu nedenle �nerilmemektedir.
�zel pop�lasyonlara ili�kin ek bilgiler:
�zel veri bulunmamaktad�r.
Pediyatrik pop�lasyon:
�zel veri bulunmamaktad�r.
4.6. Gebelik ve laktasyon
Genel tavsiye: Gebelik kategorisi C'dir.
�ocuk do�urma potansiyeli bulunan kad�nlar/Do�um kontrol� (Kontrasepsiyon): �ocuk do�urma potansiyeli bulunan kad�nlar, tedavi s�resince t�bben etkili oldu�u kabul edilen do�um kontrol y�ntemleri kullanmal�d�r.
Gebelik d�nemi: Gebe kad�nlarda kullan�m�na ili�kin yeterli ve iyi kontroll� �al��malara dayanan veri mevcut de�ildir. Hayvanlar �al��malar�, klinik olarak ilgili dozlarda �reme toksisitesi a��s�ndan direk veya indirek zararl� etkilere i�aret etmemi�tir (Bkz. 5.3). �nsanlara y�nelik potansiyel risk bilinmemektedir. T�OS�VAR, olas� yararlar fet�s �zerindeki olas� riske �st�n olmad�k�a, gebelik d�neminde kullan�lmamal�d�r.
Laktasyon d�nemi: Tiotropium brom�r�n insanlarda s�te ge�ip ge�medi�i bilinmemektedir. Laktasyondaki kemirgenlerde yap�lan �al��malarda, az miktarda tiotropiumun s�te ge�ti�i belirlenmi�tir. Bununla birlikte, T�OS�VAR emziren annelerde �nerilmez. Tiotropium brom�r uzun etkili bir maddedir. Emzirmenin kesilip kesilmeyece�i veya T�OS�VAR tedavisine devam edilip edilmeyece�i karar�, emmenin bebe�e olan yararlar� ve T�OS�VAR tedavisinin anneye yararlar� birlikte de�erlendirilerek verilmelidir.
�reme yetene�i/Fertilite: Tiotropium i�in fertilite ile ilgili klinik veri yoktur. Tiotropium ile y�r�t�len bir klinik d��� �al��mada, fertilite a��s�ndan, herhangi bir advers reaksiyon g�r�lmemi�tir (Bkz. 5.3). Tav�anlar ve s��anlardaki �reme �al��malar�nda gebelik, embriyo/fetal geil�im, do�um ve do�um sonras� geli�ime y�nelik zararl� etkiler, yaln�zca anne i�in toksik olan doz d�zeylerinde g�sterilebilmi�tir.
4.7. Ara� ve makine kullan�m� �zerindeki etkiler
Ara� ve makine kullanma becerileri �zerindeki etkilerine y�nelik bir �al��ma yap�lmam��t�r. Ba� d�nmesi ve bulan�k g�rme olaylar�n�n ortaya ��kmas�, ara� ve makine kullanma becerilerini etkileyebilir.
4.8. �stenmeyen etkiler
G�venlilik profili �zeti
Listelenmi� olan istenmeyen etkilerin �o�u, T�OS�VAR' �n antikolinerjik �zelliklerine ba�lanabilir.
Advers reaksiyonlar�n tablolu �zeti
A�a��da listelenen advers ila� reaksiyonlar� i�in belirlenen s�kl�klar, d�rt hafta ile d�rt y�l aras�nda de�i�en tedavi d�nemlerini kapsayan 28 plasebo kontroll� klinik ara�t�rmaya ait havuzun
tiotropium grubunda (9,647 hasta) g�zlenen advers reaksiyonlar�n ham (crude) insidans oranlar�na (yani, tiotropium atfedilen olaylar) dayanmaktad�r.
A�a��daki listede belirtilen istenmeyen etkilerin s�kl�k oranlar� ��yle tan�mlan�r: �ok yayg�n ≥ 1/10
Yayg�n ≥ 1/100 ilâ < 1/10
Yayg�n olmayan ≥ 1/1.000 ilâ < 1/100 Seyrek ≥ 1/10.000 ilâ < 1/1.000
�ok seyrek < 1/10.000
Bilinmiyor (eldeki verilerden hareketle tahmin edilemiyor)
Metabolizma ve beslenme hastal�klar�
Bilinmiyor: Dehidratasyon
Sinir sistemi hastal�klar�
Yayg�n olmayan: Ba� d�nmesi, ba� a�r�s�, tat alma bozukluklar� Seyrek: Uykusuzluk
G�z hastal�klar�
Yayg�n olmayan: Bulan�k g�rme
Seyrek: Glokom, g�z i�i bas�nc�nda art��
Kardiyak hastal�klar
Yayg�n olmayan: Atriyal fibrilasyon
Seyrek: Supraventrik�ler ta�ikardi, ta�ikardi, palpitasyonlar
Solunum, g���s bozukluklar� ve mediyastinal hastal�klar
Yayg�n olmayan: Farenjit, disfoni, �ks�r�k
Seyrek: Bronkospazm, burun kanamas�, larenjit, sin�zit
Gastro-intestinal hastal�klar
Yayg�n: A��z kurulu�u
Yayg�n olmayan: Stomatit, gastro�zofajiyal refl� hastal���, konstipasyon, bulant�
Seyrek: �ntestinal obstr�ksiyon (paralitik ileus dahil), gingivit, glossit, orofarenjiyal kandidiyazis, disfaji
Bilinmiyor: Di� ��r�mesi
Deri ve derialt� dokusu hastal�klar�- Ba����kl�k sistemi hastal�klar�
Yayg�n olmayan: D�k�nt�
Seyrek: A��r� duyarl�l�k reaksiyonlar� (ani reaksiyonlar dahil), �rtiker, ka��nt� Bilinmiyor: Anjiyon�rotik �dem, deri infeksiyonu ve deri �lseri, deride kuruluk
Kas-iskelet, ba� dokusu ve kemik hastal�klar�
Bilinmiyor: Eklemlerde �i�me
B�brek ve idrar hastal�klar�
Yayg�n olmayan: �drar retansiyonu, idrar yapmada g��l�k Seyrek: �drar yolu enfeksiyonu
Se�ilmi� advers reaksiyonlar�n a��klamas�
Kontroll� klinik �al��malarda yayg�n olarak g�zlenen istenmeyen etkiler, hastalar�n yakla��k
%4'�nde ortaya ��kan a��z kurulu�u gibi antikolinerjik etkilerdir. 28 klinik �al��mada tiotropium ile tedavi edilen 9.647 hastan�n 18' i (%0.2). A��z kurulu�u nedeniyle �al��may� b�rakm��t�r.
Antikolinerjik etkilerle tutarl� ciddi istenmeyen etkiler aras�nda, glokom, konstipasyon, paralitik ileus dahil intestinal obstr�ksiyon ve idrar retansiyonu bulunur.
Di�er �zel pop�lasyonlar
�lerleyen ya�la birlikte antikolinerjik etkilerde art�� g�r�lebilir.
��pheli advers reaksiyonlar�n raporlanmas�
Ruhsatland�rma sonras� ��pheli ila� advers reaksiyonlar�n�n raporlanmas� b�y�k �nem ta��maktad�r. Raporlama yap�lmas�, ilac�n yarar/risk dengesinin s�rekli olarak izlenmesine olanak sa�lar. Sa�l�k mesle�i mensuplar�n�n herhangi bir ��pheli advers reaksiyonu T�rkiye Farmakovijilans Merkezi (T�FAM)'ne bildirilmeleri gerekmektedir. (www.titck.gov.tr; e-posta: tufam@titck.gov.tr; tel: 0 800 314 00 08; faks: 0 312 218 35 99).
4.9. Doz a��m� ve tedavisi
Y�ksek dozlarda T�OS�VAR, antikolinerjik bulgu ve semptomlara yol a�abilir.
Ancak, sa�l�kl� g�n�ll�lerde 340 mikrogram tiotropium dozuna kadar inhale edilen tek doz sonras�nda, hi�bir sistemik antikolinerjik istenmeyen etki g�r�lmemi�tir. Ek olarak, sa�l�kl� g�n�ll�lerde 170 mikrogram doza kadar tiotropium brom�r�n 7 g�n uygulanmas�n� takiben a��z kurulu�u d���nda ilgili bir advers etki g�zlenmemi�tir. KOAH hastalar�nda yap�lan �oklu doz bir �al��mada, 4 hafta boyunca g�nl�k maksimum 43 mikrogram tiotropium brom�r uygulanmas� ile �nemli bir istenmeyen etki g�zlenmemi�tir.
Sa�l�kl� g�n�ll�lerde, g�nde bir kez 141 mg dozunda tekrarl� inhalasyonlar� izleyerek, a��z kurulu�u ile birlikte bilateral konjonktivit g�r�lm�� ve bu durum tedavi halen s�rmekte iken ortadan kaybolmu�tur. KOAH' � olan ki�ilerde d�rt hafta s�reyle, g�nl�k maksimum 36 mikrogram tiotropium dozlar� ile uygulanan �ok-dozlu bir �al��mada g�zlenen tiotropiuma ba�lanabilecek tek istenmeyen olay, a��z kurulu�u olmu�tur.
Tiotropium kaps�llerinin oral yoldan al�nmas� ile akut intoksikasyon pek olas� de�ildir, ��nk� oral yoldan biyoyararlan�m� d���kt�r.
 �nme
�nme, beynin hasar g�rmesinin sonucudur. Bu hasar, beynin bir k�sm�ndaki ya bir kanama
ya da akut kan eksikli�i nedeniyle o k�sm�n ge�ici ya da kal�c� olarak i�levini yapamamas�na
yol a�ar.
�nme
�nme, beynin hasar g�rmesinin sonucudur. Bu hasar, beynin bir k�sm�ndaki ya bir kanama
ya da akut kan eksikli�i nedeniyle o k�sm�n ge�ici ya da kal�c� olarak i�levini yapamamas�na
yol a�ar. |
 Deri Kanseri
Deri kanseri �ok rastlanan bir hastal�kt�r. �� ana t�r� bulunur ;genelde kemirici �lser olarak bilinen bazal h�creli karsinom, yass� h�creli karsinom ve k�t� huylu t�m�r.
Deri Kanseri
Deri kanseri �ok rastlanan bir hastal�kt�r. �� ana t�r� bulunur ;genelde kemirici �lser olarak bilinen bazal h�creli karsinom, yass� h�creli karsinom ve k�t� huylu t�m�r. |
�LA� GENEL B�LG�LER�
Grandi �la� Sanayi ve Tic.Ltd.�ti.
| Sat�� Fiyat� | TL |
| �nceki Sat�� Fiyat� | |
| Original / Jenerik | Original �la� |
| Re�ete Durumu | Normal Re�eteli bir ila�d�r. |
| Barkodu | 8680264860125 |
| Etkin Madde | Tiotropium Bromur Monohidrat |
| Yerli ve Be�eri bir ila�d�r. |
�LA� E�DE�ERLER�
| E�de�er �la� Ad� | Barkodu | �la� Fiyat� |
|---|---|---|
| E�de�er bir ila� bulunamad� |
 |
A��r� Alkol Kullan�m�, Alkolizm Alkol ba��ml�l���, alkol kullan�m� ve alkol sorunlar� aras�ndaki fark� a��klamak g��t�r. �rne�in, ge�mi�te alkol kullanm�� olan bir kimsenin mutlaka alkol ba��ml�s� olmas� gerekmez. |
 |
Rahim Boyu ( Serviks ) Kanseri Rahim boynu (serviks) kanseri 35 ya� alt� kad�nlarda g�r�len vakalarda meme kanserinden sonra ikinci s�ray� al�r.Serviks kanserinin geli�mesi y�llarca s�rebilir. |
 |
Omurilik zedelenmeleri Omurilik zedelenmesini takip eden birka� g�n i�inde, hi�kimse hasarin ne kadar olacagini tahmin edemez. Buradaki sorun, omuriligin herhangi bir zedelenmesinden hemen sonra, bir omurilik sokunun olusmasidir. |