NUMETA PED G16 %E inf�zyonluk em�lsiyon 500 ml { Baxter Renal } Farmas�tik �zellikler
{ Amino Asit + Elektrolit + Lipid + Karbonhidrat }
6. FARMAS�T�K �ZELL�KLER
6.1. Yard�mc� maddelerin listesi
Lipid em�lsiyonu odac���
Enjeksiyonluk yumurta fosfolipidleri (tavuk kaynakl�) Gliserol
Sodyum oleat
Sodyum hidroksit (pH ayar� i�in) Enjeksiyonluk su
Amino asit ��zeltisi odac��� L-Malik asit (pH ayar� i�in) Enjeksiyonluk su
Glukoz ��zeltisi odac��� Hidroklorik asit (pH ayar� i�in) Enjeksiyonluk su
6.2. Ge�imsizlikler
i�in ayr�ca B�l�m 6.2'ye bak�n�z.6.2. Ge�imsizlikler
i�in ayr�ca B�l�m 6.2'ye bak�n�z.
Herhangi bir parenteral beslenme kar���m�nda oldu�u gibi kalsiyum ve fosfat�n oran� dikkate al�nmal�d�r. A��r� kalsiyum ve fosfat eklemek, �zellikle de bunlar�n mineral tuzlar� kalsiyum fosfat �eklinde ��kelmelere neden olabilir.
Di�er kalsiyum i�eren inf�zyon ��zeltileri i�in, NUMETA PED G16%E ile seftriaksonun e� zamanl� tedavisi yenido�anlarda (28 g�nl�kten az), ayr� inf�zyon yollar� kullan�lsa bile kontrendikedir (yenido�an�n kan dola��m�nda seftriakson-kalsiyum tuzu ��kelmesi riski, bkz. B�l�m 4.5).
Her ya�taki hastada, farkl� inf�zyon yollar� veya farkl� inf�zyon b�lgeleri kullan�lsa bile, seftriakson-kalsiyum tuzu �eklinde ��kme riskinden dolay�, seftriakson, NUMETA PED G16%E de dahil olmak �zere, herhangi bir intraven�z kalsiyum i�eren ��zelti ile kar��t�r�lmamal� veya e� zamanl� olarak kullan�lmamal�d�r.
��kelme riskinden dolay�, NUMETA PED G16%E ampisilin, fosfenitoin veya furosemid ile ayn� inf�zyon yoluyla uygulanmamal�d�r.
NUMETA PED G16%E e� zamanl� olarak kanla birlikte ayn� inf�zyon setinden uygulanmamal�d�r (Bkz. B�l�m 4.5).
NUMETA PED G16%E, sitrat-antikoag�le/korunmu� kanda veya bile�enlerinde ��kelmi� ek koag�lasyon riski olu�turan kalsiyum iyonlar� i�erir.
6.3. Raf �mr�
18 ay.
Yeni do�anlarda ve iki ya��n alt�ndaki �ocuklarda kullan�ld���nda, ��zelti (torbada ve uygulama setinde) uygulama tamamlanana kadar ���k maruziyetinden korunmal�d�r (bkz. B�l�m 4.4, B�l�m 6.3 ve B�l�m 6.6.).
Rekonstit�syon sonras� raf �mr�
�ki ya da �� odac�k aras� separat�rler a��larak kar���m ger�ekle�tirildikten sonra, m�mk�n olan en k�sa s�re i�inde kullan�lmas� �nerilmektedir. Bununla birlikte odac�klar aras� separat�rler a��larak kar��t�r�ld�ktan sonra, 2°C ila 8°C aras�nda 7 g�n ve ard�ndan 30°C'de 48 saat s�reyle stabilitesini korudu�u g�sterilmi�tir.
�la� eklemeleri (elektrolitler, eser elementler, vitaminler, su) yap�ld�ktan sonraki raf �mr� Spesifik kar���mlar i�in, ila� eklendikten sonra yap�lan stabilite �al��malar�nda 2°C ila 8°C aras�nda 7 g�n ve ard�ndan 30°C'de 48 saat s�reyle stabilitesini korudu�u g�sterilmi�tir.
Mikrobiyolojik a��dan, �r�n�n hemen kullan�lmas� �nerilir. Hemen kullan�lmad��� durumda, ila� eklendikten sonraki kullan�m �ncesi saklama s�resi ve ko�ullar� uygulay�c�n�n sorumlulu�undad�r ve rekonstit�syon/seyreltme/ila� eklemeleri kontroll� ve validasyonu aseptik ko�ullarda yap�lmam��sa, �r�n 2-8°C'de 24 saatten fazla bekletilmemelidir. L�tfen ayn� zamanda B�l�m 4.2 ve B�l�m 6.6'ya bak�n�z.
6.4. Saklamaya y�nelik �zel tedbirler
25°C'nin alt�ndaki oda s�cakl���nda saklanmal�d�r. Dondurulmamal�d�r. Koruyucu d�� ambalaj� i�inde saklanmal�d�r.
6.5. Ambalaj�n niteli�i ve i�eri�i
�� odac�kl� PVC olmayan torba a�a��daki bile�enlerden olu�ur:
�ok katl� bir plastik tabaka.
Lipid em�lsiyon i�eren odac��a ili�tirilmi� k�r bir u�. Bu odac��a ekleme yap�lmas�n� engellemek i�in odac���n doldurulmas�n� takiben bu u� kapat�lm��t�r.
Amino asit ve glukoz ��zeltisi i�eren odac�klara ili�tirilmi� iki u�.
Glukoz i�eren odac���n ucunu kapatan bir enjeksiyon ucu.
Amino asit odac���n�n ucunu kapatan bir uygulama ucu.
Hi�bir bile�en do�al lateks plasti�i i�ermez.
Hava ile temas�n� engellemek i�in torba oksijen ge�irmeyen bir d�� torbayla kapl�d�r. D�� torba ile �ok katl� torba aras�nda oksijen absorban� i�eren bir sa�e bulunmaktad�r ve oksijen indikat�r� de i�erir.
6.6. Be�eri t�bbi �r�nden arta kalan maddelerin imhas� ve di�er �zel �nlemler
Tek kullan�ml�kt�r.
Hasarl� torbalar kullan�lmamal�d�r. Torban�n ve ge�ici separat�rlerin sa�laml��� kontrol edilmelidir. Amino asit ile glukoz ��zeltileri berrak, renksiz ya da hafif sar� renkteyse, partik�l i�ermiyorsa ve em�lsiyon homojen s�t g�r�n�m�ndeyse kullan�lmal�d�r.
D�� torbay� a�madan �nce oksijen indikat�r�n�n rengi kontrol edilmelidir. Bu renk "OK" sembol�n�n yan�nda bas�l� ve indikat�r etiketinin bask�l� b�l�m�nde g�sterilmi� olan renkle kar��la�t�r�lmal�d�r. Oksijen indikat�r�n�n rengi, "OK" sembol�n�n yan�nda bas�l� olan referans renkle ayn� de�ilse �r�n kullan�lmamal�d�r.
�la� eklemeleri
Yenido�anlarda ve 2 ya��n alt�ndaki �ocuklarda kullan�ld���nda uygulama tamamlanana kadar ortam �����ndan korunmal�d�r. Numeta G16%E'nin �zellikle eser elementler ve /veya vitaminlerle kar��t�r�ld�ktan sonra ortam �����na maruz kalmas�, ����a maruz kalmaktan korunarak azalt�labilen peroksitler ve di�er bozunma �r�nleri �retir (bkz. b�l�m 4.2, 4.4 ve 6.3)
Uygun eklemeler rekonstit�syonu yap�lan �r�ne enjeksiyon b�lgesinden yap�labilir (ge�ici separat�rler ayr�larak iki ya da �� odac�ktaki i�eri�in kar���m� ger�ekle�tirildikten sonra).
Vitamin eklemeler, kar���m ger�ekle�tirilmeden �nce (ge�ici separat�rler ayr�larak 3 odac�ktaki i�eri�in kar���m� ger�ekle�tirilmeden �nce) glukoz ��zeltisi i�eren odac���n i�ine de yap�labilir.
Tan�mlanm�� miktarlarda eklenme ihtimali olan, ticari olarak mevcut eser element ��zeltileri (TE1, TE2 ve TE4 olarak tan�mlanm��t�r), vitaminler (liyofilizat V1 ve em�lsiyon V2 olarak tan�mlanm��t�r) ve elektrolitler Tablo 1-6'da sunulmu�tur.
TE4, V1 ve V2 ile ge�imlilik
Tablo 1: Su ile seyreltme ile veya seyreltme olmadan ��� bir arada (Aktive 3 odac�kl� torba) ge�imlili�i
Her bir 500 mL i�in (lipidler ile 3 odac�k kar���m�) | ||||||
| Seyreltme olmadan kar���m | Seyreltme ile kar���m | ||||
Eklentiler | Mevcut seviye | Maksimum ekleme | Maksimum toplam seviye | Mevcut seviye | Maksimum ekleme | Maksimum toplam seviye |
Sodyum (mmol) | 12 | 25,6 | 37,6 | 12 | 25,6 | 37,6 |
Potasyum (mmol) | 11,4 | 26,2 | 37,6 | 11,4 | 26,2 | 37,6 |
Magnezyum (mmol) | 1,6 | 3,6 | 5,2 | 1,6 | 3,6 | 5,2 |
Kalsiyum (mmol) | 3,1 | 16,4 | 19,5 | 3,1 | 8,2 | 11,3 |
Fosfat* (mmol) | 4,4 | 6,9 | 11,3 | 4,4 | 6,9 | 11,3 |
Eser elementler & vitaminler | - | 10 mL TE4 + 1 flakon V1 + 30 mL V2 | 10 mL TE4 + 1 flakon V1 + 30 mL V2 | - | 5 mL TE4 + ½ flakon V1 + 5 mL V2 | 5 mL TE4 + ½ flakon V1 + 5 mL V2 |
Enjeksiyonluk su | - | - | - | - | 350 mL | 350 mL |
Organik fosfat
Tablo 2: Su ile seyreltme ile veya seyreltme olmadan ikisi bir arada (Aktive 2 odac�kl� torba) ge�imlili�i
Her bir 376 mL i�in (lipidler olmadan 2 odac�k kar���m�) | ||||||
| Seyreltme olmadan kar���m | Seyreltme ile kar���m | ||||
Eklentiler | Mevcut seviye | Maksimum ekleme | Maksimum toplam seviye | Mevcut seviye | Maksimum ekleme | Maksimum toplam seviye |
Sodyum (mmol) | 11,6 | 26 | 37,6 | 11,6 | 0 | 11,6 |
Potasyum (mmol) | 11,4 | 26,2 | 37,6 | 11,4 | 0 | 11,4 |
Magnezyum (mmol) | 1,6 | 3,6 | 5,2 | 1,6 | 0 | 1,6 |
Kalsiyum (mmol) | 3,1 | 8,2 | 11,3 | 3,1 | 0 | 3,1 |
Fosfat* (mmol) | 3,2 | 8,1 | 11,3 | 3,2 | 0 | 3,2 |
Eser elementler & vitaminler | - | 5mL TE4 + ½ flakon V1 | 5mL TE4 + ½ flakon V1 | - | 5mL TE4 + ½ flakon V1 | 5mL TE4 + ½ flakon V1 |
Enjeksiyonluk su | - | - | - | - | 450 mL | 450 mL |
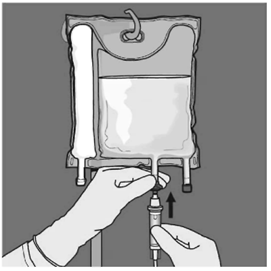
Basamak: Uygulama ucundaki koruyucu kapak ��kar�larak intraven�z uygulama seti buraya yerle�tirilmelidir.
Kullan�lmam�� olan �r�nler ya da at�k materyaller “T�bbi �r�nlerin Kontrol�” y�netmeli�i ve “Ambalaj ve Ambalaj At�klar�n�n Kontrol�” y�netmeli�ine uygun olarak imha edilmelidir.
 Belso�uklu�u, Chlamydia ve Frengi
Belso�uklu�u, bakterilerin sebep oldu�u bir enfeksiyondur. Cinsel ili�ki
yoluyla bula��r ve d�lyata�� boynunda, idrar yollar�nda, an�ste, makatta ve
bo�azda enfeksyona sebep olabilir.
Belso�uklu�u, Chlamydia ve Frengi
Belso�uklu�u, bakterilerin sebep oldu�u bir enfeksiyondur. Cinsel ili�ki
yoluyla bula��r ve d�lyata�� boynunda, idrar yollar�nda, an�ste, makatta ve
bo�azda enfeksyona sebep olabilir. |
 Mide Kanseri
Mide kanseri genellikle mideyi t�m�yle kaplayan ve mukus �retmekle g�revli h�crelerde ba�lar. Bu kanser tipine adenokarsinom denir.
Mide Kanseri
Mide kanseri genellikle mideyi t�m�yle kaplayan ve mukus �retmekle g�revli h�crelerde ba�lar. Bu kanser tipine adenokarsinom denir. |
�LA� E�DE�ERLER�
| E�de�er �la� Ad� | Barkodu | �la� Fiyat� |
|---|---|---|
| CLINIMIX | 8699556696809 | |
| EVILO | 8699606887478 | |
| KABIVEN | 8699630697180 | 1,241.30TL |
| NEONUTRIVEN | 8697637691897 | |
| NUMETA | 8681413881428 | |
| Di�er E�de�er �la�lar |
 |
Do�um Sonras� Depresyonu Do�um sonras� depresyonu, do�umdan sonra her on kad�ndan biri taraf�ndan tecr�be edilen stresli bir durumdur. |
 |
�izofrenlik �izofrenli�in psikiatrik te�hisi hakk�nda �ok fazla anla�mazl�k vard�r. Bu sayfadaki bilgiler, �izofrenli�in te�hisi, nedenleri ve tedavisi hakk�ndaki fakl� teoriler hakk�nda bilgi verecektir. |
 |
Mesane Kanseri Mesane kanseri her zaman mukozada ba�lar. Erken safhalarda bu tabakada s�n�rl� kal�r ve h�cre i�indeki karsinom olarak nitelendirilir. |
�LA� GENEL B�LG�LER�
Baxter Turkey Renal Hizmetler A.�.
| Sat�� Fiyat� | 4996.15 TL [ 4 May 2026 ] |
| �nceki Sat�� Fiyat� | 4996.15 TL [ 27 Apr 2026 ] |
| Original / Jenerik | Original �la� |
| Re�ete Durumu | Normal Re�eteli bir ila�d�r. |
| Barkodu | 8681413881107 |
| Etkin Madde | Amino Asit + Elektrolit + Lipid + Karbonhidrat |
| ATC Kodu | B05BA10 |
| Birim Miktar | 500 |
| Birim Cinsi | ML |
| Ambalaj Miktar� | 1 |
| Kan ve Kan Yap�c� Organlar > Damar ��ine Enjekte Edilenler > Beslenme Serumu Kombinasyonlar� |
| �thal ( ref. �lke : Italya ) ve Be�eri bir ila�d�r. |