OSIREC 4 G /60 G 7 rektal süspansiyon Kısa Ürün Bilgisi
{ Mesalazin }
1. BEŞERİ TIBBİ ÜRÜNÜN ADI
OSİREC® 4 g/60 ml rektal süspansiyon
2. KALİTATİF VE KANTİTATİF BİLEŞİM
Etkin madde
Her bir rektal süspansiyon (60 ml süspansiyon), etkin madde olarak 4 g mesalazin içerir.
Yardımcı maddeler
Sodyum benzoat (E211)… 0,0600 g
Potasyum metabisülfit (E224)… 0,2808 g
Yardımcı maddeler için 6.1' e bakınız.
3. FARMASÖTİK FORMU
Rektal Süspansiyon
OSİREC®, açık-mat kahverengiye yakın krem renkte homojen süspansiyondur.
4. KLİNİK ÖZELLİKLER
4.1. Terapötik endikasyonlar
Ülseratif kolitin (kalın bağırsaktaki bir kronik inflamatuvar hastalık) akut ataklarının tedavisinde endikedir.
4.2. Pozoloji ve uygulama şekli
Pozoloji/uygulamasıklığı ve süresi:
Yetişkinler:
Akut inflamasyon olan hastalarda, bir süspansiyon şişesinin (60 ml rektal süspansiyon) içeriği yatmadan önce lavman olarak bir defada bağırsağa uygulanır.
En iyi sonuç OSİREC® uygulamasından önce bağırsaklar boşaltıldığında elde edilir. OSİREC®, düzenli ve devamlı kullanılmalıdır, çünkü başarılı bir iyileşme ancak bu şekilde sağlanabilir.
Kullanım süresi doktor tarafından belirlenir.
Uygulama şekli:
Rektal kullanım. OSİREC® rektal süspansiyon günde bir defa yatmadan önce uygulanır.
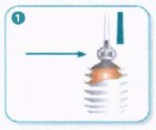
Hazırlanışı:
30 saniye boyunca şişe çalkalanır.
Aplikatörün koruyucu kapağı çıkarılır.
Şişe alttan ve üstten tutulur.
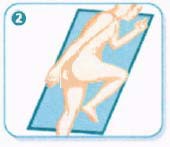
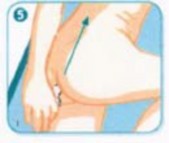
Uygulama için doğru pozisyon:
Hasta sol tarafının üzerine sol bacağını uzatıp sağ bacağını karnına doğru çekerek uzanır. Bu pozisyonla OSİREC® daha kolay uygulanır ve daha etkili olur.
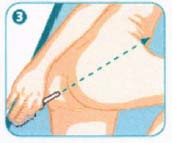
Rektal süspansiyonun uygulanması:
Aplikatörün ucu rektumun içine sokulur.
Şişenin ucu hafif aşağı bakacak şekilde eğilir ve yavaşça sıkılır.
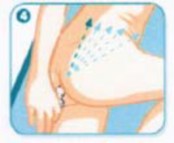
Kullanıldıktan sonra boş şişenin aplikatör ucu yavaşça rektumdan çıkarılır.
İlacın rektumda dengeli bir şekilde dağılımının sağlanması için ilacın uygulandığı yatar pozisyon, 30 dakika süre ile korunmalıdır.
Mümkünse, rektal süspansiyonun gece boyunca etki sağlamasına izin verilmelidir.
Özel popülasyonlara ilişkin ek bilgiler:
Böbrek/Karaciğer yetmezliği:
Karaciğer fonksiyon bozukluğu olan hastalarda dikkatli kullanılmalıdır.
Böbrek fonksiyonları bozuk olan hastalarda kullanılması önerilmez. Tedavi sırasında böbrek fonksiyonları bozulursa, mesalazinin yol açtığı renal toksisite düşünülmelidir.
Şiddetli böbrek ve karaciğer yetmezliği olan hastalarda kontrendikedir.
Pediyatrik popülasyon:
OSİREC®'in çocuklarda etkili olduğuna dair çok az deneyim ve sınırlı sayıda doküman vardır.
Geriyatrik popülasyon:
Yetişkinler için verilen pozoloji ve uygulama şekli geriyatrik popülasyon için de geçerlidir.
4.3. Kontrendikasyonlar
OSİREC® aşağıdaki durumlarda kontrendikedir:
Etkin madde
4.4. Özel kullanım uyarıları ve önlemleri
Tedaviye başlamadan önce ve tedavi sırasında hekimin isteğine göre kan testleri (diferansiyel kan sayımı; ALT veya AST gibi karaciğer fonksiyon testleri; serum kreatinin) ve idrar muayenesi (dipstick test) yapılmalıdır. Kılavuz olarak, kontroller tedaviye başlandıktan 14 gün sonra yapılmalı ve 4 haftalık aralarla 2-3 kez tekrarlanmalıdır.
Bulgular normal ise, tedavi sonrası kontroller 3 aylık aralarla yapılabilir. Eğer ilave belirtiler gelişirse, kontrol muayeneleri hemen yapılmalıdır.
Karaciğer fonksiyon bozukluğu olan hastalarda dikkatli kullanılmalıdır.
Böbrek fonksiyonları bozuk olan hastalarda kullanılması önerilmez. Tedavi sırasında böbrek fonksiyonları bozulursa, mesalazinin yol açtığı renal toksisite düşünülmelidir.
Mesalazin kullanımı ile %100 mesalazin içerikli taşlar içeren nefrolitiazis vakaları rapor edilmiştir. Tedavi sırasında yeterli sıvı alımının sağlanması önerilir.
Özellikle astım olmak üzere akciğer hastalığı olan hastalar OSİREC® tedavisi sırasında çok dikkatli bir şekilde izlenmelidir.
Sülfasalazin içeren ilaçlarla yan etki görülme öyküsü olan hastalarda, OSİREC® tedavisine yalnızca dikkatli bir hekim muayenesi ile başlanmalıdır. OSİREC® abdominal kramplar, akut karın ağrısı, ateş, şiddetli baş ağrısı ve deride döküntü gibi akut intolerans reaksiyonlarına neden olursa tedavi hemen kesilmelidir.
OSİREC®, 0,2808 g potasyum metabisülfit içerir. Bu nedenle, özellikle astım hastasıysanız veya alerji öykünüz varsa, nadir olarak şiddetli aşırı duyarlılık reaksiyonlarına ve bronkospazma (bronşların daralması) neden olabilir.
OSİREC®, sodyum benzoat içerir. Bu nedenle deriye, göze ve mukoz membranlarına hafif derecede irritan (tahriş edici) olabilir.
4.5. Diğer tıbbi ürünler ile etkileşimler ve diğer etkileşim şekilleri
Karşılıklı etkileşime ilişkin özel araştırmalar yapılmamıştır.
Mesalazin beraberinde azatiyoprin, 6-merkaptopürin ya da tioguanin ile tedavi görmekte olan hastalarda, azatiyoprinin, 6-merkaptopürinin ya da tioguaninin miyelosüpresif etkilerinde olası artış dikkate alınmalıdır.
Mesalazinin, varfarinin antikoagülan etkisini azaltmasına ilişkin zayıf kanıt vardır.
Özel popülasyonlara ilişkin ek bilgiler Pediyatrik popülasyon:
OSİREC®'in çocuklarda etkili olduğuna dair çok az deneyim ve sınırlı sayıda doküman vardır.
4.6. Gebelik ve laktasyon
Gebelik kategorisi B'dir.
Çocuk doğurma potansiyeli bulunan kadınlar/Doğum kontrolü (Kontrasepsiyon) OSİREC®'in çocuk doğurma potansiyeli bulunan kadınlara herhangi bir etkisi veya doğum kontrolü (kontrasepsiyon) için kullanılan ilaçlarla herhangi bir etkileşimi bildirilmemiştir.
Gebelik dönemi
OSİREC®'in gebe kadınlarda kullanımına ilişkin yeterli veri yoktur. Sınırlı sayıda gebelikte maruz kalma olgularına ilişkin veriler, mesalazinin gebelik üzerinde ya da fetüs/yenidoğan çocuğun sağlığı üzerinde advers etkileri olduğunu göstermemektedir. Bugüne kadar herhangi önemli bir epidemiyolojik veri elde edilmemiştir.
Oral yol ile alınan mesalazinde hayvanlar üzerinde yapılan çalışmalar, gebelik/embriyonal/fetal gelişim/doğum ya da doğum sonrası gelişim ile ilgili olarak doğrudan ya da dolaylı zararlı etkiler olduğunu göstermemektedir.
İzole tek bir vakada gebelik sırasında yüksek mesalazin dozunun uzun süreli uygulanması neticesinde (2-4 g/gün, oral) yeni doğanda böbrek yetmezliği bildirilmiştir.
OSİREC®, gebelik sırasında ancak beklenen faydanın potansiyel riskten fazla olması halinde uygulanmalıdır.
Laktasyon dönemi
N-asetil-5-amino salisilik asit ve daha az miktarda mesalazin anne sütüne geçmektedir. Mesalazinin kadınlarda emzirme dönemine etkisi ile ilgili sınırlı deneyim mevcuttur. Diyare gibi aşırı duyarlılık reaksiyonları emzirilen bebeklerde gözardı edilemez. Emzirmenin durdurulup durdurulmayacağına ya da OSİREC® tedavisinin durdurulup durdurulmayacağına/tedaviden kaçınılıp kaçınılmayacağına ilişkin karar verilirken, emzirmenin çocuk açısından faydası ve OSİREC® tedavisinin emziren anne açısından faydası dikkate alınmalıdır. Emzirilen bebekte diyare gelişirse emzirmeye son verilmelidir.
Üreme yeteneği/Fertilite
İnsanlarda üreme yeteneği/fertilite üzerine etkisi bilinmemektedir.
4.7. Araç ve makine kullanımı üzerindeki etkiler
OSİREC®'in araç ve makine kullanma yeteneği üzerinde hiçbir etkisi görülmemiş ya da ihmal edilebilir düzeyde etki görülmüştür.
4.8. İstenmeyen etkiler
Mesalazin uygulandıktan sonra aşağıdaki istenmeyen etkiler gözlenmiştir:
Çok yaygın: (≥1/10) Yaygın: (≥1/100 - <1/10)
Yaygın olmayan: (≥1/1000 - 1/100) Seyrek: (≥1/10.000 - 1/1000)
Çok seyrek: (<1/10.000) (istisnai raporlar dahildir) Bilinmiyor: Eldeki verilerden hareketle tahmin edilemiyor.
Kan ve lenf sistemi hastalıkları
Çok seyrek: Bozulan kan sayımı (aplastik anemi, agranülositoz, pansitopeni, nötropeni, lökopeni, trombositopeni)
Bağışıklık sistemi hastalıkları
Çok seyrek: Alerjik egzantem, ilaç ateşi, lupus eritomatozus sendromu, pankolit gibi hipersensitivite reaksiyonları
Sinir sistemi hastalıkları Seyrek: Baş ağrısı, sersemlik Çok seyrek: Periferal nöropati
Kardiyak hastalıklar
Seyrek: Miyokardit, perikardit
Solunum, göğüs bozuklukları ve mediastinal hastalıkları
Çok seyrek: Alerjik ve fibrotik akciğer reaksiyonları (dispne, öksürük, bronkospazm, alveolit, pulmoner eozinofili, akciğer infiltrasyonu, pnömoni)
Gastrointestinal hastalıklar
Seyrek: Karın ağrısı, diyare, gaz, bulantı, kusma, konstipasyon Çok seyrek: Akut pankreatit
Hepatobiliyer hastalıklar
Çok seyrek: Karaciğer fonksiyon testlerinde değişiklikler (transaminazlarda ve kolestaz parametrelerinde artış), hepatit, kolestatik hepatit
Deri ve deri altı doku hastalıkları
Seyrek: Işığa duyarlılık* Çok seyrek: Alopesi
*Işığa duyarlılık
Atopik dermatit ve atopik egzama gibi önceden var olan cilt rahatsızlığı olan hastalarda daha ciddi reaksiyonlar bildirilmiştir.
Kas-iskelet, bağ dokusu bozuklukları ve kemik hastalıkları
Çok seyrek: Miyalji, artralji
Böbrek ve idrar yolu hastalıkları
Çok seyrek: Akut ve kronik intersitisyel nefrit ve böbrek yetmezliğini içeren böbrek fonksiyon bozuklukları
Bilinmiyor: Nefrolitiazis (ilave bilgi için bkz. Bölüm 4.4).
Üreme sistemi hastalıkları
Çok seyrek: Oligospermi (geri dönüşümlü)
Şüpheli advers reaksivonların raporlanması
Ruhsatlandırma sonrası şüpheli ilaç advers reaksiyonlarının raporlanması büyük önem taşımaktadır. Raporlama yapılması, ilacın yarar/risk dengesinin sürekli olarak izlenmesine olanak sağlar. Sağlık mesleği mensuplarının herhangi bir şüpheli advers reaksiyonu Türkiye Farmakovijilans Merkezi (TÜFAM)'ne bildirmeleri gerekmektedir. (www.titck.gov.tr; e-posta: tufam@titck.gov.tr; Tel: 0 800 314 00 08; Faks: 0 312 218 35 99)
4.9. Doz aşımı ve tedavisi
Aşırı doz üzerine (örneğin oral olarak aşırı dozda mesalazin ile intihar teşebbüsü) renal veya hepatik toksisite göstermeyen seyrek veriler vardır. Özel bir antidotu yoktur, tedavi semptomatik ve destekleyicidir.
5. FARMAKOLOJİK ÖZELLİKLER
5.1. Farmakodinamik özellikler
Farmakoterapötik grup: Bağırsak içi antienflamatuvar ajanlar; aminosalisilik asit ve benzeri ajanlar
ATC kodu: A07EC02
Etki mekanizması
Antienflamatuvar etki mekanizması bilinmemektedir. İn vitro çalışmaların sonuçları lipoksijenaz inhibisyonunun etkili olabileceğini göstermektedir.
Bağırsak mukozasındaki prostaglandin konsantrasyonları üzerine etkisi de gösterilmiştir. Mesalazin (5-Aminosalisilik asit/5-ASA) reaktif oksijen bileşenlerin radikal tutucusu olarak da etki göstermektedir.
Farmakodinamik etkiler
Rektal yol ile uygulanan mesalazin, bağırsağın luminal bölümüne eriştiğinde, bağırsağın mukoza ve submukoza dokusunda büyük oranda lokal etki gösterir.
5.2. Farmakokinetik özellikler
Emilim:
Mesalazin emilimi en yüksek oranda bağırsağın proksimal bölgelerinde, en düşük oranda da bağırsağın distal bölgelerinde gerçekleşir.
Kararlı durum koşulları altında remisyondaki ülseratif kolitli hastaların üzerinde yapılan bir çalışmada, pik plazma konsantrasyonlarına (0.92 mikrogram/ml 5-ASA ve 1.62 mikrogram/ml N-Ac-5-ASA) yaklaşık 11-12 saat sonra ulaşılmıştır.
OSİREC® ile tedavi edilen kronik enflamatuvar bağırsak hastalığı olan çocuklarda kararlı durum plazma konsantrasyonları; 0,5-2,8 mikrogram/ml 5-ASA ve 0,9-4,1 mikrogram/ml N-Ac-5-ASA'dır.
Dağılım:
Hafif – orta dereceli akut ülseratif kolitli hastalarda yapılan bir görüntüleme çalışması, tedavinin başlangıcında ve 12 hafta sonra remisyonunda rektal süspansiyonun çoğunlukla rektum, sigmoid kolon ve daha az olmak üzere kolonun geri kalanına dağıldığını göstermiştir.
Biyotransformasyon:
Mesalazin presistemik olarak bağırsak mukozasında ve karaciğerde farmakolojik açıdan inaktif metaboliti olan N-asetil-5-aminosalisilik asite (N-Ac-5-ASA) dönüşür. Asetilasyon, hastanın asetilatör fenotipinden bağımsız olarak gerçekleşmektedir. Bazı asetilasyon işlemleri kalın bağırsak bakterileri tarafından oluşmaktadır. Mesalazin ve N-Ac-5-ASA'nın proteine bağlanma oranları sırasıyla %43 ve %78'dir.
Eliminasyon:
Mesalazin ve metaboliti olan N-Ac-5-ASA feçes (büyük kısmı) ile birlikte renal (miktarı uygulama şekline, farmasötik formuna ve mesalazinin salınma yoluna bağlı olarak %20-
%50 arasında değişir) ve biliyer (küçük bir kısmı) yollarıyla atılmaktadır. Renal atılım temelde N-Ac-5-ASA şeklinde gerçekleşir. Ağız yoluyla toplam uygulanan mesalazin dozunun yaklaşık %1'i temelde N-Ac-5-ASA şeklinde anne sütüne geçer. Mesalazinin eliminasyon oranı; en çok elimine edilen (yaklaşık %85) metabolit formundaki N-Ac-5- ASA ile yaklaşık %13'tür (45 saatlik değer).
Doğrusallık/Doğrusal olmayan durum: Veri yoktur.
5.3. Klinik öncesi güvenlilik verileri
İyi rektal tolerans gösteren köpekler üzerindeki lokal tolerans çalışması dışında OSİREC® ile preklinik çalışmalar yapılmamıştır.
Güvenlilik farmakolojisi, genotoksisite, karsinojenite (sıçanlarda) veya üreme toksisitesi çalışmalarından elde edilen preklinik veriler, insanlar için özellikli bir tehlike göstermemiştir.
Toksisite çalışmalarında, mesalazinin oral olarak yüksek dozda tekrarlı uygulanmasından sonra böbrek toksisitesi (böbrek papiller nekrozu ve tüm nefron veya proksimal kıvrımlı (pars convoluta) tübüllerinin epitelyal hasarı) gözlenmiştir. Bu bulguların klinik önemi bilinmemektedir.
6. FARMASÖTİK ÖZELLİKLER
6.1. Yardımcı maddelerin listesi
Sodyum benzoat (E 211) Sodyum EDTA
Potasyum metabisülfit (E 224) [maksimum 0,28 g = maksimum 0,16 SO'ye eşdeğer] Potasyum asetat
Karbomer 974 P Ksantan gam Saf su
6.2. Geçimsizlikler
Geçerli değil.
6.3. Raf ömrü
24 ay
6.4. Saklamaya yönelik özel tedbirler
25°C'nin altındaki oda sıcaklığında saklayınız. Orijinal paketinde saklayınız ve ışıktan koruyunuz.
6.5. Ambalajın niteliği ve içeriği
7 adet mavi koruyucu HDPE kapak ile yuvarlak beyaz akordeon biçimli LDPE şişe içeren karton kutuda ambalajlanır.
6.6. Beşeri tıbbi üründen arta kalan maddelerin imhası ve diğer özel önlemler
Kullanılmamış olan ürünler ya da materyaller "Tıbbi Atıkların Kontrolü Yönetmeliği" ve "Ambalaj Atıklarının Kontrolü Yönetmeliği"ne uygun olarak imha edilmelidir.
 Mide Kanseri
Mide kanseri genellikle mideyi tümüyle kaplayan ve mukus üretmekle görevli hücrelerde başlar. Bu kanser tipine adenokarsinom denir.
Mide Kanseri
Mide kanseri genellikle mideyi tümüyle kaplayan ve mukus üretmekle görevli hücrelerde başlar. Bu kanser tipine adenokarsinom denir. |
 İnme
İnme, beynin hasar görmesinin sonucudur. Bu hasar, beynin bir kısmındaki ya bir kanama
ya da akut kan eksikliği nedeniyle o kısmın geçici ya da kalıcı olarak işlevini yapamamasına
yol açar.
İnme
İnme, beynin hasar görmesinin sonucudur. Bu hasar, beynin bir kısmındaki ya bir kanama
ya da akut kan eksikliği nedeniyle o kısmın geçici ya da kalıcı olarak işlevini yapamamasına
yol açar. |
İLAÇ EŞDEĞERLERİ
| Eşdeğer İlaç Adı | Barkodu | İlaç Fiyatı |
|---|---|---|
| ASAMESA | 8699819911311 | 886.13TL |
| ASAZIN | 8699293925972 | 1,193.71TL |
| E.S. | 8680400771124 | |
| ENCOLİT | ||
| MESAFALK | 8681801920999 | 1,053.04TL |
| Diğer Eşdeğer İlaçlar |
 |
Kalp Krizi Kalbe giden kan akışı durduğunda kalp krizi meydana gelir. |
 |
Doğum Sonrası Depresyonu Doğum sonrası depresyonu, doğumdan sonra her on kadından biri tarafından tecrübe edilen stresli bir durumdur. |
 |
Ağız Kanseri Ağız kanserinin en yaygın türleri, dudak, dil, dişetidir. Nadiren yanak içi veya damak bölgelerini de içine alır. |
İLAÇ GENEL BİLGİLERİ
MCG PHARMA İLAÇ SANAYİ VE TİCARET LİMİTED ŞİRKETİ
| Geri Ödeme Kodu | A17598 |
| Satış Fiyatı | 1105.7 TL [ 4 May 2026 ] |
| Önceki Satış Fiyatı | 1105.7 TL [ 27 Apr 2026 ] |
| Original / Jenerik | Original İlaç |
| Reçete Durumu | Normal Reçeteli bir ilaçdır. |
| Barkodu | 8681807005188 |
| Etkin Madde | Mesalazin |
| ATC Kodu | A07EC02 |
| Birim Miktar | 4 |
| Birim Cinsi | G |
| Ambalaj Miktarı | 7 |
| Sindirim Sistemi ve Metabolizma > Barsak Antienflamatuarları > Mesalazin |
| Yerli ve Beşeri bir ilaçdır. |