TOBLAIR 300 mg/5 ml nebulizasyon ��zeltisi (56 amp�l) K�sa �r�n Bilgisi
{ Tobramisin }
1. BE�ER� TIBB� �R�N�N ADI
TOBLA�R 300 mg/5 ml neb�lizasyon ��zeltisi Steril
2. KAL�TAT�F VE KANT�TAT�F B�LE��M
Etkin madde
Her 5 ml'lik �i�ede; Tobramisin… 300 mg
Tobramisin ipek b�ce�i ve bal�ktan elde edilmektedir.
Yard�mc� maddeler
Yard�mc� maddeler i�in 6.1'e bak�n�z.
3. FARMAS�T�K FORMU
Neb�lizasyon ��zeltisi i�eren �i�e Berrak ve hafif sar� renkli sulu ��zelti
Bir elinizle alt�n� tutarak ve di�er elinizle �i�enin �st�n� �evirerek TOBLA�R �i�esini a��n�z.
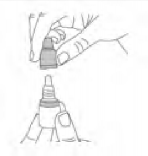
Il�k suyla g�zelce durulay�n�z.
Kullan�lmam�� TOBLA�R ��zeltisini, kullan�mdan hemen sonra neb�liz�r�n�zden temizlemelisiniz. Neb�liz�r�n i� k�sm�nda TOBLA�R kuruyup kal�rsa, temizlemek olduk�a g�� olacakt�r.
4. KL�N�K �ZELL�KLER
4.1. Terap�tik endikasyonlar
6 ya� ve �st�ndeki kistik fibroz (KF) hastalar�nda Pseudomonas aeruginosa'ya ba�l� kronik akci�er enfeksiyonunun tedavisinde endikedir.
4.2. Pozoloji ve uygulama �ekli
TOBLA�R solunum yoluyla kullan�lmak �zere haz�rlanm��t�r ve parenteral kullan�m i�in uygun de�ildir.
Pozoloji/uygulama s�kl��� ve s�resi:
Kullan�lacak TOBLA�R dozu ya� ve kiloya bak�lmaks�z�n t�m hastalarda ayn�d�r. Yeti�kinler ve �ocuklar (6 ya� ve �zeri) i�in �nerilen doz, 28 g�n boyunca g�nde iki kez bir �i�edir (tek kullan�ml�k 5 ml'lik �i�eler). Doz aral��� m�mk�n oldu�unca 12 saat olmal� ve 6 saatten az olmamal�d�r. 28 g�nl�k tedaviden sonra, hastalar TOBLA�R tedavisine m�teakip 28 g�n ara vermelidir. 28 g�nl�k aktif tedavi ve 28 g�nl�k dinlenme devreleri tekrarlanmal�d�r.
Kontroll� klinik �al��malarda tobramisin doz rejimi
D�ng� 1 | D�ng� 2 | D�ng� 3 | |||
28 G�n | 28 G�n | 28 G�n | 28 G�n | 28 G�n | 28 G�n |
G�nde 2 kere |
| G�nde 2 kere |
| G�nde 2 kere |
|
tobramisin | Standart | tobramisin | Standart | tobramisin | Standart |
tedavisi + | bak�m | tedavisi | bak�m | tedavisi | bak�m |
standart bak�m |
| + standart bak�m |
| + standart bak�m |
|
*Standart bak�m: Kistik fibrozlu hastalar�n tedavisinde standart olarak kullan�lan oral veya parenteral antips�domonal antibiyotikleri, betaagonistleri, kromolini, inhale kortikosteroidleri, hava yollar�n� temizlemeye y�nelik teknikleri i�ermektedir. Ek olarak hastalar�n yakla��k %77'si dornaz alfa kullanmaktad�r.
Alt� ya��ndan daha k���k hastalarda, beklenen FEV'i (1 saniyede zorlu ekspiratuvar hacim)
<%25 veya >%75 olan hastalarda veya Burkholderia cepacia kolonizasyonu olan hastalarda g�venlilik ve etkililik g�sterilmemi�tir.
Tedaviye kistik fibroz tedavisinde deneyimli bir hekim taraf�ndan ba�lanmal�d�r. TOBLA�R tedavisine, hekim hastan�n TOBLA�R tedavisinden klinik yarar sa�lad���n� d���nd��� s�rece belirtilen devreler �eklinde devam edilmelidir. Akci�erlerde klinik olarak k�t�le�me s�z konusuysa ayr�ca antips�domonal tedavi uygulanmal�d�r.
Klinik �al��malar, ilaca kar�� in vitro diren� g�sterildi�ini belirten mikrobiyolojik raporlar bulunsa bile hastalar�n klinik a��dan fayda g�rebildi�ini g�stermektedir.
Uygulama �ekli:
TOBLA�R, folyo i�inde yer alan, her biri 300 mg tobramisin i�eren tek dozluk, kullan�ma haz�r �i�eler �eklinde sat�l�r. Bir TOBLA�R �i�esinin i�eri�i neb�liz�re bo�alt�l�r, sonra elle kullan�lan PARI LC PLUS tekrar kullan�labilir tip neb�liz�r ve uygun bir kompres�r ile yakla��k 15 dakika solunur. Kompres�r�n uygun say�lmas� i�in PARI LC PLUS neb�liz�re tak�ld���nda 4-6 litre/dakika ak�� h�z� ve/veya 110-217 kPa geri bas�n� sa�lamas� gerekir. �reticilerin neb�liz�r ve kompres�r bak�m�na ve kullan�m�na ili�kin talimatlar� yerine getirilmelidir. Tobramisinin PARI LC PLUS d���ndaki neb�liz�rlerle birlikte kullan�lmas� yeterince ara�t�r�lmam��t�r.
Hastalar dik otururken veya ayakta dururken ve neb�liz�r�n a��zl���ndan normal nefes al�rken TOBLA�R solunmal�d�r. Hastalar�n a��zlar�ndan nefes almas�na yard�mc� olmas� i�in burun klipsleri kullan�labilir. Hastalar kendi standart g���s fizyoterapisi doz rejimlerine devam etmelidir. Klinik a��dan gerekli g�r�ld��� takdirde uygun bronkodilat�rler kullanmaya devam edilmelidir. Hastalar solunum sistemine do�rudan etkili birden fazla tedavi g�r�yorsa bunlar�n a�a��da belirtilen s�raya g�re uygulanmas� tavsiye edilir:
Bronkodilat�r,
�i�enin t�m i�eri�ini neb�liz�r�n alt k�sm�na bo�alt�n�z.
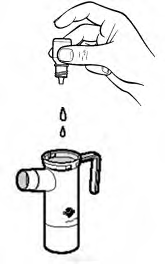
Neb�liz�r�n par�alar�n� kurumaya b�rak�n�z veya temiz, liflenmeyen bir bezle siliniz. T�m par�alar kurudu�unda, tekrar bir araya getirip neb�liz�r�n�z� kald�r�n�z.
4.3. Kontrendikasyonlar
TOBLA�R aminoglikozidlerden herhangi birine kar�� a��r� duyarl�l��� oldu�u bilinen hastalarda kontrendikedir.
4.4. �zel kullan�m uyar�lar� ve �nlemleri
Ototoksisite:
Parenteral yoldan aminoglikozid uygulanan hastalarda hem i�itsel (i�itme kayb�) hem de vestib�ler toksisite olarak ortaya ��kan ototoksisite bildirilmi�tir. Vestib�ler toksisite belirtileri aras�nda vertigo, ataksi veya sersemlik bulunabilir. Tinnitus, ototoksisitenin ba�lang�� bulgusu olabilir ve bu nedenle bu semptomun ortaya ��kmas� �nlem al�nmas�n� gerektirir.
Klinik �al��malarda tobramisin tedavisi s�ras�nda i�itme kayb� �ikâyeti veya odyometrik incelemelerle saptanan ototoksisite g�zlenmemi�tir. Pazarlama sonras� deneyimlerde, tobramisin kullanan hastalarda i�itme kayb� bildirilmi�tir. Bunlardan baz�lar� �nceden veya e� zamanl� sistemik aminoglikozid tedavisi g�rm�� hastalarda bildirilmi�tir. ��itme kayb� olan hastalarda tinnitus s�kl�kla bildirilmi�tir.
Bilinen veya ��pheli bir i�itsel ya da vestib�ler disfonksiyonu olan hastalara TOBLA�R re�ete edilirken dikkatli olunmal�d�r. Hekimler, aminoglikozidlerin vestib�ler veya kohlear toksisiteye yol a�ma potansiyelini dikkate almal� ve TOBLA�R tedavisi s�ras�nda i�itme ile ilgili i�levleri uygun �ekilde �l�melidirler. �nceden uzun s�reli sistemik aminoglikozid tedavisine ba�l� olarak risk bulunan hastalarda, TOBLA�R tedavisine ba�lanmadan �nce odyolojik de�erlendirme yap�lmas� gerekebilir.
Kulak ��nlamas�n�n ba�lamas� �nemli bir uyar�d�r, ��nk� ototoksisitenin uyar�c� belirtilerinden biridir. E�er bir hasta aminoglikozid tedavisi s�ras�nda kulak ��nlamas� veya i�itme kayb� �ikâyeti bildirirse hekim odyolojik inceleme yapt�rmal�d�r. Ayn� zamanda parenteral aminoglikozid tedavisi g�ren hastalar, k�m�latif toksisite riski dikkate al�narak klinik a��dan uygun �ekilde g�zlenmelidir. Serum tobramisin konsantrasyonlar�n�n takibi ile ilgili olarak “Laboratuvar testi ve takibi” b�l�m�ne bak�n�z.
Nefrotoksisite:
Parenteral aminoglikozid tedavisinde nefrotoksisiteye rastlanm��t�r, ancak tobramisin ile yap�lan klinik �al��malar s�ras�nda nefrotoksisite kan�t�na rastlanmam��t�r. TOBLA�R, b�brek fonksiyon bozuklu�u bilinen veya ��phelenilen hastalarda dikkatli kullan�lmal�d�r ve tobramisin serum konsantrasyonlar� g�zlenmelidir. Serum tobramisin konsantrasyonlar�n�n takibi ile ilgili olarak “Laboratuvar testi ve takibi” b�l�m�ne bak�n�z.
�iddetli b�brek yetmezli�i olan hastalar, �rne�in serum kreatinini 2 mg/dl (176,8 µmol/l)'nin �zerinde olanlar, klinik �al��malara dahil edilmemi�tir.
Mevcut klinik uygulamalara g�re, b�brek fonksiyonunun alt s�n�r� incelenmelidir. Tamamlanan her alt� TOBLA�R tedavi devresinin ard�ndan (180 g�nl�k neb�liz�r ile uygulanan aminoglikozid tedavisi) �re ve kreatinin de�erleri tekrar de�erlendirilmelidir. Nefrotoksisiteyi g�steren bir kan�t bulunursa, serum konsantrasyonlar� 2 mcg/ml'nin alt�na d��ene kadar t�m tobramisin tedavisi durdurulmal�d�r. Daha sonra hekimin g�r���ne g�re TOBLA�R tedavisine devam edilebilir. TOBLA�R ve beraberinde parenteral aminoglikozid tedavisi g�ren hastalar k�m�latif toksisite riski dikkate al�narak klinik a��dan uygun �ekilde g�zlenmelidir.
Klinik olarak gerekli g�r�ld���nde de b�brek fonksiyonuna ili�kin laboratuvar testleri yap�lmal�d�r.
Laboratuvar testleri ve takibi - serum konsantrasyonlar�:
Bilinen veya ��pheli i�itsel veya renal fonksiyon bozuklu�u olan hastalarda serum tobramisin konsantrasyonlar�n�n takip edilmesi gerekir. TOBLA�R kullanan hastalarda ototoksisite veya nefrotoksisite g�r�lmesi halinde serum konsantrasyonlar� 2 mcg/ml'nin alt�nda d��ene kadar tobramisin tedavisinin kesilmesi gerekir.
B�brek fonksiyonlar� normal olan ve TOBLA�R tedavisi g�ren hastalarda serum tobramisin konsantrasyonlar�n�n doz uygulamas�ndan bir saat sonra yakla��k 1 mcg/ml olmas� gerekir.
E� zamanl� parenteral aminoglikozid tedavisi (veya b�brek at�l�m� etkileyebilecek di�er ila�lar� kullanan) g�ren hastalarda serum tobramisin konsantrasyonlar�n�n takip edilmesi gerekir. Bu hastalar klinik olarak gerekli g�r�ld���nde takip edilmelidir.
Serum tobramisin konsantrasyonu, parmak ucundan kan �rneklemesi ile de�il, sadece ven ponksiyonu ile kan �rneklemesi ile takip edilmelidir. Parmak derisi ile tobramisinin temas etmesi ilac�n serum d�zeylerinde yanl�� y�ksek sonu�lar elde edilmesine yol a�abilir. Bu bula�ma, testten �nce ellerin y�kanmas�yla b�t�n�yle �nlenemez.
Bronkospazm:
T�bbi �r�nler inhalasyon yolu ile al�nd���nda bronkospazm meydana gelebilir. Tobramisinin neb�liz�r ile uygulanmas�nda bronkospazm meydana geldi�i bildirilmi�tir. �lk TOBLA�R dozu g�zetim alt�nda verilmeli ve e�er hastan�n mevcut doz rejiminin bir par�as� ise �n neb�lizasyon ile bronkodilat�r ila� kullan�lmal�d�r. Neb�lizasyondan �nce ve sonra FEVde�eri �l��lmelidir. E�er bronkodilat�r ila� almayan bir hastada tedavinin bronkospazma yol a�t��� saptan�rsa, test ba�ka bir zamanda bronkodilat�r kullanarak tekrar yap�lmal�d�r. Bronkodilat�r ila� tedavisi s�ras�nda bronkospazm�n meydana gelmesi alerjik bir yan�t� belirtiyor olabilir. Alerjik bir yan�ttan ��phelenilirse TOBLA�R kullan�m�na son verilmelidir. Bronkospazm uygun bir t�bbi y�ntemle tedavi edilmelidir.
N�rom�sk�ler hastal�klar:
Myastenia gravis veya Parkinson hastal��� gibi bilinen veya ��pheli bir n�rom�sk�ler hastal��� olan hastalara TOBLA�R re�ete ederken dikkatli olunmal�d�r. Aminoglikozidler n�rom�sk�ler fonksiyon �zerindeki potansiyel k�rar benzeri etkileri ile kas zay�fl���n� art�rabilir.
Hemoptizi (Kan t�k�rme):
Neb�liz�r ile uygulanan ��zeltilerin teneff�s edilmesi, �ks�r�k refleksini art�rabilir. Aktif, �iddetli hemoptizisi olan hastalarda TOBLA�R, sadece tedavinin faydalar�n�n kanamay� art�rma riskinden fazla olmas� durumunda uygulanmal�d�r.
4.5. Di�er t�bbi �r�nler ile etkile�imler ve di�er etkile�im �ekilleri
Tobramisin ile yap�lm�� klinik ila� etkile�imi �al��mas� bulunmamaktad�r. Baz� di�retikler serum ve dokudaki antibiyotik konsantrasyonlar�n� de�i�tirerek aminoglikozid toksisitesini art�rabilmektedir. TOBLA�R'�n etakrinik asit, furosemid, �re veya intraven�z mannitol ile e� zamanl� kullan�lmamas� gerekir.
TOBLA�R'�n n�rotoksik, nefrotoksik veya ototoksik potansiyele sahip di�er ila�larla e� zamanl� ve/veya ard���k kullan�m�ndan ka��n�lmal�d�r.
Etkile�im yoklu�u:
Tobramisin ile yap�lan klinik �al��malarda tobramisin ile e� zamanl� olarak dornaz alfa, beta agonist, inhaler kortikosteroid, di�er antips�domonal antibiyotikleri veya parenteral aminoglikozidleri kullanan hastalarda g�zlenen advers olay profilleri �al��ma pop�lasyonunun geneli ile benzerlik g�stermi�tir.
Parenteral olarak uygulanan aminoglikozidlerin olas� toksisitesini art�rd��� bildirilen di�er ila�lar a�a��da belirtilmi�tir:
Amfoterisin B, sefalotin, siklosporin, takrolimus, polimiksin (nefrotoksisiteyi art�rma riski)
Platin bile�ikleri (nefrotoksisiteyi ve ototoksisiteyi art�rma riski)
Antikolinesterazlar, botulinum toksinleri (n�rom�sk�ler etkiler)
4.6. Gebelik ve laktasyon
Gebelik kategorisi: D
�ocuk do�urma potansiyeli bulunan kad�nlar/Do�um kontrol� (Kontrasepsiyon)
Herhangi bir veri yoktur.
Gebelik d�nemi
Tobramisinin gebe kad�nlarda inhalasyon yoluyla kullan�m�na ili�kin yeterli veri bulunmamaktad�r. Aminoglikozidler gebe kad�nlarda y�ksek sistemik konsantrasyonlara ula�t�klar�nda fet�ste hasara yol a�abilirler (�r. konjenital sa��rl�k).
TOBLA�R, gerekli olmad�k�a gebelik d�neminde kullan�lmamal�d�r.
Laktasyon d�nemi
�nhalasyon yoluyla uygulama sonras�nda anne s�t�ne ge�en tobramisin miktar� bilinmemektedir. Bebeklerde ototoksisite ve nefrotoksisite potansiyeli nedeniyle, ilac�n anne a��s�ndan olan �nemi de dikkate al�narak emzirmenin sonland�r�lmas� veya TOBLA�R tedavisinin s�rd�r�lmesi konusunda bir karar verilmelidir.
�reme yetene�i/Fertilite
Hayvanlarda subkutan tobramisin uygulamas�na ili�kin veriler erkek veya di�ilerde fertiliteye ili�kin bir soruna veya olas� bir soruna i�aret etmemi�tir (bkz. B�l�m 5.3Klinik �ncesi g�venlilik verileri).
4.7. Ara� ve makine kullan�m� �zerindeki etkiler
Bildirilen advers etki reaksiyonlar�na g�re, TOBLA�R'�n ara� ve makine kullanma �zerine etkisi olmad��� tahmin edilmektedir.
4.8. �stenmeyen etkiler
G�venlilik profilinin �zeti
Tobramisinin g�venlilik profili iki randomize, �ift k�r, plasebo kontroll� �al��mada (paralel olarak y�r�t�lm��) ve iki ard���k a��k etiketli takip �al��mas�nda de�erlendirilmi�tir. D�rt �al��man�n t�m�nde de hastalara 28 g�n ila� kullan�lan ve 28 g�n ila� kullan�lmayan sikluslar halinde g�nde iki kez �al��ma ilac� verilmi�tir. �ift k�r �al��malarda hastalar tobramisin veya plasebo ile tedavi gruplar�na randomize edilmi�tir. A��k etiketli �al��malarda t�m hastalara tobramisin verilmi�tir.
Plasebo kontroll� �al��malarda 24 haftal�k tedavi d�nemleri uygulanm�� ve �al��ma serilerinin a��k etiketli izlem �al��malar�n� da i�eren toplam s�resi 96 hafta olmu�tur. 24 haftal�k iki �ift k�r �al��may� tamamlayan 464 hastan�n 396's� a��k etiketli uzatma �al��malar�na kat�lm��t�r. Toplamda 313, 264 ve 120 hasta s�ras�yla 48, 72 ve 96 haftal�k tobramisin tedavilerini tamamlam��t�r.
Bu �al��ma serileri boyunca t�m hastalara �al��ma ilac�n�n yan� s�ra doktorlar�n�n takdirine g�re kistik fibroza y�nelik standart bak�m verilmi�tir.
�ki paralel 24 haftal�k plasebo kontroll� klinik �al��mada tobramisin ya�lar� 6 ila 48 aras�ndaki 258 kistik fibroz hastas�nda genel olarak iyi tolere edilmi�tir.
En yayg�n (≥%10) bildirilen advers olaylar (�al��ma ilac� ile ili�kisine bak�lmaks�z�n) ve bunlar�n plasebo kontroll� �al��malardaki s�kl�klar� (tobramisine kar��l�k plasebo) �u �ekildedir:
Advers olay | S�kl�k |
�ks�r�k | %46,1'e kar��l�k %47,3 |
Farenjit | %38'e kar��l�k %39,3 |
Balgaml� �ks�r�k | %37,6'ya kar��l�k %39,7 |
Asteni | %35,7'ye kar��l�k %39,3 |
Rinit | %34,5'e kar��l�k %33,6 |
Dispne | %33,7'ye kar��l�k %38,5 |
Pireksi | %32,9'a kar��l�k %43,5 |
Akci�er hastal��� | %31,4'e kar��l�k %31,3 |
Ba� a�r�s� | %26,7'ye kar��l�k %32,1 |
G���s a�r�s� | %26'ya kar��l�k %29,8 |
Balgamda renk de�i�ikli�i | %21,3'e kar��l�k %19,8 |
Hemoptizi | %19,4'e kar��l�k %23,7 |
Anoreksi | %18,6'ya kar��l�k %27,9 |
Akci�er fonksiyon testlerinde azalma | %16,3'e kar��l�k %15,3 |
Ast�m | %15,9'a kar��l�k %20,2 |
Kusma | %14'e kar��l�k %22,1 |
Kar�n a�r�s� | %12,8'e kar��l�k %23,7 |
Disfoni | %12,8'e kar��l�k %6,5 |
Bulant� | %11,2'ye kar��l�k %16 |
Kilo kayb� | %10,1'e kar��l�k %15,3 |
Plasebo grubuna k�yasla tobramisin grubunda anlaml� olarak daha s�k bildirilen tek advers ila� reaksiyonu disfoni (tobramisin ve plasebo tedavi gruplar�nda s�ras�yla %12,8 ve %6,5) ve
tinnitus (s�ras�yla %3,1 ve %0) olmu�tur. Disfoni genel olarak hafif olmu�tur ve ila� kullan�lan d�nemlerde daha s�k g�r�lm��t�r.
T�m tinnitus olaylar� ge�ici karakterde olmu� ve tedavinin b�rak�lmas� ile d�zelmi�, i�itme kayb�na yol a�mam��t�r. Ba� d�nmesi gibi vestib�ler advers deneyimler bildiren hastalar�n say�s� tobramisin ve plasebo gruplar�nda benzer bulunmu�tur. Ayr�ca tobramisin ile yap�lan �ift k�r �al��malarda, 8000 Hz'e kadarki i�itmenin de�erlendirildi�i odyometrik testlerde i�itme kayb� saptanmam��t�r. Pazarlama sonras� deneyimde, tobramisin kullanan hastalarda i�itme kayb� bildirilmi�tir. Bu raporlardan baz�lar� �nceden ve e� zamanl� sistemik aminoglikozid tedavisi g�rm�� hastalarda bildirilmi�tir. ��itme kayb� olan hastalarda tinnitus s�kl�kla bildirilmi�tir.
�lac�n piyasaya verilmesinden sonra meydana gelen a�a��daki advers ila� reaksiyonlar�, MedDRA sistem organ s�n�f�na g�re s�ralanm��t�r. Advers reaksiyonlar her bir sistem organ s�n�f� i�inde a�a��daki kategoriler alt�nda azalan s�kl�k s�ras�na g�re dizilmi�tir (CIOMS III): �ok yayg�n (≥1/10); yayg�n (≥1/100 ila <1/10); yayg�n olmayan (≥1/1.000 ila <1/100); seyrek (≥1/10.000 ila <1/1.000); �ok seyrek (<1/10.000), bilinmiyor (eldeki verilerden hareketle tahmin edilemiyor).
Enfeksiyonlar ve enfestasyonlar
Yayg�n: Larenjit
�ok seyrek: Oral kandidiyazis, mantar enfeksiyonu
Kan ve lenf sistemi hastal�klar�
�ok seyrek: Lenfadenopati
Ba����kl�k sistemi hastal�klar�
�ok seyrek: A��r� duyarl�l�k
Metabolizma ve beslenme hastal�klar�
�ok yayg�n: Anoreksiya
Sinir sitemi hastal�klar�
Seyrek: Ba� a�r�s�, ba� d�nmesi, afoni
�ok seyrek: Uyuklama
Kulak ve i� kulak hastal�klar� Yayg�n: Kulak ��nlamas� Seyrek: ��itme kayb�
�ok seyrek: Kulak rahats�zl���, kulak a�r�s�
Solunum, g���s hastal�klar� ve mediastinal hastal�klar
�ok yayg�n: Akci�er hastal���, rinit, ses de�i�ikli�i, balgamda renk de�i�ikli�i, farenjit, �ks�r�k, balgaml� �ks�r�k, dispne, ast�m, kan t�k�rme
Seyrek: Bronkospazm, g���ste rahats�zl�k hissi, burun kanamas� �ok seyrek: Hiperventilasyon, hipoksi, sin�zit
Gastrointestinal hastal�klar
�ok yayg�n: Kusma, bulant�, kilo kayb�, kar�n a�r�s� Seyrek: Tat alg�s�nda de�i�iklik, a��zda �lserasyon �ok seyrek: Diyare
Deri ve deri alt� doku hastal�klar�
Seyrek: D�k�nt�
�ok seyrek: �rtiker, ka��nt�
Kas-iskelet bozukluklar�, ba� doku ve kemik hastal�klar�
Yayg�n: Miyalji
�ok seyrek: S�rt a�r�s�
Genel bozukluklar ve uygulama b�lgesine ili�kin hastal�klar
Yayg�n: Keyifsizlik, asteni, ate�, g���s a�r�s� Seyrek: A�r�
Ara�t�rmalar
�ok yayg�n: Akci�er fonksiyon testlerinde bozulma
A��k etiketli �al��malarda ve �r�n piyasaya ��kt�ktan sonra elde edilen deneyimlere g�re, daha �nceden uzun s�reli intraven�z aminoglikozid kullan�m �yk�s� olan hastalarda veya tobramisin ile beraber intraven�z aminoglikozid kullanan hastalarda i�itme kayb� meydana gelmi�tir (bkz. B�l�m �zel kullan�m uyar�lar� ve �nlemleri). Parenteral aminoglikozidler; a��r� duyarl�l�k, ototoksisite ve nefrotoksisite ile ili�kilendirilmi�tir (bkz. B�l�m 4.3 ve b�l�m 4.4.).
�ki a��k etiketli uzatma �al��mas�nda, tobramisine maruziyetin s�resi artt�k�a balgaml� �ks�r�k ve akci�er fonksiyon testlerinde bozulmada art��; fakat disfoni insidans�nda d���� g�zlenmi�tir. Genel olarak a�a��daki MedDRA Sistem Organ S�n�f�na (SOC) ili�kin advers olaylar�n insidans� tobramisine maruziyetin artmas�yla azalm��t�r: Solunum, g���s hastal�klar� ve mediastinal hastal�klar, gastrointestinal hastal�klar ve genel ve uygulama b�lgesine ili�kin hastal�klar.
Spontan bildirimlerden elde edilen advers ila� reaksiyonlar�
A�a��da yer alan spontan bildirilen advers reaksiyonlar g�n�ll� olarak bildirilmi�tir ve s�kl�k veya ilaca maruziyet ile nedensel ili�kinin kurulmas� her zaman i�in m�mk�n de�ildir.
Kulak ve labirent bozukluklar�
��itme kayb�
Deri ve subkutan doku bozukluklar�
A��r� duyarl�l�k, ka��nt�, �rtiker, d�k�nt�
Sinir sistemi bozukluklar�
Afoni, disg�zi
Solunum, toraks ve mediasten bozukluklar�
Bronkospazm, orofaringeal a�r�
��pheli advers reaksiyonlar�n raporlanmas�
Ruhsatland�rma sonras� ��pheli ila� advers reaksiyonlar�n�n raporlanmas� b�y�k �nem ta��maktad�r. Raporlama yap�lmas�, ilac�n yarar/risk dengesinin s�rekli olarak izlenmesine olanak sa�lar. Sa�l�k mesle�i mensuplar�n�n herhangi bir ��pheli advers reaksiyonu T�rkiye Farmakovijilans Merkezi (T�FAM)'ne bildirmeleri gerekmektedir (www.titck.gov.tr; e-posta: tufam@titck.gov.tr; tel: 0 800 314 00 08; faks: 0 312 218 35 09).
4.9. Doz a��m� ve tedavisi
Tobramisinin tolere edilebilen maksimum dozu belirlenmemi�tir. Tobramisin serum konsantrasyonlar� doz a��m�n�n takibinde yararl� olabilmektedir.
Akut toksisite, TOBLA�R derhal kesilerek tedavi edilmeli ve temel renal fonksiyon testleri yap�lmal�d�r.
Tobramisinin gastrointestinal sistemden emilimi �ok az oldu�undan, TOBLA�R'�n yanl��l�kla oral yoldan al�nmas� halinde sistemik toksisite beklenmez.
TOBLA�R'�n yanl��l�kla intraven�z yoldan uygulanmas� halinde ba� d�nmesi, tinnitus, vertigo, y�ksek tonda i�itme keskinli�i kayb�, solunum s�k�nt�s�, n�rom�sk�ler blokaj ve b�brek bozuklu�u gibi parenteral tobramisin doz a��m� belirti ve semptomlar� ortaya ��kabilir. Hemodiyaliz tobramisinin v�cuttan uzakla�t�r�lmas�nda yararl� olabilmektedir.
Neb�liz�r�n �st k�sm�n� geri tak�n�z, a��zl��� ve solunum valfi ba�l���n� neb�liz�rdeki yerlerine yerle�tiriniz, daha sonra kompres�r� PARI LC PLUS neb�liz�r kullan�m k�lavuzunda anlat�ld��� �ekilde ba�lay�n�z.
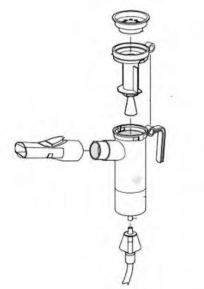
�sterseniz neb�liz�r�n t�m par�alar�n� (ba�lant� borusu hari�) bula��k makinesinde y�kayabilirsiniz. Neb�liz�r par�alar�n� bula��k makinesinin �st raf�na yerle�tiriniz. ��lem tamamland�ktan sonra par�alar� ��kart�p kurutunuz.
Neb�liz�r�n�z�n dezenfekte edilmesi
Neb�liz�r�n�z� kesinlikle ba�ka ki�ilerle payla�may�n�z.
Ayr�ca neb�liz�r�n�z�, �u y�ntemlerden birini kullanarak her tedavi g�n�nde d�zenli olarak dezenfekte etmeniz son derece �nemlidir.
5. FARMAKOLOJ�K �ZELL�KLER
5.1. Farmakodinamik �zellikler
Farmakoterap�tik grup: Sistemik kullan�lan antibakteriyeller; di�er aminoglikozidler ATC kodu: J01GB01
Etki mekanizmas�:
Tobramisin, Streptomyces tenebrarius taraf�ndan �retilen bir aminoglikozid antibiyotiktir. Etkisini esas olarak bakteri h�cresinde protein sentezini bozarak g�sterir. Protein sentezinin bozulmas� bakteri h�cre membran ge�irgenli�ini de�i�tirir, bakteri h�cre duvar�n� ileriye d�n�k bozar ve sonu�ta bakteri h�cresinin �l�m�ne sebep olur. �nhibit�r konsantrasyonlar�na e�it veya biraz daha y�ksek konsantrasyonlarda bakterisit etki g�sterir.
Duyarl�l�k testi:
Parenteral tobramisin tedavisinde kullan�lan in vitro antimikrobiyal duyarl�l�k test y�ntemleri kistik fibroz hastalar�ndan izole edilen P. aeruginosa duyarl�l���n�n takibinde kullan�labilir.
Tobramisin parenteral uygulamas� i�in bilinen duyarl�l�k k�r�lma noktalar� inhaler tobramisin uygulamas� i�in ge�erli de�ildir.
Kistik fibrozda balgam�n neb�lize aminoglikozidlerin lokal biyolojik etkisi �zerinde inhibit�r etkisi vard�r. Bu balgamdaki aerosol tobramisin konsantrasyonlar�n�n, P. Aeruginosa �zerine b�y�meyi bask�lay�c� ve bakterisit etkisi i�in Minimum �nhibit�r Konsantrasyonlar�n (M�K) s�ras�yla on ve yirmi be� kat �zerinde olmas�n� gerektirir. Kontroll� klinik �al��malarda tobramisin kullanan hastalar�n %97'sinde hastadan k�lt�r� yap�lan en y�ksek P. aeruginosa M�K de�erinin 10 kat� balgam konsantrasyonlar�na ve tobramisin kullanan hastalar�n %95'inde en y�ksek M�K de�erinin 25 kat�na ula��lm��t�r. M�K de�erleri parenteral k�r�lma noktas�n�n �zerinde k�lt�r su�lar� olan hastalar�n �o�unda da klinik yarar sa�lanmaktad�r.
5.1. Farmakodinamik �zellikler
Neb�lize uygulama yolu i�in konvansiyonel duyarl�l�k s�n�r de�erlerinin yoklu�unda, organizmalar� neb�lize tobramisine duyarl� ve duyarl� de�il �eklinde tan�mlarken dikkat edilmelidir.
Tobramisin ile yap�lan klinik �al��malarda, ba�lang��ta <128 mcg/ml'lik tobramisin M�K'leri ile P. aeruginosa izolatlar�na sahip �o�u hasta tobramisin ile tedaviyi takiben akci�er fonksiyonunda iyile�me g�stermi�tir. Ba�lang��ta ≥128 mcg/ml'lik bir M�K ile P. aeruginosa izolat�na sahip hastalar�n klinik bir yan�t g�sterme olas�l��� daha d���kt�r. Bununla birlikte, plasebo kontroll� �al��malarda tobramisin kullan�rken ≥128 mcg/ml M�K ile izolat edinmi� 13 hastadan yedisi (%54) pulmoner fonksiyonda iyile�me g�stermi�tir.
�n vitro ve/veya klinik �al��ma deneyimine dayal� olarak, KF'de pulmoner enfeksiyonlarla ili�kili organizmalar�n tobramisin tedavisine a�a��daki �ekilde yan�t vermesi beklenebilir.
Duyarl� | Pseudomonas aeruginosa Haemophilus influanzae Staphylococcus aureus |
Duyarl� de�il | Burkholderia cepacia Stenotrophomonas maltophilia |
| Alcaligenes xylosoxidans |
Klinik �al��malarda tobramisin rejimi ile tedavi test edilen P. aeruginosa izolatlar� i�in tobramisin, amikasin ve gentamisin Minimum �nhibe Edici Konsantrasyonlar�nda k���k ancak net bir art�� g�stermi�tir. Her bir ilave 6 ayl�k tedavi, 6 ayl�k kontroll� �al��malarda g�zlenene benzer boyutta y�kselen art��larla sonu�lanm��t�r. Kronik enfeksiyon g�r�len KF hastalar�ndan izole edilen P. aeruginosa' da tespit edilen en bask�n aminoglukozidaz diren� mekanizmas�, t�m aminoglikozidlere genel bir duyarl�l�k eksikli�i olarak tan�mlanan impermeabilitedir. KF hastalar�ndan izole edilen P. aeruginosa'n�n ayr�ca antibiyotik uzakla�t�r�ld���nda duyarl�l��a geri d�nme ile karakterize adaptif bir aminoglikozid direnci sergiledi�i g�sterilmi�tir.
Klinik �al��malar:
P. aeruginosa'l� kistik fibroz hastalar�nda e� tasar�ml�, �ift k�r, randomize, plasebo kontroll�, paralel grup, 24 haftal�k iki klinik �al��ma (�al��ma 1 ve �al��ma 2) yap�lm��t�r. Bu �al��malara ba�lang��taki FEV� de�eri �ng�r�len normal de�erin %25 ve %75'i aras�nda olan 520 olgu kat�lm��t�r. Alt� ya��n alt�nda olan veya ba�lang��taki kreatinin d�zeyi >2 mg/dl olan veya balgam�ndan Burkholderia cepacia izole edilen hastalar �al��madan d��lanm��t�r. Bu klinik �al��malarda 258 hastaya elle kullan�lan PARI LC PLUS™ Tekrar Kullan�labilir Neb�liz�r ve DeVilbiss® Pulmo-Aide® kompres�r arac�l���yla ayaktan tedavi �eklinde tobramisin uygulanm��t�r (bkz. Tablo 1).
Tablo 1. Klinik �al��malardaki doz rejimleri
| Siklus 1 | Siklus 2 | Siklus 3 | |||
28 g�n | 28 g�n | 28 g�n | 28 g�n | 28 g�n | 28 g�n | |
Tobramisin rejimi n=258 | Tobramisin + standart bak�m | Standart bak�m | Tobramisin + standart bak�m | Standart bak�m | Tobramisin + standart bak�m | Standart bak�m |
Plasebo rejimi n=262 | Plasebo + standart bak�m | Standart bak�m | Plasebo + standart bak�m | Standart bak�m | Plasebo + standart bak�m | Standart bak�m |
T�m hastalara kistik fibroz hastalar� i�in �nerilen ve oral ve parenteral antips�domonal tedavi, betaagonisti, kromolin, inhaler steroid ve hava yolu klirens y�ntemlerini i�eren standart tedaviye ek olarak tobramisin veya plasebo (tatland�r�c� olarak 1,25 mg kinin) verilmi�tir. Ayr�ca hastalar�n yakla��k %77'sine dornaz alfa (Pulmozyme®, Genentech) ile e� zamanl� tedavi uygulanm��t�r.
Her �al��mada tobramisin ile tedavi edilen hastalar�n solunum fonksiyonlar�nda anlaml� d�zeyde iyile�me g�zlenmi�tir. �al��ma 1'de 24 haftal�k s�re i�erisinde tobramisin grubunda FEV'de ba�lang�ca g�re yakla��k %11'lik bir ortalama art�� g�zlenirken plasebo hastalar�nda ortalama de�i�iklik olmam��t�r. �al��ma 2'de tobramisin ile tedavi edilen hastalarda FEV'de yakla��k %7 ortalama art�� kaydedilirken plasebo ile tedavi edilen hastalarda yakla��k %1 ortalama azalma kaydedilmi�tir. �ekil 1 her iki �al��mada da 24 haftal�k d�nemde FEV'deki ortalama ba��l de�i�ikli�i g�stermektedir. �la� kullan�lmayan 28 g�nl�k d�nemlerde ortalama FEVba�lang�c�n �zerinde seyretmi�, fakat bazen tersine de d�nebilmi�tir.
�ekil 1. Ba�lang��taki %FEV'e g�re ba��l de�i�iklik
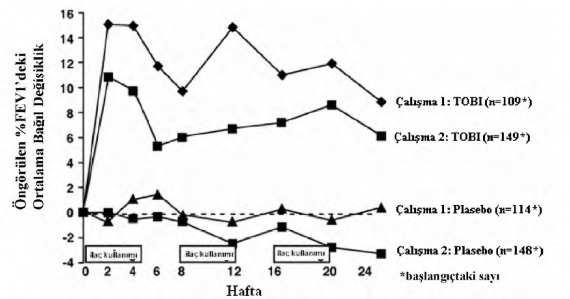
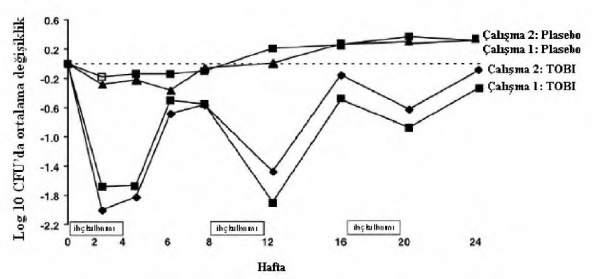
Her �al��mada tobramisin tedavisi, ila� kullan�lan d�nemlerde balgam�n gram� ba��na d��en P. aeruginosa CFU (“colony forming unit”) say�s�nda anlaml� azalmaya (�al��ma 1'de log -1,17 ve �al��ma 2'de log -0,99) yol a�m��t�r. �la� kullan�lmayan d�nemlerde balgam�n bakteriyel
yo�unlu�u ba�lang��taki d�zeylerine d�nm��t�r. Balgamdaki bakteriyel yo�unluktaki azalma ard���k her siklusta giderek azalm��t�r (bkz. �ekil 1).
�ekil 2. logCFU'larda ba�lang�ca g�re mutlak de�i�iklik
Tobramisin ile tedavi edilen hastalar ortalama 5,1 g�n hastanede yatarken bu oran plasebo ile tedavi edilen hastalarda 8,1 olmu�tur. Tobramisin ile tedavi edilen hastalarda ortalama 9,6 g�n parenteral antips�domonal antibiyotik tedavisi uygulanmas� gerekirken plasebo ile tedavi edilen hastalarda bu s�re 14,1 g�n olmu�tur. Alt� ayl�k tedavi d�neminde tobramisin hastalar�n�n %40'� ve plasebo hastalar�n�n %53'� parenteral antips�domonal antibiyotik ile tedavi edilmi�tir.
24 haftal�k iki �ift k�r �al��malar� tamamlayan 464 hastan�n 396's� a��k etiketli uzatma �al��malar�na kat�lm��t�r. Toplamda 313, 264 ve 120 hasta s�ras�yla 48, 72 ve 96 haftal�k tobramisin tedavilerini tamamlam��t�r.
Akci�er fonksiyonundaki kayb�n oran� �ift k�r randomize tedavi d�neminde tobramisin tedavisinin ba�lat�lmas�ndan sonra plasebo hastalar�ndakine k�yasla anlaml� olarak daha d���k bulunmu�tur. Ortalama akci�er fonksiyonu de�erleri, tobramisin tedavisinin ba�lang�c�nda kaydedilenlerden y�ksek (ortalama FEV�'de ba�lang�ca g�re %4,7 ba��l de�i�iklik) ve 96 haftaya kadar plasebo ile tedavi edilen hastalarda regresyon modelinde hesaplanandan y�ksek seyretmi�tir. Akci�er fonksiyonundaki kayb�n regresyon modelinde hesaplanan e�imi k�rle�tirilmi� plasebo tedavisinde -%6,52 ve tobramisin tedavisi s�ras�nda -%2,53 bulunmu�tur
(p=0,0001).
Di�er bilgiler:
18 aya kadar tobramisin ile tedavi edilen hastalar�n B. cepacia, S. maltophilia veya A. xylosoxidans edinme a��s�ndan tobramisin ile tedavi edilmeyen hastalarda beklenenden daha b�y�k bir risk ta��d�klar�na dair bir kan�t yoktur. Aspergillus t�rleri tobramisin kullanan hastalar�n balgam�ndan daha s�k olarak geri kazan�lm��t�r; ancak, Alerjik Bronkopulmoner Aspergilloz (ABPA) gibi klinik sekel nadiren ve kontrol grubundaki benzer bir s�kl�kta bildirilmi�tir.
5.2. Farmakokinetik �zellikler
Genel �zelliklerTobramisin i�eren TOBLA�R, katyonik polar bir molek�l olup epitel membranlardan kolayca ge�emez.
TOBLA�R �zel olarak inhalasyon yoluyla uygulanmak �zere form�le edilmi�tir. TOBLA�R'�n biyoyararlan�m� neb�liz�r performans� ve hava yolu patolojisine ba�l� olarak de�i�kenlik g�sterebilir. TOBLA�R uygulamas�n� takiben, tobramisin �zellikle hava yolunda konsantre halde bulunur.
Emilim:
TOBLA�R inhalasyonu sonras�nda tobramisine sistemik maruziyetin akci�erlere ula�t�r�lan doz fraksiyonunun pulmoner emiliminden kaynaklanmas� beklenir; ��nk� tobramisin oral yoldan uyguland���nda dikkate de�er d�zeyde emilmez. TOBLA�R'�n biyoyararlan�m� neb�liz�r performans� ve hava yolu patolojisindeki bireysel farkl�l�klara ba�l� olarak de�i�iklik g�sterebilmektedir.
Balgam konsantrasyonlar�:
�lk 300 mg tobramisin dozunun inhalasyonundan on dakika sonra balgamdaki ortalama tobramisin konsantrasyonu 1,237 mcg/g bulunmu�tur (35 ila 7,414 mcg/g aral���nda). Tobramisin balgamda birikmez; 20 haftal�k tobramisin rejimi tedavisinden sonra tobramisinin inhalasyondan 10 dakika sonraki ortalama balgam konsantrasyonu 1,154 mcg/g (aral�k: 39 ila
8,085 mcg/g'a kadar) bulunmu�tur. Balgam tobramisin konsantrasyonlar�nda y�ksek de�i�kenlik de g�zlenmi�tir. �nhalasyondan iki saat sonra balgam konsantrasyonlar� inhalasyondan sonraki 10. dakikada �l��len tobramisin d�zeylerinin yakla��k %14'�ne d��m��t�r.
Serum konsantrasyonlar�:
Kistik fibroz hastalar�nda tek bir 300 mg'l�k tobramisin dozunun inhalasyonundan 1 saat sonraki ortalama serum tobramisin konsantrasyonu 0,95 mcg/ml bulunmu�tur (aral�k: kantitasyon s�n�r�n�n alt�nda [BLQ] – 3,62 mcg/ml). Yirmi haftal�k tobramisin tedavisinden sonra doz uygulamas�ndan 1 saat sonraki ortalama serum tobramisin konsantrasyonu 1,05 mcg/ml bulunmu�tur (aral�k: BLQ – 3,41 mcg/ml).
Da��l�m:
TOBLA�R uygulamas�ndan sonra tobramisin primer olarak hava yollar�nda konsantre olur. Tobramisinin serum proteinlerine ba�lanmas� ihmal edilebilir d�zeydedir.
Biyotransformasyon:
Tobramisin metabolize edilmez ve b�y�k oranda idrarla de�i�memi� halde at�l�r.
Eliminasyon:
�nhalasyon yolu ile uygulanan tobramisinin eliminasyonu ara�t�r�lmam��t�r.
�ntraven�z uygulamay� takiben, sistematik olarak emilen tobramisin ba�l�ca glomer�ler filtrasyonu yoluyla at�l�r. Tobramisinin kistik fibroz hastalar�nda serumdan eliminasyon yar�lanma �mr� yakla��k 3 saattir. Tobramisinin %10'undan az� plazma proteinlerine ba�l�d�r. TOBLA�R uygulamas�n� takiben emilmemi� tobramisin muhtemelen ba�l�ca ��kart�lm�� balgamda elimine edilir.
Hastalardaki karakteristik �zellikler
Karaci�er yetmezli�i:
Tobramisin metabolize edilmedi�inden, karaci�er yetmezli�inin tobramisin maruziyetine etkisinin olmas� beklenmez (bkz. B�l�m Pozoloji ve uygulama �ekli).
B�brek yetmezli�i:
Tobramisin b�y�k oranda idrar yoluyla, de�i�memi� olarak at�l�r ve b�brek fonksiyonunun tobramisine maruziyeti etkilemesi beklenir.
Pediyatrik pop�lasyon:
TOBLA�R, 6 ya��n alt�ndaki hastalarda kullan�lmamal�d�r.
Geriyatrik pop�lasyon:
Bu pop�lasyonda bir doz ayarlamas� yap�lmas� y�n�nde veya aleyhine �neriyi destekleyen veriler yetersizdir.
5.3. Klinik �ncesi g�venlilik verileri
Preklinik veriler g�venlilik farmakolojisi, tekrarlanan doz toksisitesi, genotoksisite veya �reme toksisitesi �al��malar� �����nda insanlardaki ba�l�ca tehlikenin renal toksisite ve ototoksisite oldu�unu g�stermi�tir. Tekrarlanan doz toksisitesi �al��malar�nda, hedef toksisite organlar� b�brekler ve vestib�ler/koklear fonksiyonlard�r. Genel olarak �nerilen klinik dozda inhalasyon ile elde edilebilecek olandan daha y�ksek sistemik tobramisin d�zeylerinde toksisite g�zlenmi�tir.
Tobramisinin karsinojenik potansiyelini ara�t�ran iki y�ll�k bir s��an inhalasyon toksikolojisi �al��mas� tamamlanm��t�r. S��anlar 95 hafta boyunca g�nde 1,5 saat s�resince tobramisine maruz b�rak�lm��t�r. S��anlarda 35 mcg/ml'ye varan serum tobramisin d�zeyleri bulunurken, klinik �al��malarda kistik fibroz hastalar�nda maksimum 3,62 mcg/ml d�zeyi g�zlenmi�tir. Herhangi bir t�m�r t�r�n�n insidans�nda ilaca ba�l� art�� g�zlenmemi�tir.
Ayr�ca tobramisin bir dizi in vitro ve in vivo testte genotoksisite y�n�nden de de�erlendirilmi�tir. Be� test su�u �zerinde ger�ekle�tirilen Ames bakteriyel reversiyon testinde hi� bir su�ta metabolik aktivasyonlu veya aktivasyonsuz olarak revertanlarda anlaml� bir art�� g�sterilmemi�tir. Tobramisin i�in “fare lenfoma ileriye d�n�k mutasyon deneyi” negatif bulunmu�; �in hamsteri over h�crelerinde kromozomal sapmalar� tetiklememi� ve fare mikron�kleus testinde negatif bulunmu�tur.
�nhalasyon yoluyla uygulanan tobramisin ile �reme toksikolojisi �al��mas� yap�lmam��t�r. Fakat tobramisinin organogenez s�ras�nda 100 (s��an) veya 20 (tav�an) mg/kg/g�n dozlar�nda subkutan yoldan uygulanmas� teratojen bulunmam��t�r. Tobramisinin ≥40 mg/kg/g�n dozlar� di�i tav�anlarda a��r derecede maternal toksisiteye neden olmu� (spontan abort ve �l�me yol a�an nefrotoksisite) ve teratojenite de�erlendirmesine engel olmu�tur. Tobramisin ile yap�lan klinik d��� �reme toksisitesi �al��malar�nda yavrularda ototoksisite de�erlendirilmemi�tir. Hayvanlardan elde edilmi� mevcut veriler do�rultusunda prenatal maruziyet d�zeylerinde toksisite (�r. ototoksisite) riski d��lanamaz.
Tobramisinin 100 mg/kg'a kadar subkutan yoldan uygulanmas� erkek veya di�i s��anlarda �iftle�me davran���n� etkilememi� veya fertilitede bozulmaya yol a�mam��t�r.
Kompres�r� �al��t�r�n�z. A��zl�ktan buhar ��k���n� kontrol ediniz. Buhar ��k��� yoksa t�m boru ba�lant�lar�n� kontrol ediniz ve kompres�r�n do�ru �ekilde �al��t���ndan emin olunuz.
6. FARMAS�T�K �ZELL�KLER
6.1. Yard�mc� maddelerin listesi
Sodyum klor�r Enjeksiyonluk su
S�lf�rik asit ve sodyum hidroksit
6.2. Ge�imsizlikler
TOBLA�R, neb�liz�r i�inde di�er ila�larla seyreltilmemeli veya kar��t�r�lmamal�d�r.
6.3. Raf �mr�
24 ay
�i�enin a��lmas�ndan hemen sonra t�m i�eri�i kullan�lmal�d�r. TOBLA�R, sadece tek kullan�ml�kt�r. ��eri�inde koruyucu madde olmad��� i�in a��ld�ktan sonra t�m �i�e i�eri�i hemen kullan�lmal� ve kullan�lmam�� ��zelti ��pe at�lmal�d�r. A��lan �i�eler hi�bir zaman tekrar kullan�m i�in saklanmamal�d�r.
6.4. Saklamaya y�nelik �zel tedbirler
2-8°C aras�nda buzdolab�nda ve orijinal kutusunda saklay�n�z. TOBLA�R yo�un ����a kar�� korunmal�d�r.
Buzdolab�ndan ��kart�ld�ktan sonra veya buzdolab�n�n bulunmad��� ortamlarda, TOBLA�R folyolar� (kapal� veya a��k), 25°C alt�nda en fazla 28 g�n saklanabilir.
TOBLA�R'�n buzdolab�nda sakland���nda (2-8°C) �i�e �zerinde bas�l� olan son kullanma tarihinden sonra veya oda s�cakl���nda sakland���nda (25°C) 28 g�nden uzun s�re kullan�lmamas� gerekir. ��zelti bulan�ksa ve i�erisinde par�ac�klar varsa kullan�lmamal�d�r.
Buzdolab�nda saklanmamas� halinde normalde hafif sar� renkli olan TOBLA�R'�n zamanla rengi koyula�abilir; fakat �r�n �nerilen saklama ko�ullar�nda sakland��� m�ddet�e renk de�i�ikli�i �r�n�n kalitesinde de�i�iklik oldu�unu g�stermez.
6.5. Ambalaj�n niteli�i ve i�eri�i
TOBLA�R, 5 ml ��zelti i�eren 5 ml'lik LDPE �i�elerde bulunur. Bir karton kutu i�erisinde 4 adet �i�e i�eren 14 kapal� folyo �eklinde toplam 56 adet �i�e bulunmaktad�r.
6.6. Be�eri t�bbi �r�nden arta kalan maddelerin imhas� ve di�er �zel �nlemler
Kullan�lmam�� olan �r�nler ya da at�k materyaller “T�bbi At�klar�n Kontrol� Y�netmeli�i” ve “Ambalaj ve Ambalaj At�klar�n�n Kontrol� Y�netmeli�i”ne uygun olarak imha edilmelidir.
 D�� Gebelik
D�� gebelik, her 100 gebelikten birini etkileyen, s�k g�r�len ve �l�me sebep
olabilecek bir durumdur. Bu, d�llenen yumurta, rahimin d���na yerle�irse, olu�an
bir durumdur. Gebelik ilerledik�e, a�r�ya ve kanamalara sebep olur.
D�� Gebelik
D�� gebelik, her 100 gebelikten birini etkileyen, s�k g�r�len ve �l�me sebep
olabilecek bir durumdur. Bu, d�llenen yumurta, rahimin d���na yerle�irse, olu�an
bir durumdur. Gebelik ilerledik�e, a�r�ya ve kanamalara sebep olur. |
 S�rt A�r�s�
S�rt a�r�s� birden bire ortaya
��k�p �iddetli (akut) olabilir veya zamanla geli�ip daha uzun
s�reli sorunlara (kronik) neden olabilir.
S�rt A�r�s�
S�rt a�r�s� birden bire ortaya
��k�p �iddetli (akut) olabilir veya zamanla geli�ip daha uzun
s�reli sorunlara (kronik) neden olabilir. |
�LA� E�DE�ERLER�
| E�de�er �la� Ad� | Barkodu | �la� Fiyat� |
|---|---|---|
| KFIBROGEN | 8699783520014 | 39,503.72TL |
| OBRAMIS | 8680199611670 | |
| OFTAMYCIN | 8699525618252 | 207.79TL |
| PROMESIN | 8699828610014 | |
| TOBEL | 8699540751101 | |
| Di�er E�de�er �la�lar |
 |
Artrit Artrit, olduk�a yayg�n bir hastal�kt�r ancak iyi anla��lamam��t�r. Asl�nda �artrit� tek bir hastal���n ad� de�ildir; eklem a�r�s� veya eklem hastal�klar�n� adland�rman�n gayri resmi yoludur. |
 |
Ast�m Ast�ml� ki�ilerin akci�erlerindeki hava borular� (bron�lar) hassast�r. Bu ki�iler belirli tetikleyici fakt�rlere maruz kald�klar�nda, hava borular� nefes almalar�n� g��le�tirecek �ekilde daral�r. |
 |
Pankreas Kanseri Pankreas karn�n alt k�sm�nda yatay �ekilde bulunan bir organd�r. Sindirime yard�mc� olan enzimleri ve kan �ekerini y�netmeye yard�mc� olan hormonlar� v�cuda da��tmakla g�revlidir. |
�LA� GENEL B�LG�LER�
Vem �la� Sanayi Ve Ticaret Ltd. �ti
| Sat�� Fiyat� | 39503.72 TL [ 4 May 2026 ] |
| �nceki Sat�� Fiyat� | 39503.72 TL [ 27 Apr 2026 ] |
| Original / Jenerik | Original �la� |
| Re�ete Durumu | Normal Re�eteli bir ila�d�r. |
| Barkodu | 8699844523350 |
| Etkin Madde | Tobramisin |
| ATC Kodu | J01GB01 |
| Birim Miktar | 300/5 |
| Birim Cinsi | MG/ML |
| Ambalaj Miktar� | 56 |
| Enfeksiyona Kar�� Kullan�lan (Antienfektif) �la�lar > Aminoglikozidler > Tobramisin |
| Yerli ve Be�eri bir ila�d�r. |