TEMOZOLID 250 mg kapsül Kısa Ürün Bilgisi
{ Temozolomid }
1. BEŞERİ TIBBİ ÜRÜNÜN ADI
TEMOZOLİD 250 mg kapsül Sitotoksik
2. KALİTATİF VE KANTİTATİF BİLEŞİM
Etkin madde
Temozolomid 250 mg
Yardımcı maddeler
Anhidr laktoz (sığır sütünden elde edilir)….209,50 mg Yardımcı maddeler için 6.1.'e bakınız.
3. FARMASÖTİK FORMU
Sert kapsül
Sert kapsüller opak beyaz gövdeli ve opak beyaz kapaklı olup, siyah mürekkep ile yazılmıştır.
4. KLİNİK ÖZELLİKLER
4.1. Terapötik endikasyonlar
TEMOZOLİD, birinci basamakta yeni tanı konmuş glioblastoma multiforme tedavisinde radyoterapi ile birlikte ve sonrasında endikedir.
TEMOZOLİD, standart tedaviden sonra nükseden veya progresyon gösteren glioblastoma multiforme veya anaplastik astrositoma gibi malign glioma hastalarında endikedir.
TEMOZOLİD, metastatik malign melanomlu hastaların tedavisinde endikedir.
4.2. Pozoloji ve uygulama şekli
TEMOZOLİD sadece beyin tümörleri konusunda uzman doktorlar tarafından reçetelendirildiği zaman kullanılmalıdır.
TEMOZOLİD yemekten en az bir saat önce, aç karnına verilmelidir. Uygulamadan önce veya sonra antiemetik tedavisi uygulanabilir.
TEMOZOLİD tedavisi hastalığın ilerlemesine kadar maksimum 2 yıl sürdürülebilir.
Yeni teşhis edilen glioblastoma multiformeli erişkin hastalar:
Eş zamanlı faz:
TEMOZOLİD, radyoterapi (30 fraksiyonda verilen 60 Gy) ile eş zamanlı olarak, 42 gün süreyle günde 75 mg/m dozunda ve takibinde 6 kür adjuvan tedavi olarak oral yoldan verilir. Doz azaltılması önerilmez; ama hastanın toleransına göre doza ara verilebilir. Aşağıdaki koşulların tümü sağlanır ise, TEMOZOLİD ile eş zamanlı dönem 42 günden 49 güne kadar sürdürülebilir:
mutlak nötrofil sayısı ≥1,5x10/L;
4.3. Kontrendikasyonlar
TEMOZOLİD,
Etkin madde
4.4. Özel kullanım uyarıları ve önlemleri
Fırsatçı enfeksiyonlar ve enfeksiyonların reaktivasyonu
TEMOZOLİD ile tedavi sırasında fırsatçı enfeksiyonlar (Pneumocystis jirovecii pnömonisi gibi) ve enfeksiyonların reaktivasyonu (hepatit B virüsü (HBV), sitomegalovirüs (CMV) gibi) gözlenmiştir (bkz. Bölüm 4.8).
Pneumocystis jirovecii pnömonisi
Bir pilot çalışmada uzatılmış 42 günlük şemayla eş zamanlı temozolomid ve radyoterapi alan hastaların Pneumocystis jirovecii pnömonisi (PCP) gelişimi yönünden özel bir riske sahip oldukları gösterilmiştir. Bu nedenle, 42 günlük (maksimum 49 günlük) rejimde eş zamanlı temozolomid ve radyoterapi alan bütün hastalara lenfosit sayısı ne olursa olsun PCP için profilaksi uygulanması gerekir. Lenfopeni ortaya çıkarsa, hastalar lenfopeni Evre ≤1'e gerileyinceye kadar profilaksiye devam etmelidir.
Temozolomidin, daha uzun süreli bir dozaj rejiminde kullanılması durumunda PCP görülme sıklığı artabilir. Ancak, temozolomid alan tüm hastalar, özellikle de steroid kullanan hastalar, doz rejimine bakılmaksızın PCP açısından yakından izlenmelidir. Özellikle deksametazon veya diğer steroidlerle birlikte temozolomid kullanan hastalarda ölümcül solunum yetmezliği vakaları rapor edilmiştir.
HBV
Ölümle sonuçlanan bazı vakalarda, hepatit B virüsü (HBV) reaktivasyonuna bağlı hepatit rapor edilmiştir. Pozitif hepatit B serolojisi olan hastalarda (aktif hastalığı olanlar da dahil) tedaviye başlanmadan önce karaciğer hastalığında uzmanlara danışılmalıdır. Tedavi sırasında hastalar izlenmeli ve uygun şekilde tedavi edilmelidir.
Herpetik meningoensefalit
Pazarlama sonrası vakalarda, eş zamanlı steroid kullanan vakalar dahil, radyoterapi ile birlikte temozolomid alan hastalarda herpetik meningoensefalit (ölümle sonuçlanan vakalar dahil) görülmüştür.
Hepatotoksisite
Temozolomid ile tedavi edilen hastalarda ölümcül karaciğer yetmezliği dahil olmak üzere karaciğer hasarı bildirilmiştir (bkz. Bölüm 4.8). Tedaviye başlamadan önce karaciğer fonksiyon testleri yapılmalıdır. Bu testler anormal ise, hekimler temozolomide başlamadan önce ölümcül karaciğer yetmezliği potansiyeli dahil risk/yarar oranını değerlendirmelidir. 42 günlük tedavi kürü alan hastalarda, karaciğer fonksiyon testleri bu kürün ortalarında tekrarlanmalıdır. Tüm hastalarda, her bir tedavi küründen sonra karaciğer fonksiyon testleri yapılmalıdır. Anlamlı karaciğer fonksiyon anormallikleri saptanan hastalarda hekimler tedaviye devam edilmesinin risk/yarar oranını değerlendirmelidir. En son temozolomid tedavisinden birkaç hafta sonra veya daha sonra karaciğer toksisitesi meydana gelebilir.
Maligniteler
Çok nadir olarak miyeloid lösemi dahil olmak üzere miyelodisplastik sendrom ve sekonder malignite vakaları bildirilmiştir. (bkz. Bölüm 4.8)
Antiemetik tedavi
Bulantı ve kusma TEMOZOLİD tedavisiyle çok yaygın şekilde görülür. TEMOZOLİD uygulanmadan önce veya uygulandıktan sonra antiemetik tedavi uygulanabilir.
Yeni teşhis edilen glioblastoma multiformeli erişkin hastalar için:
Eş zamanlı fazın başlangıç dozundan önce anti-emetik profilaksisi önerilir ve monoterapi fazında anti-emetik profilaksisi kuvvetle önerilir.
Rekürran veya progresif malign glioması olan hastalar:
Önceki tedavi kürlerinde şiddetli (evre 3 veya 4) kusma yaşayan hastalarda antiemetik tedavi gerekebilir.
Laboratuvar parametreleri:
TEMOZOLİD ile tedavi edilen hastalar uzun süren pansitopeni dahil miyelosupresyon yaşayabilir; bu durum bazı vakalarda ölümle sonuçlanan aplastik anemiye neden olabilir. Bazı vakalarda karbamazepin, fenitoin ve sülfametoksazol/trimetoprim gibi aplastik anemiyle ilişkili tıbbi ürünlere eş zamanlı maruz kalım değerlendirmeyi karmaşıklaştırır. Tedaviden önce aşağıdaki laboratuvar parametreleri karşılanmalıdır: MNS ≥ 1,5 x 10/L ve trombosit
sayısı ≥ 100 x 10/L. İlk dozdan 21 gün sonra (22. günde) veya o günden sonraki 48 saat içinde tam kan sayımı yapılmalı ve MNS 1,5 x 10/L'nin üzerine ve trombosit sayısı 100 x 10/L'nin üzerine çıkıncaya kadar haftada bir tam kan sayımı yapılmalıdır. Herhangi bir kürde MNS 1,0 x 10/L'nin altına veya trombosit sayısı 50 x 10/L'nin altına düşerse bir sonraki kürde 1 doz düzeyi azaltılmalıdır (bkz. Bölüm 4.2). Doz düzeyleri 100 mg/m, 150 mg/m ve 200 mg/m'dir. Önerilen en düşük doz 100 mg/m'dir.
Pediyatrik kullanım:
3 yaşın altındaki çocuklarda TEMOZOLİD kullanımına ilişkin klinik deneyim yoktur. Daha büyük yaştaki çocuklarda ve ergenlerde deneyim çok sınırlıdır (bkz. Bölüm 4.2 ve 5.1).
Yaşlı hastalarda kullanım (70 yaş ve üzeri):
Yaşlı hastalarda genç hastalara göre nötropeni ve trombositopeni riski daha fazladır. Bu nedenle, yaşlı hastalarda TEMOZOLİD kullanımında dikkatli olunmalıdır.
Erkek hastalar:
TEMOZOLİD ile tedavi edilen erkeklerin son dozu aldıktan sonraki 6. aya kadar çocuk sahibi olmamaları ve tedaviden önce spermlerin dondurularak korunması konusunda tavsiye alması önerilir(bkz. Bölüm 4.6).
Diğer:
TEMOZOLİD her dozunda 209.50 mg laktoz içerir. Nadir kalıtımsal galaktoz intoleransı, Lapp laktoz yetmezliği ya da glukoz-galaktoz malabsorpsiyon problemi olan hastaların bu ilacı kullanmamaları gerekir.
4.5. Diğer tıbbi ürünler ile etkileşimler ve diğer etkileşim şekilleri
Ayrı bir faz I çalışmada, ranitidinle birlikte temozolomid uygulaması temozolomidin emilim derecesinde ya da onun aktif metaboliti monometil triazenoimidazol karboksamid (MTIC) maruz kalımda değişikliklere yol açmamıştır.
Temozolomid yemekle birlikte uygulandığında C'da % 33'lük azalma ve EAA'da % 9'luk azalma görülmüştür. C'daki değişimin klinik anlamlılığı bertaraf edilemeyeceğinden, TEMOZOLİD yemekle birlikte uygulanmamalıdır.
Faz II çalışmalardaki popülasyon farmakokinetiği üzerinde yapılan bir analize dayalı olarak deksametazon, proklorperazin, fenitoin, karbamazepin, ondansetron, H reseptör antagonistleri veya fenobarbital ile birlikte uygulanması, temozolomidin klerensini değiştirmemektedir. Valproik asit ile birlikte uygulanması durumunda temozolomid klerensinde küçük ama istatistiksel olarak anlamlı bir azalma meydana gelmektedir.
Temozolomidin diğer tıbbi ürünlerin metabolizması ya da eliminasyonu üzerindeki etkilerini belirlemek amacıyla hiçbir çalışma yapılmamıştır. Bununla beraber temozolomid karaciğerde metabolize edilmediği ve proteinlere düşük oranda bağlandığı için diğer tıbbi ürünlerin farmakokinetiğini etkilemesi muhtemel değildir (bkz. Bölüm 5.2).
Temozolomid ile diğer miyelosupresif ajanların kombine kullanımı, miyelosupresyon olasılığını artırabilir.
Pediyatrik popülasyon
Etkileşim çalışmaları yalnızca erişkinlerde yapılmıştır.
4.6. Gebelik ve laktasyon
Gebelik Kategorisi: D
Çocuk doğurma potansiyeli bulunan kadınlar/Doğum kontrolü (Kontrasepsiyon)
Çocuk doğurma potansiyeli olan kadınlara TEMOZOLİD kullanımı sırasında gebeliği önlemek için etkili kontrasepsiyon kullanmaları tavsiye edilmelidir.
Gebelik dönemi
TEMOZOLİD'in gebe kadınlarda kullanımına ilişkin veri mevcut değildir. 150 mg/m temozolomid alan fare ve tavşanlarda yapılan klinik öncesi çalışmalarda teratojenite ve/veya fetal toksisite gösterilmiştir (bkz. Bölüm 5.3). TEMOZOLİD, gebe kadınlara verilmemelidir. Gebelikte kullanılması düşünülüyorsa, hasta fetusa yönelik potansiyel riskler konusunda bilgilendirilmelidir.
Laktasyon dönemi
TEMOZOLİD'in anne sütüne geçip geçmediği bilinmediğinden TEMOZOLİD emziren kadınlarda kullanılmamalıdır.
Üreme yeteneği/Fertilite
Sıçan ve köpeklerde erkek üreme sisteminde toksisite gösterilmiştir (bkz. Bölüm 5.3).
Erkek fertilitesi
Temozolomidin genotoksik etkileri olabilir. Bu nedenle temozolomid ile tedavi edilen erkeklere son dozu aldıktan sonra 6 aya kadar çocuk sahibi olmamaları ve temozolomid tedavisine bağlı geri dönüşsüz infertilite olasılığı nedeniyle tedaviden önce spermlerini dondurarak saklamaları (kriyokonservasyon) önerilmelidir.
4.7. Araç ve makine kullanımı üzerindeki etkiler
TEMOZOLİD bitkinlik ve uyku hali nedeniyle araç ve makine kullanma becerisi üzerinde hafif bir etki gösterebilir (bkz. Bölüm 4.8).
4.8. İstenmeyen etkiler
Güvenlik profilinin özeti Klinik çalışma deneyimi
Klinik çalışmalarda temozolomid ile tedavi edilen hastalarda bildirilen en yaygın advers
reaksiyonlar bulantı, kusma, konstipasyon, anoreksi, baş ağrısı, yorgunluk, konvülsiyonlar ve döküntüdür. Hematolojik advers reaksiyonların çoğu yaygın şekilde raporlanmıştır; derece 3- 4 laboratuvar bulgularının sıklığı Tablo 4'den sonra sunulmaktadır.
Rekürren ve progresif gliomalı hastalarda bulantı (%43) ve kusma (%36) genellikle derece 1 veya 2'dir (24 saatte 0 – 5 kusma episodu) ve kendini sınırlayan tarzdadır veya standart antiemetik tedaviyle kolayca kontrol altına alınabilmiştir. Şiddetli bulantı ve kusma insidansı
%4'dür.
Advers reaksiyonların tablolaştırılmış listesi
Klinik çalışmalarda gözlenen ve temozolomidin pazarlama sonrası kullanımı sırasında bildirilen advers reaksiyonlar Tablo 4'de listelenmektedir.
Bu reaksiyonlar Sistem Organ Sınıfı ve sıklığa göre sınıflanmaktadır. Sıklık gruplamaları aşağıdaki standart oranlara göre tanımlanmaktadır: Çok yaygın (≥ 1/10); yaygın (≥ 1/100 ila < 1/10); yaygın olmayan (≥ 1/1.000 ila < 1/100); seyrek ≥ 1/10.000 ila < 1/1.000); çok seyrek (< 1/10.000); bilinmiyor: eldeki verilerden hareketle tahmin edilemiyor. Her bir sıklık gruplamasında istenmeyen etkiler azalan ciddiyet sırasıyla sunulmaktadır.
Tablo 4. Temozolomid ile tedavi edilen hastalarda bildirilen advers reaksiyonlar | |
Enfeksiyonlar ve enfestasyonlar | |
Yaygın: | Enfeksiyonlar, herpes zoster, farenjit, oral kandidiyazis |
Yaygın olmayan: | Fırsatçı enfeksiyon (PCP dahil), sepsis, herpetik meningoensefalit ,CMV enfeksiyonu, CMV reaktivasyonu, hepatit B virüsü, herpes simpleks, enfeksiyon reaktivasyonu, yara enfeksiyonu, gastroenterit |
(Kist ve polipler de dahil olmak üzere) İyi huylu ve kötü huylu neoplazmalar | |
Yaygın olmayan: | Miyelodisplastik sendrom (MDS), sekonder maligniteler (miyeloid lösemi dahil) |
Kan ve lenf sistemi hastalıkları | |
Yaygın: | Febril nötropeni, nötropeni, trombositopeni, lenfopeni, lökopeni, anemi |
Yaygın olmayan: | Uzamış pansitopeni, aplastik anemi†, pansitopeni, peteşi |
Bağışıklık sistemi hastalıkları | |
Yaygın: | Alerjik reaksiyon |
Yaygın olmayan: | Anaflaksi |
Endokrin hastalıklar | |
Yaygın: | Cushingoid |
Yaygın olmayan: | Diabetes insipidus |
Metabolizma ve beslenme hastalıkları | |
Çok Yaygın: | Anoreksi |
Yaygın: | Hiperglisemi |
Yaygın olmayan: | Hipokalemi, alkali fosfataz artışı |
Psikiyatrik hastalıklar | |
Yaygın: | Ajitasyon, amnezi, depresyon, anksiyete, konfüzyon, insomni |
Yaygın olmayan: | Davranış bozukluğu, emosyonel labilite, halüsinasyonlar, apati |
Sinir sistemi hastalıkları | |
Çok Yaygın: | Konvülsiyonlar, hemiparezi, afazi/disfazi, baş ağrısı |
Yaygın: | Ataksi, denge bozukluğu, bilişsel bozukluk, konsantrasyon bozukluğu, bilinç azalması, baş dönmesi, hipoestezi, hafıza bozukluğu, |
| nörolojik bozukluk, nöropati , parestezi, somnolans, konuşma bozukluğu, tat duyumunda değişiklik, tremor |
Yaygın olmayan: | Status epileptikus, hemipleji, ekstrapiramidal bozukluk, parosmi, yürümede anormallik, hiperestezi, duyusal bozukluk, anormal koordinasyon |
Göz hastalıkları | |
Yaygın: | Hemianopi, bulanık görme, görme bozukluğu , görme alanı defekti, diplopi, göz ağrısı |
Yaygın olmayan: | Görme keskinliğinde azalma, gözlerde kuruluk |
Kulak ve iç kulak hastalıkları | |
Yaygın: | Sağırlık , vertigo, tinnitus, kulak ağrısı |
Yaygın olmayan: | İşitme bozukluğu, hiperakuzi, otitis media |
Kardiyak hastalıklar | |
Yaygın olmayan: | Palpitasyon |
Vasküler hastalıklar | |
Yaygın: | Hemoraji, pulmoner emboli, derin ven trombozu, hipertansiyon |
Yaygın olmayan: | Serebral hemoraji, yüzde ve boyunda kızarıklık, sıcak basması |
Solunum, göğüs bozuklukları ve mediastinal hastalıklar | |
Yaygın: | Pnömoni, dispne, sinüzit, bronşit, öksürük, üst solunum yolu enfeksiyonu |
Yaygın olmayan: | Solunum yetmezliği†, interstisyel pnömonit/pnömonit, pulmoner fibroz, nazal konjesyon |
Gastrointestinal hastalıklar | |
Çok Yaygın: | Diyare, konstipasyon, bulantı, kusma |
Yaygın: | Stomatit, abdominal ağrı , dispepsi, disfaji |
Yaygın olmayan: | Abdominal distansiyon, fekal inkontinans, gastrointestinal bozukluk, hemoroidler, ağız kuruluğu |
Hepato-bilier hastalıklar | |
Yaygın olmayan: | Karaciğer yetmezliği†, karaciğer hasarı, hepatit, kolestaz, hiperbilirübinemi |
Deri ve deri altı doku hastalıkları | |
Çok Yaygın: | Döküntü, alopesi |
Yaygın: | Eritem, cilt kuruluğu, prurit |
Yaygın olmayan: | Toksik epidermal nekroliz, Stevens-Johnson sendromu, anjiyoödem, eritema multiforme, eritroderma, deri soyulması, fotosensitivite reaksiyonu, ürtiker, ekzantem, dermatit, terleme artışı, anormal pigmentasyon |
Bilinmiyor: | Eozinofili ve sistemik semptomların eşlik ettiği ilaç reaksiyonu (DRESS) |
Kas-iskelet bozuklukları, bağ doku ve kemik hastalıkları | |
Yaygın: | Miyopati, kas güçsüzlüğü, artralji, sırt ağrısı, kasiskelet ağrısı, miyalji |
Böbrek ve idrar yolu hastalıkları | |
Yaygın: | Sık idrara çıkma, üriner inkontinans |
Yaygın olmayan: | Dizüri |
Üreme sistemi ve meme hastalıkları | |
Yaygın olmayan: | Vajinal hemoraji, menoraji, amenore, vajinit, meme ağrısı, impotans |
Genel bozukluklar ve uygulama bölgesine ilişkin hastalıklar | |
Çok Yaygın: | Yorgunluk |
Yaygın: | Ateş, grip benzeri semptomlar, asteni, kırıklık, ağrı, ödem, periferik ödem |
Yaygın olmayan: | Durumda ağırlaşma, rigor, yüzde ödem, dil renginde değişiklik, susama, diş hastalığı |
Araştırmalar | |
Yaygın: | Karaciğer enzimlerinde yükselme , vücut ağırlığında azalma, vücut ağırlığında artma |
Yaygın olmayan: | Gama-glutamiltransferaz artışı |
Yaralanma, zehirlenme ve prosedüre bağlı komplikasyonlar | |
Yaygın: | Radyasyona bağlı hasar |
Yeni teşhis edilen glioblastoma multiformeli hastalar:
Laboratuvar sonuçları:
Temozolomid dahil çoğu sitotoksik ajan için doz kısıtlayıcı olduğu bilinen miyelosupresyon (nötropeni ve trombositopeni) gözlemlenmiştir. Eş zamanlı ve monoterapi tedavi fazları için laboratuvar anormallikleri ve advers olaylar kombine edildiğinde, nötropenik olaylar dahil evre 3 veya evre 4 nötrofil anormallikleri hastaların % 8'inde gözlenmiştir. Trombositopenik olaylar dahil evre 3 veya evre 4 trombosit anormallikleri temozolomid alan hastaların % 14'ünde gözlenmiştir.
Rekürran veya progresif malign gliomalı hastalar:
Laboratuvar sonuçları:
Evre 3 veya 4 trombositopeni ve nötropeni malign glioma için tedavi edilen hastaların sırasıyla % 19 ve % 17'sinde görülmüştür. Bu durum hastaların sırasıyla % 8 ve % 4'ünde temozolomid tedavisinin kesilmesini ve/veya hospitalizasyonu gerektirmiştir.
Miyelosupresyon tahmin edilebilir olup (genellikle ilk birkaç kürde, en düşük noktası 21 ve 28. günler arasında görülmüş), düzelme hızlı ve genellikle 1-2 hafta içinde olmuştur. Kümülatif miyelosupresyona ilişkin kanıtlar gözlenmemiştir. Trombositopeni varlığı kanama riskini arttırabilir ve nötropeni veya lökopeni varlığı enfeksiyon riskini arttırabilir.
Cinsiyet:
Klinik çalışma deneyiminin popülasyon farmakokinetik analizinde 101 kadın ve 169 erkek hastadaki en düşük mutlak nötrofil sayısı ve 110 kadın ve 174 erkek hastadaki en düşük mutlak trombosit sayısı kaydedilmiştir. Evre 4 nötropeni, (MNS < 500 hücre/mikrolitre), tedavinin 1. küründe kadınlarda % 12, erkeklerde % 5, trombositopeni (< 20,000 hücre/mikrolitre) ise kadınlarda % 9 erkeklerde % 3 olarak saptanmıştır. 400 rekürran gliomalı hastayı içeren veri setinde, tedavinin ilk küründe Evre 4 nötropeni kadınların % 8, erkeklerin % 4'ünde gelişirken, Evre 4 trombositopeni kadınların % 8, erkeklerin ise % 3'ünde gelişmiştir. Yeni glioblastoma multiforme tanısı konmuş 288 hastayı içeren bir çalışmada, tedavinin ilk küründe Evre 4 nötropeni, kadınların % 3'ünde görülürken erkeklerde bu oran % 0'dır. Evre 4 trombositopeni ise kadınların % 1'inde görülürken erkeklerde bu oran % 0'dır.
Pediyatrik popülasyon
Oral temozolomid nüks eden beyin sapı glioması veya nüks eden yüksek dereceli astrositoması olan pediyatrik hastalarda (3-18 yaş arası) 28 günde bir 5 gün boyunca uygulanan bir rejimde çalışılmıştır. Veriler sınırlı olmakla birlikte, çocuklardaki toleransın erişkinlerdekiler ile aynı olması beklenir. 3 yaşın altındaki çocuklarda temozolomidin güvenliliği belirlenmemiştir.
Şüpheli advers reaksiyonların raporlanması
Ruhsatlandırma sonrası şüpheli advers reaksiyonlarının raporlanması büyük önem taşımaktadır. Raporlanma yapılması, ilacın yarar/risk dengesinin sürekli olarak izlenmesine olanak sağlar. Sağlık mesleği mensuplarının herhangi bir şüpheli advers reaksiyonu Türkiye Farmakovijilans Merkezi (TÜFAM)'ne bildirmeleri gerekmektedir (www.titck.gov.tr; e- posta: tufam@titck.gov.tr; tel: 0 800 314 00 08; faks: 0 312 218 35 99).
4.9. Doz aşımı ve tedavisi
Hastalarda 500, 750, 1000 ve 1250 mg/m'lik (5 gün boyunca kür başına toplam doz) dozlar klinik olarak incelenmiştir. Doz kısıtlayıcı toksisite hematolojik toksisitedir ve birçok dozda bildirilmiştir, fakat yüksek dozlarda daha şiddetli olması beklenir. Bir hastada 10,000 mg'lık (5 gün boyunca tek bir kürde toplam doz) doz aşımı yaşanmıştır. Bildirilen yan etkiler pansitopeni, pireksi, çoklu organ yetmezliği ve ölümdür. 5 günden fazla (64 güne kadar) tedavide önerilen dozu almış hastalarda enfeksiyon ile birlikte ya da enfeksiyonsuz kemik iliği supresyonu bildirilmiş ve bazı vakalarda şiddetli ve uzun süreli olmuş ve ölüm ile sonuçlanmıştır. Doz aşımı durumunda hematolojik inceleme gerekmektedir. Gerektiği takdirde destekleyici tedavi uygulanmalıdır.
5. FARMAKOLOJİK ÖZELLİKLER
5.1. Farmakodinamik özellikler
Farmakoterapötik grup: Antineoplastik ajanlar - Diğer alkilleyici ajanlar ATC kodu: L01AX03
Etki mekanizması
Temozolomid fizyolojik pH'da hızlı bir kimyasal dönüşüm göstererek aktif bileşen olan monometil triazenoimidazol karboksamide (MTIK) dönüşen bir triazendir. MTİK'nin sitotoksisitesinin, primer olarak guaninin O pozisyonunun alkilasyonundan ve ilaveten N pozisyonunda alkilasyonundan ileri geldiği düşünülmektedir. Bunu takiben gelişen sitotoksik lezyonların, metil katılımının anormal onarımı ile ilgili olduğu düşünülmektedir.
Klinik etkililik ve güvenlilik
Yeni teşhis edilen glioblastoma multiforme
Toplam 573 hasta temozolomid + RT (n=287) veya tek başına RT (n=286) almak üzere randomize edilmiştir. Temozolomid + RT kolundaki hastalar RT'nin ilk gününden itibaren RT'nin son gününe kadar 42 gün süreyle (maksimum 49 gün) günde bir kez eş zamanlı temozolomid (75 mg/m) almıştır. Bunu RT'nin bitiminden sonraki 4 haftadan başlayarak 6 küre kadar, 28 günlük her bir kürün 1-5. günlerinde verilen temozolomid monoterapisi (150- 200 mg/m) izlemiştir. Kontrol kolundaki hastalar yalnızca RT almıştır. RT ve kombine TEMOZOLİD tedavisi süresince Pnemocytis jirovecii pnömonisine (PCP) yönelik profilaksi gerekmiştir.
Tek başına RT kolundaki 282 hastadan 161'i (% 57) ve temozolomid + RT kolundaki 277 hastadan 62'sine (% 22) takip döneminde kurtarıcı tedavi olarak temozolomid uygulanmıştır.
Genel sağkalım için tehlike oranı (HR) 1,59'dur (HR için % 95 güven aralığı (GA) =1,33 - 1,91) ve log-rank p değeri temozolomid kolunun lehine < 0,0001'dir. Hesaplanan 2 yıl veya daha uzun süre hayatta kalma olasılığı (% 26'ya karşı % 10) RT + temozolomid kolunda daha yüksektir. Yeni teşhis edilmiş glioblastoma multiformeli hastaların tedavisinde RT'ye eş zamanlı temozolomid eklenmesi ve ardından temozolomid monoterapisi tek başına RT'ye kıyasla genel sağkalımda (OS) istatistiksel olarak anlamlı iyileşme göstermiştir (Şekil 1).
ITT Popülasyonu: Genel Sağkalım
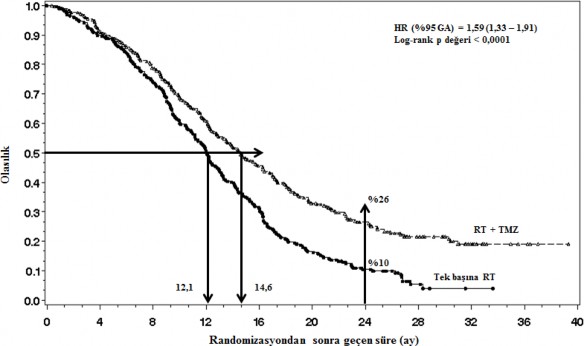
Şekil 1. Genel sağkalım için Kaplan-Meier eğrileri (ITT (tedavi amaçlı) popülasyon)
Çalışmanın sonuçları performans durumu kötü olan bir hasta alt grubunda (WHO PS=2, n=70) tutarlı değildir ve bu alt grupta genel sağkalım ve progresyona kadar geçen süre her iki kolda benzerdir. Ancak bu hasta grubunda kabul edilemez risklerin mevcut olmadığı anlaşılmaktadır.
Nüks eden veya ilerleyen malign glioma
Cerrahiden ve RT'den sonra ilerleyen veya nüks eden glioblastoma multiformeli hastalarda (Karnofski performans durumu [KPS] ≥ 70) klinik etkinlik verileri oral temozolomid ile yürütülen iki klinik çalışmaya dayanmaktadır. Bunlardan biri 138 hastada (% 29'u daha önce kemoterapi almıştı) yürütülen karşılaştırmasız bir çalışma, diğeri ise toplam 225 hastada (% 67'si daha önce nitrozoüreye dayalı kemoterapi almıştı) yürütülen, temozolomidin prokarbazin ile karşılaştırıldığı randomize, aktif-kontrollü bir çalışmadır. Her iki çalışmada, birincil son nokta manyetik rezonans görüntülemesi veya nörolojik kötüleşme ile tanımlanan progresyonsuz sağkalımdır (PFS). Karşılaştırmasız çalışmada 6 ayda PFS % 19, progresyonsuz medyan sağkalım süresi 2,1 ay ve medyan genel sağkalım 5,4 aydır. MR görüntülemelerine dayanan objektif yanıt oranı (ORR) % 8'dir.
Randomize, aktif-kontrollü çalışmada temozolomid ile 6 ayda PFS prokarbazine göre anlamlı olarak daha fazladır (% 21'e karşı % 8 – ki-kare p = 0,008) ve medyan PFS sırasıyla 2,89 ay ve 1,88 aydır (log sıra p = 0,0063). Temozolomid ve prokarbazin için medyan sağkalım süresi sırasıyla 7,34 ay ve 5,66 aydır (log sıra p = 0,33). Altı ayda, temozolomid kolunda hayatta kalan hastaların oranı (% 60) prokarbazin koluna kıyasla(% 44) anlamlı olarak daha yüksektir (ki-kare p = 0,019). Daha önce kemoterapi almış hastalarda yarar KPS
≥ 80 olan hastalarda gösterilmiştir.
Nörolojik durumda kötüleşmeye kadar geçen süreye ilişkin veriler ve performans durumunda kötüleşmeye kadar geçen süreye ilişkin veriler prokarbazine göre temozolomid lehinedir (KPS'nin < 70'e gerilemesi veya en az 30 puan azalma). Bu son noktalarda progresyona kadar geçen medyan süreler prokarbazine kıyasla temozolomid ile 0,7 – 2,1 ay daha uzundur (log sıra p = < 0,01 - 0,03).
Nüks eden anaplastik astrositoma
Anaplastik astrositomalı hastaların ilk relapstaki tedavisinde oral temozolomidin güvenliliğini ve etkililiğini değerlendiren çok-merkezli, ileriye dönük bir faz II çalışmada, 6 ayda PFS % 46 ve medyan PFS 5,4 aydır. Medyan genel sağkalım süresi 14,6 aydır. Merkezi gözden geçirmeyi yapan araştırmacının değerlendirmesine dayanan yanıt oranı tedavi amaçlı popülasyonda (ITT) (n=162) % 35'dir (13 tam yanıt ve 43 kısmi yanıt). 43 hastada stabil hastalık bildirilmiştir. ITT popülasyonunda 6 aylık olaysız sağkalım oranı % 44 ve medyan olaysız sağkalım süresi 4,6 aydır; bu rakamlar progresyonsuz sağkalım sonuçlarıyla benzerdir. Uygun nitelikteki histoloji popülasyonunda etkinlik sonuçları benzerdir. Radyolojik objektif yanıta ulaşılması veya progresyonsuz durumun korunması yaşam kalitesinin korunması veya iyileşmesiyle güçlü biçimde ilişkili bulunmuştur.
Pediyatrik hastalar:
Oral temozolomid, 28 günde bir 5 gün boyunca günlük olarak uygulanmış bir rejimde nüks eden beyin sapı glioması ya da nüks eden yüksek evreli astrositomu olan pediyatrik hastalarda (3-18 yaş) incelenmiştir. Temozolomide tolerans erişkinlerdekine benzerdir.
5.2. Farmakokinetik özellikler
Genel özellikler
Temozolomid fizyolojik pH'de esas olarak aktif tür olan 3-metil-(triazen-1-il)imidazol-4- karboksamide (MTİK) kendiliğinden hidrolize olur. MTİK, pürin ve nükleik asit biyosentezinde bilinen bir ara bileşik olan 5-amino-imidazol-4-karboksamide (AİK) ve aktif alkilleyici tür olduğuna inanılan metilhidrazine kendiliğinden hidrolize olur. MTİK sitotoksisitesinin, esas olarak guaninin O ve N pozisyonlarında olmak üzere DNA alkillenmesinden kaynaklandığı düşünülmektedir. Temozolomid EAA'sına kıyasla MTİK ve AİK'ye maruziyet sırasıyla ~% 2,4 ve % 23'tür. İn vivo MTİK'nin t'si temozolomidinkine (1,8 saat) benzerdir.
Emilim:
Erişkin hastalarda oral yoldan uygulandıktan sonra temozolomid hızla emilmekte ve dozdan sonra 20 dakika gibi kısa bir sürede doruk konsantrasyona ulaşmaktadır (ortalama süre 0,5 ile 1,5 saat). C ile işaretlenmiş temozolomid oral yolla uygulandıktan sonra C'nin dozdan sonra 7 gün boyunca feçes ile ortalama atılım oranı % 0,8 bulunmuştur; bu oran tam emilimi gösterir.
Dağılım:
Temozolomid proteinlere düşük oranda bağlanır (% 10-% 20) ve proteine yüksek oranda bağlanan ajanlarla etkileşmesi beklenmez.
Klinik öncesi veriler ve insanlarda yapılan PET çalışmaları, temozolomidin kan beyin bariyerini hızla geçtiğini ve beyin-omurilik sıvısında (BOS) bulunduğunu düşündürmektedir. Beyin omurilik sıvısına penetrasyonu 1 hastada doğrulanmıştır ve temozolomidin eğri altında kalan alanına göre BOS maruz kalımı plazmadakinin yaklaşık % 30'u kadardır; bu bulgu hayvan verileriyle paraleldir.
Biyotransformasyon:
Oral uygulamayı takiben dozun ortalama % 5-% 10'u 24 saat içinde idrarla değişmeden ve geriye kalanı ise temozolomid asidi, 5-aminoimidazol-4-karboksamid (AİK) veya tanımlanmamış polar metabolitler şeklinde atılmaktadır. Plazma konsantrasyonları doza- bağımlı bir tarzda artmaktadır.
Eliminasyon:
Plazma yarılanma ömrü (t1/2) yaklaşık 1,8 saattir. 14C'nin eliminasyonu esas olarak böbreklerde gerçekleşir.
Hastalardaki karakteristik özellikler
Temozolomidin popülasyon bazlı farmakokinetik analizi sonucunda plazma temozolomid klerensinin yaş, böbrek fonksiyonu veya tütün kullanımından bağımsız olduğu bulunmuştur. Diğer bir farmakokinetik çalışmada hafif ilâ orta dereceli hepatik disfonksiyonu bulunan hastaların, normal hepatik fonksiyonu olan hastalar ile benzer plazma farmakokinetik profilleri olduğu gözlenmiştir.
Pediyatrik hastalarda eğri altında kalan alan (EAA) daha büyüktür; ancak, maksimum tolere edilebilen doz (MTD) hem çocuklar hem de erişkinlerde kür başına 1000 mg/m dir.
5.3. Klinik öncesi güvenlilik verileri
Sıçanlarda ve köpeklerde tek kürlük (5-günlük doz, 23 günlük tedavisiz dönem), üç ve altı kürlük toksisite çalışmaları yürütülmüştür. Toksisitenin primer hedefleri kemik iliği, lenforetiküler sistem, testisler ve gastrointestinal kanaldı ve daha yüksek dozlarda (test edilen sıçanların ve köpeklerin % 60-100'ünde ölümcül olmuştur) retina dejenerasyonu gözlenmiştir. Erkek üreme sistemi ve retina dejenerasyonunu içeren istenmeyen olaylar hariç, toksisitenin büyük kısmı geri dönüşlü olma bulguları sergilemiştir. Ancak retina dejenerasyonundan sorumlu tutulan dozlar ölümcül doz aralığında olduğundan ve klinik çalışmalarda benzer bir etki gözlenmediğinden, bu bulgunun klinik yönden önemli olduğu düşünülmemiştir.
Temozolomid embriyotoksik, teratojenik ve genotoksik alkilleyici ajandır. Temozolomid sıçan ve köpeklerde insanlara göre daha toksiktir ve klinik doz sıçan ve köpeklerde minimum ölümcül doza yakındır. Lökosit ve trombositlerin doza bağlı olarak azalmaları, toksisitenin duyarlı birer göstergesidir. Altı kürlük sıçan çalışmasında gözlemlenen meme karsinomları, deride keratoakantoma ve bazal hücreli adenomu içeren çeşitli neoplazmlar gözlenmiş ancak köpek çalışmalarında tümörler veya preneoplastik değişiklikler gözlenmemiştir. Sıçanların temozolomidin onkojenik etkilerine özellikle duyarlı olduğu anlaşılmaktadır ve ilk tümörler dozaja başlandıktan sonra 3 ay içinde görülmüştür. Bu latent dönem bir alkilleyici ajan için bile çok kısadır.
Ames/Salmonella ve İnsan Periferik Kan Lenfositi (HPBL) kromozom aberasyonu testlerinin sonuçlarında pozitif bir mutajenik yanıt görülmüştür.
6. FARMASÖTİK ÖZELLİKLER
6.1. Yardımcı maddelerin listesi
Anhidr laktoz (sığır sütünden elde edilir) Anhidr silika kolloidal
Tip A sodyum nişasta glikolat Tartarik asit granülü
Stearik asit
Jelatin (sığır jelatini) Titanyum dioksit Sodyum lauril sülfat Gomalak
Propilen glikol Saf su
Amonyum hidroksit Potasyum hidroksit Siyah demir oksit
6.2. Geçimsizlikler
Uygulanamaz.
6.3. Raf ömrü
24 ay
6.4. Saklamaya yönelik özel tedbirler
25°C'nin altındaki oda sıcaklığında saklayınız.
6.5. Ambalajın niteliği ve içeriği
Karton kutuda 5 adet kapsül içeren, çocuk emniyet kapaklı amber renkli (USP Tip III) cam şişede sunulmaktadır.
6.6. Beşeri tıbbi üründen arta kalan maddelerin imhası ve diğer özel önlemler
Kapsüller açılmamalıdır. Kapsülün tahrip olması halinde, cilt ya da mukoz membranların kapsülün toz içeriği ile temasından kaçınılmalıdır. Temas olduğu takdirde bölge su ve sabunla hemen ve iyice yıkanmalıdır.
Herhangi bir kullanılmamış ürün ya da atık materyal, yerel düzenlemelere uygun olarak atılmalıdır.
Hastalara kapsülleri çocukların göremeyeceği ve erişemeyeceği bir yerde, tercihen kilitli bir dolapta saklamaları söylenmelidir. Kazara yutulmaları özellikle çocuklarda ölüme sebebiyet verebilir.
Kullanılmamış olan ürünler ya da atık materyaller ‘Tıbbi Atıkların Kontrolü Yönetmeliği' ve ‘Ambalaj ve Ambalaj Atıklarının Kontrolü Yönetmelikleri'ne uygun olarak imha edilmelidir.
Sitotoksik ve sitostatik beşeri tıbbi ürünlerin kullanımları sonucu boşalan iç ambalajlarının atıkları TEHLİKELİ ATIKTIR ve bu atıkların yönetimi 2/4/2015 tarihli ve 29314 sayılı Resmî Gazetede yayımlanan Atık Yönetimi Yönetmeliğine göre yapılır.
 Gıda Alerjisi
Her yıl milyonlarca insan yiyeceklere alerji gösteriyor.
Gıda Alerjisi
Her yıl milyonlarca insan yiyeceklere alerji gösteriyor. |
 Pankreas Kanseri
Pankreas karnın alt kısmında yatay şekilde bulunan bir organdır. Sindirime yardımcı olan enzimleri ve kan şekerini yönetmeye yardımcı olan hormonları vücuda dağıtmakla görevlidir.
Pankreas Kanseri
Pankreas karnın alt kısmında yatay şekilde bulunan bir organdır. Sindirime yardımcı olan enzimleri ve kan şekerini yönetmeye yardımcı olan hormonları vücuda dağıtmakla görevlidir. |
İLAÇ EŞDEĞERLERİ
| Eşdeğer İlaç Adı | Barkodu | İlaç Fiyatı |
|---|---|---|
| TEMODAL | 8699636150504 | 4,433.99TL |
| TEMOMID | 8699828150442 | |
| TEMOTU | 8699650151365 | 3,507.46TL |
| TEMOZOLID | 8699769150051 | 4,655.38TL |
| Diğer Eşdeğer İlaçlar |
 |
İnme İnme, beynin hasar görmesinin sonucudur. Bu hasar, beynin bir kısmındaki ya bir kanama ya da akut kan eksikliği nedeniyle o kısmın geçici ya da kalıcı olarak işlevini yapamamasına yol açar. |
 |
Deri Kanseri Deri kanseri çok rastlanan bir hastalıktır. Üç ana türü bulunur ;genelde kemirici ülser olarak bilinen bazal hücreli karsinom, yassı hücreli karsinom ve kötü huylu tümör. |
 |
Depresyonu Anlamak Depresyon farklı kişileri farklı biçimlerde etkiler. Duygusal veya fiziksel olmak üzere geniş alanda belirtilere sebep olabilir.Depresyona neler sebep olur? |
İLAÇ GENEL BİLGİLERİ
Dem İlaç San. Tic. Ltd. Şti.
| Geri Ödeme Kodu | A15691 |
| Satış Fiyatı | 11187.47 TL [ 4 May 2026 ] |
| Önceki Satış Fiyatı | 11187.47 TL [ 27 Apr 2026 ] |
| Original / Jenerik | Jenerik İlaç |
| Reçete Durumu | Normal Reçeteli bir ilaçdır. |
| Barkodu | 8699769150068 |
| Etkin Madde | Temozolomid |
| ATC Kodu | L01AX03 |
| Birim Miktar | 250 |
| Birim Cinsi | MG |
| Ambalaj Miktarı | 5 |
| Antineoplastik ve İmmünomodülatör Ajanlar > Alkilleyici Ajanlar > Temozolomid |
| İthal ( ref. ülke : Yunanistan ) ve Beşeri bir ilaçdır. |