SPINRAZA 12 mg/5 ml intratekal enjeksiyonluk ��zelti K�sa �r�n Bilgisi
{ Nusinersen }
1. BE�ER� TIBB� �R�N�N ADI
SP�NRAZA 12 mg/5 ml intratekal enjeksiyonluk ��zelti
2. KAL�TAT�F VE KANT�TAT�F B�LE��M
Etkin madde
Her 5 ml flakon, 12 mg nusinersene e�de�er nusinersen sodyum i�erir. Her ml 2,4 mg nusinersen i�erir.
Yard�mc� maddeler
Her bir flakon sodyum dihidrojen fosfat dihidrat, disodyum fosfat, sodyum klor�r, potasyum klor�r ve pH ayarlay�c� olarak sodyum hidroksit i�ermektedir.
Yard�mc� maddeler i�in 6.1'e bak�n�z.
3. FARMAS�T�K FORMU
Enjeksiyonluk ��zelti.
pH de�eri yakla��k 7.2 olan berrak ve renksiz ��zelti.
Uygulamadan �nce, flakon buzdolab�ndan ��kar�lmal� ve harici �s� kaynaklar� kullan�lmaks�z�n oda s�cakl���na (25°C) gelmesi sa�lanmal�d�r.
4. KL�N�K �ZELL�KLER
4.1. Terap�tik endikasyonlar
SP�NRAZA, 5q Spinal Musk�ler Atrofi tedavisinde endikedir.
4.2. Pozoloji ve uygulama �ekli
SP�NRAZA tedavisi sadece spinal m�sk�ler atrofi (SMA) tedavisinin y�netiminde tecr�beli bir
doktor taraf�ndan ba�lat�lmal�d�r.
Tedavi karar�, SP�NRAZA ile tedavinin potansiyel risklerine kar��l�k tedavinin birey i�in beklenen faydalar�n�n bir uzman taraf�ndan bireye �zg� de�erlendirmesine dayanmal�d�r. SP�NRAZA'n�n �al���lmad��� do�umda �iddetli hipotonisi ve solunum yetmezli�i olan hastalar, ciddi SMN protein eksikli�i nedeniyle klinik olarak anlaml� bir fayda sa�lamayabilir.
Pozoloji:
SP�NRAZA, lomber ponksiyon ile intratekal kullan�m i�indir. �nerilen doz her uygulama i�in 12 mg (5 ml)'d�r.
SP�NRAZA tedavisi, te�histen sonra m�mk�n olan en erken s�rede 0, 14, 28 ve 63. g�nlerdeki
4 y�kleme dozuyla ba�lat�lmal�d�r. Bunun sonras�nda, her 4 ayda bir idame dozu uygulanmal�d�r.
Tedavinin s�resi
Bu t�bbi �r�n�n uzun s�reli etkilili�i ile ilgili bilgi mevcut de�ildir. Tedavinin s�rd�r�lmesi ihtiyac� d�zenli olarak g�zden ge�irilmeli ve hastan�n klinik durumuna ve tedaviye yan�t�na ba�l� olarak bireysel olarak de�erlendirilmelidir.
Ka��r�lan ve geciken dozlar
E�er bir y�kleme dozu ka��r�ld� veya geciktiyse; SP�NRAZA, dozlar aras�nda en az 14 g�n olacak �ekilde m�mk�n olan en k�sa s�rede uygulanmal� ve re�ete edilen s�kl�kta dozlamaya devam edilmelidir. E�er bir idame dozu ka��r�ld� veya geciktiyse; SP�NRAZA, m�mk�n olan en k�sa s�rede uygulanmal� ve her 4 ayda bir dozlamaya devam edilmelidir.
Uygulama �ekli:
Tedavi, lomber ponksiyon uygulamalar�nda deneyimli sa�l�k meslek mensuplar� taraf�ndan uygulanmal�d�r.
SP�NRAZA, spinal anestezi i�nesi kullan�larak 1 ila 3 dakika boyunca intratekal bolus enjeksiyon ile uygulan�r. Enjeksiyon, cildin enfeksiyon veya inflamasyon belirtileri olan b�lgelerine yap�lmamal�d�r. SP�NRAZA uygulamas�ndan �nce enjekte edilecek SP�NRAZA hacmine e�de�er hacimde boyun omurilik s�v�s�n�n (BOS) al�nmas� �nerilmektedir.
SP�NRAZA uygulamas� i�in hastan�n klinik durumuna g�re sedasyon gerekebilir. �zellikle daha k���k hastalarda ve skolyozlu hastalarda ultrason (veya di�er g�r�nt�leme teknikleri) rehberli�inde, SP�NRAZA'n�n intratekal uygulamas� d���n�lebilir. SP�NRAZA'n�n haz�rlanmas�nda ve uygulanmas�nda aseptik teknikler kullan�lmal�d�r; kullan�m talimatlar� i�in bkz. b�l�m 6.6.
�zel pop�lasyonlara ili�kin bilgiler:
B�brek yetmezli�i:
SP�NRAZA, b�brek yetmezli�i olan hastalarda �al���lmam��t�r. B�brek yetmezli�i olan hastalarda g�venlilik ve etkilili�i saptanmam��t�r ve bu hastalar yak�ndan takip edilmelidir.
Karaci�er yetmezli�i:
SP�NRAZA, karaci�er yetmezli�i olan hastalarda �al���lmam��t�r. SP�NRAZA, karaci�erde sitokrom P450 enzim sistemi ile metabolize edilmez, bu nedenle karaci�er yetmezli�i olan hastalarda doz ayarlamas� yap�lmas� gerekli de�ildir (bkz. b�l�m 4.5 ve 5.2).
Pediyatrik pop�lasyon:
�ocuklar i�in ayr� bir doz ayarlamas� yoktur.
Geriyatrik pop�lasyon:
65 ya� �st�ndeki hastalarda veri bulunmamaktad�r.
4.3. Kontrendikasyonlar
Etkin madde
Her 5 ml flakon, 12 mg nusinersene e�de�er nusinersen sodyum i�erir. Her ml 2,4 mg nusinersen i�erir.
4.4. �zel kullan�m uyar�lar� ve �nlemleri
Lomber ponksiyon prosed�r�
Lomber ponksiyon prosed�r�n�n bir par�as� olarak advers reaksiyonlar�n ortaya ��kma riski vard�r (�rne�in; ba� a�r�s�, s�rt a�r�s�, kusma. bkz. b�l�m 4.8). Bu uygulama y�nteminin potansiyel zorluklar� �ok k���k hastalarda ve skolyozu olanlarda g�r�lmektedir. SP�NRAZA'n�n intratekal uygulamas�na yard�mc� olmak i�in ultrason veya di�er g�r�nt�leme tekniklerinin kullan�m� doktorun takdirine ba�l� olarak d���n�lebilir.
Trombositopeni ve koag�lasyon anomalileri
Subk�tan veya intraven�z olarak uygulanan di�er antisens oligon�kleotidlerin uygulanmas�ndan sonra akut ciddi trombositopeni dahil trombositopeni ve koag�lasyon anomalileri g�zlenmi�tir. E�er klinik olarak gerekliyse, SP�NRAZA uygulamas�ndan �nce platelet ve koag�lasyon laboratuvar testlerinin yap�lmas� �nerilmektedir.
Renal toksisite
Subk�tan ve intraven�z uygulanan di�er antisens oligon�kleotidlerin uygulanmas�ndan sonra
renal toksisite g�zlenmi�tir. E�er klinik olarak gerekliyse, idrar protein testlerinin (tercihen sabah ilk idrar �rne�i kullan�larak) yap�lmas� �nerilmektedir. �drar proteinin inat�� art��� i�in
ileri de�erlendirmeler d���n�lmelidir.
Hidrosefali:
Pazarlama sonras� raporlarda menenjit veya nusinersen ile tedavi edilen hastalarda kanama ile ili�kili olmayan komunikan hidrosefali bildirilmi�tir. Baz� hastalar ventrik�loperitoneal �ant ile implante edildi. Bilin� kayb� olan hastalarda, hidrosefali i�in bir de�erlendirme d���n�lmelidir. Ventrik�loperitoneal �ant� olan hastalarda nusinersen tedavisinin yararlar� ve riskleri halen bilinmemektedir ve tedavinin s�rd�r�lmesi dikkatle de�erlendirilmelidir.
4.5. Di�er t�bbi �r�nler ile etkile�imler ve di�er etkile�im �ekilleri
Hi�bir etkile�im �al��mas� yap�lmam��t�r. �n vitro �al��malar, nusinersenin CYP450 arac�l� metabolizman�n ind�kleyicisi ya da inhibit�r� olmad���n� g�stermi�tir. �n vitro �al��malar, plazma proteinlerine ba�lanmak i�in yar��ma ya da ta��y�c�larla yar��ma veya inhibisyonu nedeniyle nusinersen ile etkile�me olas�l���n�n d���k oldu�unu g�stermi�tir.
�zel pop�lasyonlara ili�kin ek bilgiler Herhangi bir etkile�im �al��mas� yap�lmam��t�r. Pediyatrik pop�lasyon:
Herhangi bir etkile�im �al��mas� yap�lmam��t�r.
4.6. Gebelik ve laktasyon
Genel tavsiyeGebelik kategorisi: B
Hayvanlardaki toksisite �al��malar�nda; �reme organlar�, erkek veya di�i fertilitesi veya embriyo-fetal geli�im �zerine hi�bir etki g�zlenmemi�tir.
�ocuk do�urma potansiyeli bulunan kad�nlar / Do�um kontrol� (Kontrasepsiyon):
SP�NRAZA i�in, gebeliklerde maruz kalmaya iliskin klinik veri mevcut de�ildir.
Hayvanlar �zerinde yap�lan �al�smalar, gebelik / embriyonal / fetal gelisim / do�um ya da do�um sonras� geli�im ile ilgili olarak do�rudan ya da dolayl� zararl� etkiler oldu�unu g�stermemektedir (bkz. k�s�m 5.3).
Gebe kad�nlara verilirken tedbirli olunmal�d�r.
Gebelik d�nemi:
SP�NRAZA'n�n gebe kad�nlarda kullan�m�na ili�kin yetersiz/s�n�rl� veri mevcuttur.
Hayvanlar �zerinde yap�lan �al��malar, �reme toksisitesi ile ilgili olarak do�rudan ya da dolayl� zararl� etkiler oldu�unu g�stermemektedir. (bkz. b�l�m 5.3).
Tedbir ama�l� olarak, gebelik s�resince SP�NRAZA kullan�m�ndan ka��n�lmas� daha uygundur.
Laktasyon d�nemi:
Nusinersen veya metabolitlerin'in insan s�t�yle at�l�p at�lmad��� bilinmemektedir. Yenido�an/ infant a��s�ndan bir risk oldu�u g�z ard� edilemez. Emzirmenin durdurulup durdurulmayaca��na ya da SP�NRAZA tedavisinin durdurulup durdurulmayaca��na/tedaviden ka��n�l�p ka��n�lmayaca��na ili�ki karar verilirken, emzirmenin �ocuk a��s�ndan faydas� ve SP�NRAZA tedavisinin emziren anne a��s�ndan faydas� dikkate al�nmal�d�r.
�reme yetene�i / Fertilite:
Hayvanlardaki toksisite �al��malar�nda, erkek ya da di�i fertilitesi �zerine herhangi bir etki g�zlenmemi�tir (bkz. b�l�m 5.3). �nsan fertilitesi �zerine potansiyel etkileri hakk�nda veri yoktur.
4.7. Ara� ve makine kullan�m� �zerindeki etkiler
SP�NRAZA'n�n ara� ve makine kullan�m� �zerine etkisi yoktur ya da �nemsizdir.
4.8. �stenmeyen etkiler
G�venlilik profili �zeti
SP�NRAZA'n�n g�venlilik de�erlendirmesi, SMA'l� yenido�anlarda ve �ocuklarda (CS7) bir Faz 2 �al��mas�na ve SMA genetik tan�s� alm�� pre-semptomatik yenido�anlar (CS5) ve SMA'l� yenido�anlarda ve �ocuklarda dahil a��k etiketli �al��malar ile birlikte SMA'l� yenido�an (CS3B) ve �ocuklarla (CS4) yap�lan iki Faz 3 klinik �al��maya dayanmaktad�r. CS11 �al��mas�, infantilleri ve CS3B, CS4 ve CS12 �al��malar�n� tamamlam�� olanlar da dahil olmak �zere ge� ba�lang��l� hastalar� kaydetmi�tir. En fazla 5 y�la kadar SP�NRAZA alan 346 hastan�n 258 tanesi en az 1 y�l tedavi g�rm��t�r.
Advers reaksiyonlar�n tablola�t�r�lm�� listesi
�stenmeyen etkiler, Tablo 2'de MedDRA Sistem Organ S�n�f� ve s�kl�k kategorilerine g�re listelenmi�tir. S�kl�klar t�m dereceleri temel almaktad�r ve istenmeyen etkiler a�a��daki s�kl�k derecesine g�re listelenmi�tir:
�ok yayg�n (≥ 1/10); yayg�n (≥ 1/100 ila < 1/10); yayg�n olmayan (≥ 1/1.000 ila < 1/100);
seyrek (≥ 1/10.000 ila < 1/1.000); �ok seyrek (< 1/10.000); bilinmeyen (eldeki verilerden hareketle tahmin edilemiyor).
Tablo 1: CS4 (ge� ba�lang��l� SMA) �al��mas�nda, SP�NRAZA ile tedavi edilen hastalarda sham kontrol grubuna g�re %5 daha y�ksek olan lomber ponksiyon prosed�r� ile ili�kili advers reaksiyon insidans oranlar�
MedDRA Sistem Organ S�n�f� | MedDRA tercih edilen terim | SP�NRAZA S�kl�k Kategorisi, n=84 |
Sinir sistemi hastal�klar� | Ba� a�r�s�* | �ok yayg�n |
Gastrointestinal hastal�klar | Kusma* | �ok yayg�n |
Kas-iskelet bozukluklar�, ba� doku ve kemik hastal�klar� | S�rt A�r�s�* | �ok yayg�n |
Pazarlama sonras� deneyim
Spinraza'n�n onay sonras� kullan�m� s�ras�nda advers reaksiyonlar tespit edilmi�tir. Lomber ponksiyon prosed�r� ile Spinraza uygulanan hastalar aras�nda, menenjit gibi ciddi enfeksiyonlar g�zlenmi�tir. Komunikan hidrosefali, aseptik menenjit ve a��r� duyarl�l�k (�rne�in anjiyo�dem, �rtiker ve d�k�nt�) da rapor edilmi�tir. Bu reaksiyonlar�n s�kl���, reaksiyonlar pazarlama sonras� verilerden raporland��� i�in bilinmemektedir.
Se�ilmi� advers reaksiyonlar�n tan�mlanmas�
Lomber ponksiyon ile SP�NRAZA uygulamas�yla ili�kili advers reaksiyonlar g�zlenmi�tir. Bunlar�n b�y�k bir k�sm� prosed�rden sonraki 72 saat i�inde rapor edilmi�tir. Bu olaylar�n insidans� ve �iddeti, lomber ponksiyon ile meydana gelmesi beklenen olaylarla uyumluydu. SP�NRAZA'n�n klinik �al��malar�nda, ciddi enfeksiyonlar gibi lomber ponksiyonun hi�bir ciddi komplikasyonu g�zlenmemi�tir.
SP�NRAZA'ya maruz kalan yenido�an pop�lasyonunda, lomber ponksiyonla yayg�n bir �ekilde ili�kili olan baz� advers olaylar (�rn., ba� a�r�s� ve s�rt a�r�s�) bu ya� grubunun s�n�rl� s�zl� ileti�imi nedeniyle de�erlendirilememi�tir.
�mmunojenesite
Nusinersene immunojenik yan�t�, anti-ila� antikorlar� (ADA) i�in ba�lang�� plazma �rnekleri ve ba�lang�� sonras� plazma �rnekleri bulunan 346 hastada belirlenmi�tir. Genel olarak, 4 tanesi ge�ici, 5 tanesi kal�c� ve 6 hastada ise veri kesilmesi s�ras�nda ge�ici veya kal�c� olarak s�n�fland�r�lamam�� �ekilde 15 hasta (%4) genelde ADA pozitif olarak s�n�fland�r�larak ADA insidans� d���kt�r. ADA'l� hstalar�n say�s� d���k oldu�u i�in immunojenesitenin g�venlik �zerindeki etkisi resmi olarak analiz edilememi�tir. Oysaki, tedavi ile ortaya ��kan ADA-pozitif durumlar i�in tekil veriler g�zden ge�irilmi�tir ve ilgilenilen hi�bir AE tan�mlanmam��t�r.
��pheli advers reaksiyonlar�n raporlanmas�
Ruhsatland�rma sonras� ��pheli ila� advers reaksiyonlar�n raporlanmas� b�y�k �nem ta��maktad�r. Raporlama yap�lmas�, ilac�n yarar/risk dengesinin s�rekli olarak izlenmesine olanak sa�lar. Sa�l�k mesle�i mensuplar�n�n herhangi bir ��pheli advers reaksiyonu T�rkiye Farmakovijilans Merkezi (T�FAM)'ne bildirmeleri gerekmektedir (www.titck.gov.tr; e-posta: tufam@titck.gov.tr; tel: 0 800 314 00 08; faks: 0 312 218 35 99)
4.9. Doz a��m� ve tedavisi
Klinik �al��malarda, advers reaksiyonlar ile ili�kili hi�bir doz a��m� bildirilmemi�tir.
Doz a��m� durumunda, bir sa�l�k profesyoneline dan���lmas� ve hastan�n klinik durumunun yak�ndan izlenmesini kapsayan destekleyici t�bbi bak�m sa�lanmal�d�r.
E�er flakon a��lmam��sa ve ��zelti kullan�lmam��sa, tekrar buzdolab�na koyulmal�d�r (bkz. B�l�mSaklamaya y�nelik �zel tedbirler tedbirler)
5. FARMAKOLOJ�K �ZELL�KLER
5.1. Farmakodinamik �zellikler
Farmakoterap�tik grup: Kas-iskelet sistemi bozukluklar�nda kullan�lan di�er ila�lar, ATC kodu: M09AX07
Etki Mekanizmas�
Nusinersen, SMN2 pre-messenger ribon�kleik asidinin (pre-mRNA) intron 7'de bulunan intronik splice silencing b�lgesine (ISS-N1) ba�lanarak survival motor n�ron 2 (SMN2) messenger ribon�kleik asit (mRNA) transkriptlerinde ekson 7 inkl�zyonunun oran�n� artt�ran bir antisens oligon�kleotiddir (ASO). Bu ba�lanma ile ASO, normalde splicingi bask�layan splicing fakt�rlerin yerine ge�er. Bu fakt�rlerin yer de�i�imi, SMN2 mRNA's�nda ekson 7'nin tutulmas�na neden olur ve dolay�s�yla SMN2 mRNA �retildi�inde, tam uzunlukta fonksiyonel SMN proteinine �evrilebilir.
SMA, kromozom 5q �zerindeki SMN1 genindeki mutasyondan kaynaklanan ilerleyici bir n�rom�sk�ler hastal�kt�r. SMN1 geninin yan�nda yer alan ve ikinci bir gen olan SMN2, az miktarda SMN proteini �retiminden sorumludur. SMA, SMN2 gen kopyas�n�n az say�da olmas�yla ba�lant�l� olarak hastal�k �iddetinin ve semptomlar�n ortaya ��k�� ya��n�n de�i�ti�i klinik bir hastal�k yelpazesidir.
Klinik etkililik ve g�venlilik
Semptomatik hastalar
�nfantil ba�lang��
�al��ma CS3B (ENDEAR), SMA tan�s� alan (semptom ba�lang��lar� 6 aydan �nce olan), ≤7 ay olan 121 semptomatik infant ile yap�lan Faz 3, randomize, �ift k�r, sham-prosed�r kontroll� bir �al��mad�r. CS3B, SP�NRAZA'n�n motor fonksiyon ve sa�kal�m �zerine etkisini de�erlendirmek �zere tasarlanm��t�r. Hastalar, ya SP�NRAZA (onaylanan doz rejimine g�re) ya da sham kontrol grubuna 2:1 oran�nda 6 ila 442 g�n aras�nda de�i�en bir tedavi rejimine randomize edilmi�tir.
SMA klinik belirtilerinin ve semptomlar�n�n ortaya ��kt��� medyan ya�, SP�NRAZA ile tedavi edilenler ve sham-kontrol gruplar�nda s�ras�yla 6,5 hafta ve 8 haftayd�, hastalar�n %99'u SMN2 geninin 2 kopyas�n� ta��maktayd� ve bu nedenle muhtemel Tip I SMA kabul edilmi�tir. Hastalar�n ilk dozu ald��� medyan ya�, tedavi alan hastalarda 164,5 g�n ve sham-kontrol hastalar�nda 205 g�nd�. Ba�lang�� hastal�k karakteristikleri, Sham-kontrol hastalar�na k�yasla SP�NRAZA tedavisi alan hastalarda daha y�ksek oranda g�r�nen paradoksal solunum (%66'ya kar�� %89), pn�moni ve solunum semptomlar� (%22'ye kar�� %35), yutma ve beslenme g��l�kleri (%29'a kar�� %51) ve solunum deste�i gereksinimi (%15'e kar�� %26) haricinde b�y�k �l��de benzerdi.
Son analizde, sham-kontrol grubuna (%0) (p<0,0001) g�re SP�NRAZA grubunda (%51), hastalar�n istatistiksel olarak anlaml� b�y�k bir y�zdesi “motor kilometre ta�lar� yan�tl�” tan�m�na ula�m��lard�r. �l�me veya kal�c� ventilasyona (akut reversible bir olay ya da trakeostomi olmaks�z�n >21 g�n boyunca ≥16 saat ventilasyon/g�n) kadar ge�en zaman primer sonlan�m noktas� olarak de�erlendirilmi�tir. Olays�z sa�kal�m, genel sa�kal�m, bir motor kilometre ta�� yan�tl� hasta tan�m�na ula��lmas� ve ba�lang��tan itibaren Children's Hospital of Philadelphia Infant Test for Neuromuscular Disease (CHOP INTEND) skorunda en az 4 puan iyile�me g�steren hastalar�n y�zdesinde Sham-kontrol grubuna k�yasla SP�NRAZA grubunda, istatistiksel olarak anlaml� etkiler g�r�lm��t�r (Tablo 2).
Etkililik setinde, SP�NRAZA grubunda 18 hastada (%25) ve sham-kontrol grubunda 12 hastada (%32) kal�c� ventilasyon gerekmi�tir. Bu hastalardan, protokolde tan�mlanan motor kilometre ta�� yan�t kriterini kar��layanlar�n say�s� SP�NRAZA grubunda 6 (%33) ve sham-kontrol grubunda 0'd�r (%0).
Tablo 2: Son analizde primer ve sekonder sonlan�m noktalar� - �al��ma CS3B
Etkililik Parametresi | SP�NRAZA ile tedavi edilen hastalar | Sham-kontrol hastalar� |
Sa�kal�m | ||
Olays�z sa�kal�m �len veya kal�c� ventilasyona ge�en hastalar�n say�s� Tehlike Oran� (%95 GA) p-de�eri |
31 (%39) |
28 (%68) |
0,53 (0,32 – 0,89) p = 0,0046 | ||
Genel sa�kal�m �len hastalar�n say�s� Tehlike Oran� (%95 GA) p-de�eri |
13 (%16) |
%16 (39) |
0,37 (0,18 – 0,77) p=0,0041 | ||
Motor fonksiyon | ||
Motor kilometre ta�lar� �n tan�ml� motor kilometre ta�� yan�t kriterlerine ula�anlar�n oran� (HINE b�l�m 2) 183. g�ndeki oran 302. g�ndeki oran |
37 (%51) p<0,0001
%41 %45 |
0 (%0)
%5 %0 |
394. g�ndeki oran | %54 | %0 |
toplam motor kilometre ta�� skorundaki iyile�me ile orant�s� | 49 (%67) | 5 (%14) |
toplam motor kilometre skorundaki k�t�le�me ile orant�s� | 1 (%1) | 8 (%22) |
CHOP INTEND |
|
|
4 puan iyile�me olanlar�n oran� | 52 (%71) p<0,0001 | 1 (%3) |
4 puan k�t�le�me olanlar�n oran� | 2 (%3) | 17 (%46) |
Herhangi bir iyile�me olanlar�n oran� | 53 (%73) | 1 (%3) |
Herhangi bir k�t�le�me olanlar�n oran� | 5 (%7) | 18 (%49) |
CHOP INTEND'deki iyile�menin boyutu �ekil 1'de g�sterilmi�tir (her hasta i�in ba�lang��tan itibaren skordaki de�i�im).
�ekil 1: Ba�lang��tan 183. G�n, 302. G�n ve 394. g�n sonras� �al��ma vizitlerinde CHOP INTEND de�i�imi - Endear �al��mas�/CS3B (Etkililik Seti, ES)
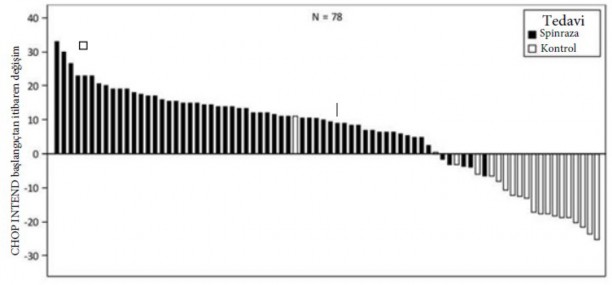
Not 1: 0. Sat�rdaki en k�sa �ubuklar hi�bir de�eri g�stermez.
Not 2: Etkililik setindeki 110 hastan�n 29'u �ld� (SP�NRAZA grubundan 13(%18), kontrol grubundan 16 (%43)), 3'� �l�m d���nda nedenlerle ayr�ld� (SP�NRAZA grubundan 2(%3), kontrol grubundan 1(%3)) ve bu nedenle ES'nin bu analizine dahil edilmedi.
Bu hastalar�n uzun s�reli takibini sa�lamak i�in, CS3B �al��mas�n�n sonunda, 89 hasta (Spinraza: n= 65; Sham kontrol: n= 24) CS11 �al��mas�na (SHINE) kaydolmu�tur. CS11 �al��mas�, daha �nce di�er Spinraza klinik �al��malar�na kat�lan SMA hastalar� i�in a��k u�lu uzat�lm�� bir �al��mad�r. CS11 �al��mas�nda, 655 g�nden 592 g�ne kadar uzayan tedavi boyunca (medyan 289 g�n) ara analiz s�ras�nda t�m hastalar Spinraza alm��lard�r. CS11 �al��mas�na en b�y�k faydan�n g�zlendi�i erken tedaviye ba�layan hastalar yan�nda CS3B'de SPINRAZA tedavisine devam edenler ve CS11 �al��mas�nda SP�NRAZA tedavisi ba�lanan hastalarda fayda g�rm��lerdir (�ekil 3). CS11 �al��mas�n�n ba�lang�c�nda ve ara analizinde s�rekli ventilasyon uygulanmayan hastalar �o�unlukla hayatta kalm��t�r.
CSB3 �al��mas�ndaki Spinraza'ya randomize edilen hastalar ve CS11 �al��ma deneyimlerinde, �l�m veya s�rekli ventilasyon medyan zaman� 73 haftad�r. CS11 �al��mas� ara analizinde 65 hastan�n 61'i (94) hayatta kalm��t�r. CS3B �al��mas�nda s�rekli ventilasyon tan�m� kapsam�na girmeyen 45 hastan�n 38'i (%84), CS11 �al��mas�n�n ara analizde s�rekli ventilasyon olmadan hayatta kalm��t�r. Ortalama motor kilometre ta��nda art�� (HINE-Section 2) (2,1; SD 4,36; n=22) ve CHOP INTEND (4,68; SD 3,993, n=22) skorlar� CS11 �al��mas�n�n ba�lang�c�ndan
304. �al��ma g�n�ne kadar g�zlenmi�tir.
CS11 �al��mas�nda ilk Spinraza uygulamas� ba�lat�lan hastalarda (n=24; CS3B �al��mas�ndaki sham-kontrol) medyan ya� 17,8 ay ( 10-23 ay aral���) ve CS11 �al��ma ba�lang�c�nda ortalama CHOP �NTEND skoru 17.25 (2,0-46,0) idi. Ara analizde 24 hastan�n 22'si (92%) hayatta kalm��t�r. CS3B �al��mas�nda s�rekli ventilasyon tan�m�n� kar��lamayan 12 hastan�n (%50) 7'si (%58) CS11 �al��mas�nda s�rekli ventilasyon gereksinimi olmadan hayatta kalm��t�r. CS11 �al��mas�nda Spinraza uygulamas�n�n ba�lat�lmas�ndan sonra �l�m veya s�rekli ventilasyon
medyan zaman� 50.9 hafta olmu�tur. Ortalama motor kilometre ta��nda art�� (HINE-Section 2) (1.2; SD 1,8; n=12) ve CHOP INTEND (3,58; SD 7,051 n=12) skorlar� CS11 �al��mas�n�n ba�lang�c�ndan 304. �al��ma g�n�ne kadar g�zlenmi�tir.
Bu sonu�lar, SMA tan�s� alan semptomatik hastalarda a��k etiketli bir faz 2 �al��ma (CS3A) ile desteklenmi�tir. Klinik belirtilerin ve semptomlar�n ortaya ��kt��� medyan ya� 56 g�nd� ve hastalar ya 2 SMN2 gen kopyas� (n=17) ya da 3 SMN2 gen kopyas� (n=2) ta��maktayd� (SMN2 gen kopya say�s� bilinmeyen 1 hasta). Bu �al��madaki hastalar muhtemel Tip 1 SMA olarak d���n�lmektedir. �lk dozun al�nd��� medyan ya� 162 g�nd�r.
Primer sonlan�m noktas�, motor kilometre ta�lar�nda bir veya daha fazla kategoride iyile�me olan hastalar�n oran�yd� (HINE b�l�m 2'ye g�re: tekme kabiliyeti ya da g�n�ll� kavramada ≥2 puan art�� [ya da azami skorda], YA DA ba��n kontrol�, yuvarlanma, oturma, emekleme, ayakta durma ve y�r�me motor kilometre ta�lar�nda ≥1 puan art��). Zamanla 20 hastan�n 12'si (%60), zaman i�inde ortalama motor kilometre ta�� ula��m�nda s�rekli iyile�me ile primer sonlan�m noktas�n� kar��lam��t�r. Ba�lang��tan 1072. g�ne kadar ortalama CHOP INTEND skorunda s�rekli bir iyile�me g�zlendi (ortalama de�i�im 21,30). Genel olarak, 20 hastan�n 11'i (%55) veri kesiminden �nceki son �al��ma vizitlerinde toplam CHOP INTEND skorunda ≥4 puan art�� ile sonlan�m noktas�n� kar��lam��t�. Kay�tl� 20 hastan�n 11'i (%55) hayatta kalm��t�r ve son ziyarette s�rekli ventilasyondan muaf tutulmu�tur. 4 hasta kal�c� ventilasyon tan�m�n� kar��lam�� ve 5 hasta ise �al��ma s�resince kaybedilmi�tir.
Ge� ba�lang��
�al��ma CS4 (CHERISH), ge� ba�lang��l� SMA's� olan (semptomlar�n 6 aydan sonra ba�lad���) 126 semptomatik hastada y�r�t�len randomize, �ift k�r, sham-prosed�r kontroll� bir faz 3 �al��mas�d�r. Hastalar, 2:1 oran�nda ya SP�NRAZA (3 y�kleme dozu ve sonras�nda her 6 ayda bir idame dozu ile dozlanan) veya sham-kontrol gruplar�nda 324. g�nden 482. g�ne de�i�en uzunluktaki tedavilerine 2:1 oran�nda randomize edilmi�tir.
Taramadaki medyan ya� 3 y�l ve SMA'n�n klinik belirti ve semptomlar�n�n ba�lad��� medyan ya� 11 ayd�. Hastalar�n �o�unlu�u (%88) 3 SMN2 gen kopyas� (%8'i 2 kopya, %2'si 4 kopya ve %2'si bilinmeyen say�da kopya) ta��maktayd�. Ba�lang��ta, hastalar�n ortalama Hammersmith Fonksiyonel Motor Skalas� Geni�letme (HFMSE) skoru 21,6, ortalama revize �st ekstremite mod�l� (RULM) 19,1 idi, hepsi ba��ms�z bir �ekilde oturmu�tu ve hi�bir hasta ba��ms�z y�r�memi�ti. Bu �al��madaki hastalar muhtemel Tip II ya da III SMA hastas� olarak kabul edildiler. Ba�lang�� hastal�k �zellikleri, desteksiz ayakta durma kabiliyetini halen kaybetmemi� hastalar�n (SP�NRAZA grubunda hastalar�n %13'� ve sham-kontrol grubunda hastalar�n %29'u) veya destekle y�r�yen hastalar�n (SP�NRAZA grubunda hastalar�n %24'� ve sham-kontrol grubunda hastalar�n %33'�) oran�ndaki bir dengesizlik d���nda genel olarak benzerdi.
Son analizde, SP�NRAZA ile tedavi edilen hastalarda, sham-kontrol hastalar�na k�yasla HFMSE skorunda ba�lang��tan itibaren 15. aya kadar istatistiksel olarak anlaml� bir iyile�me g�zlendi (Tablo 3, �ekil 2). Analiz ITT (tedavi amac�na y�nelik) pop�lasyonda (SP�NRAZA:
n=84; sham-kontrol: n=42) ger�ekle�tirildi ve �oklu imputasyon y�ntemi kullan�larak 15. ay ziyareti olmayan hastalar i�in ba�lang�� sonras� HFMSE verileri tamamland�. 15. ayda g�zlenen de�erlere sahipolan ITT pop�lasyonundaki hastalar�n alt k�mesinin bir analizinin tutarl�, istatistiksel olarak anlaml� sonu�lar verdi�i kan�tland�. 15. Ay'da g�zlenen de�erlere sahip olanlardan, Spinraza ile tedavi edilen deneklerin daha y�ksek bir oran�n�n iyile�me g�sterdi�i (s�ras�yla %41'e kar�� %73) ve daha d���k bir oranda Spinraza ile tedavi edilen deneklerin toplam HFMSE skorunda sham-kontrol�ne k�yasla k�t�le�me oldu�u (s�ras�yla %44'e kar��
%23) g�r�lm��t�r. Fonksiyonel �nlemleri ve WHO motor kilometre ta�� ba�ar�s�n� i�eren ikincil sonlan�m noktalar� resmen istatistiksel olarak test edilmi� ve Tablo 3'te a��klanm��t�r.
Semptomlar�n ba�lang�c�ndan hemen sonra tedavinin ba�lat�lmas�, gecikmi� tedavi ba�lang�c� olanlara k�yasla motor fonksiyonlarda daha erken ve daha b�y�k iyile�me kaydedilmesini sa�lam��t�r, bununla beraber sham-kontrol grubuna nazaran her iki grup da fayda g�rm��t�r.
Tablo 3: Son analizde primer ve sekonder sonlan�m noktalar� - �al��ma CS4
| SP�NRAZA ile tedavi edilen hastalar | Sham-kontrol hastalar� |
HFMSE score |
|
|
15. ayda toplam HFMSE skorunda ba�lang��tan itibaren olan de�i�im | 3,9 (%95 CI: 3,0, 4,9) p=0,0000001 | -1,0 (%95 CI: -2,5, 0,5) |
Ba�lang��tan itibaren 15. Aya kadar en az 3 puan iyile�me olan hastalar�n oran� | 56,8% (%95 CI:45,6, 68,1) P=0,0006 | 26,3% (%95 CI: 12,4, 40,2) |
RULM |
4,2 (%95 CI: 3,4, 5,0) p=0,0000001 |
0,5 (%95 CI: -0,6, 1,6) |
Toplam RULM skorunda ba�lang��tan 15. aya kadar olan ortalama de�i�im | ||
WHO motor kilometre ta�lar� |
%19,7 (%95 CI: 10,9, 31,3) p=0,0811 |
%5,9 (%95 CI: 0,7, 19,7) |
15. ayda yeni bir kilometre ta��na ula�an hastalar�n oran� |
�ekil 2: HFMSE skorunun ba�lang�c�ndan zaman i�indeki son analizde (ITT) ortalama de�i�im - �al��ma CS4
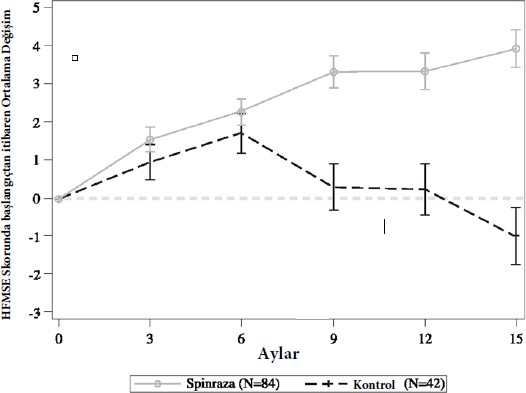
1�oklu imputasyon y�ntemi kullan�larak 15. ay ziyareti olmayan hastalar i�in veriler
CS4 (CHERISH) �al��mas� tamamlad�ktan hemen sonra 125 hasta, t�m hastalar�n Spinraza ald��� CS11'e (SHINE) �al��mas�na kaydedildi. Ara analiz zaman�nda tedavi s�resinin uzunlu�u 74 g�nden 474 g�ne kadar de�i�mekteydi (medyan 250 g�n). Spinraza ile tedavi edilen hastalar�n �o�u motor fonksiyonlarda stabilizasyon veya iyile�me g�sterirlerken, en b�y�k iyile�me erken tedavi ba�lang�c�nda g�zlenmi�tir.
�al��ma CS4'te Spinraza tedavisi ba�lat�lan hastalarda (n= 39), stabilizasyon veya ortalama HFMSE (0,2; SD 3,06) ve RULM (0,7; SD 2,69) skorlar�nda ek iyile�meler ba�lang��tan CS11 �al��mas�n�n 265. g�n�ne kadar g�zlenmi�tir.
Bu sonu�lar, 2 a��k etiketli �al��ma ile (CS2 ve CS12 �al��malar�) ile desteklenmi�tir. �lk dozlar�n� �al��ma CS2'de alan 28 hasta analize dahil edildi ve sonras�nda uzatma faz� olan �al��ma CS12'ye transfer edildi. Bu �al��malara ilk dozlar�n� 2 ila 15 ya�lar� aras�nda alan hastalar kay�t edilmi�tir. 28 hastadan 3 tanesi, son �al��ma vizitlerinde en az 18 ya��ndalard�. 28 hastadan 1'i 2 SMN2 gen kopyas�na, 21 tanesi 3 gen kopyas�na ve 6 tanesi 4 gen kopyas�na sahipti.
Hastalar 3 y�ldan fazla s�ren bir tedavi periyodunda de�erlendirilmi�tir. Tip II SMA hastalar�nda ba�lang�� HFMSE skorlar�nda 253'�nc� g�nde ortalama 5,1 (SD 4,05, n=11) ve 1050'nci g�nde
ortalama 9,1 (SS 6,61, n=9) kal�c� iyile�me g�zlenmi�tir. Plato olmaks�z�n, 253 g�n sonras�nda ortalama skor 26,4 (SD 11,91) ve 1050 g�n sonras�nda ortalama skor 31,3 (SD 13,02) idi. Tip III SMA hastalar�nda, ba�lang��tan itibaren HFMSE skorunda 253 g�n sonras�nda ortalama 1,3 (SD 1,87, n=16) ve 1050 g�n sonras�nda ortalama 1,2 (SD 4,64, n=11) toplam skorda iyile�me g�r�lm��t�r. Ortalama toplam skor 253 g�n sonras�nda 49,8 (SD 12,46) ve 1050 g�n sonras�nda 52,6 (SD 12,78) idi.
Tip II SMA'l� hastalarda �st Ekstremite Mod�l� testi, 253 g�n sonras�nda ortalama 1,9 (SD 2,68, n= 11) ve 1050 g�n sonras�nda ortalama 3,5 (SD 3,32, n= 9) ortalama iyile�me ile
y�r�t�lm��t�r. Ortalama toplam skor 253 g�n sonras�nda 13,8 (SD 3,09) ve 1050 g�n sonras�nda 15,7'dir (SD 1,92).
6MWT (6 dakika y�r�me testi) sadece ambulatuvar hastalarda yap�lm��t�r. Bu hastalarda, ortalama iyile�me 253 g�n sonras�nda 28,6 metre (SD 47,22, n=12) ve 1050 g�n sonras�nda 86,5 metre (SD 40,58, n=8) olarak g�zlendi. Ortalama 6 MWT uzunlu�u, 253 g�n sonras�nda 278,5 metre (SD 206,46) ve 1050 g�n sonras�nda 333,6 metre (SD 176,47) dir. Daha �nceden ba��ml� ambulatuvar olan 2 (Tip III) hasta ve ambulatuvar olmayan bir (Tip II) hasta ba��ms�z y�r�meyi ba�arm��lard�r.
Tarama ya�� veya SMN2 kopya numaras� �al��ma CS4 veya CS3B'ye uygun olmayan hastalar i�in ek bir klinik �al��ma olan CS7 (EMBRACE) a��lm��t�r. CS7, infantil ba�lang��l� SMA (≤6 ay) veya ge� ba�lang��l� SMA (>6 ay) ve uzun s�reli a��k etiketli uzatma �al��mas� faz�n� (2. b�l�m) takip eden 2 veya 3 SMN2 kopyas� (1. b�l�m) te�hisi konan hastalarda randomize, �ift k�r, sham-prosed�r kontroll� bir faz 2 �al��mas�d�r. �al��man�n 1. b�l�m�nde, hastalar medyan 302 g�n takip edildiler.
Spinraza alan t�m hastalar B�l�m 1'in erken sonlanmas� itibariyle hayatta kalm��t�r, ancak kontrol kolundaki bir hasta 289. �al��ma g�n�nde hayat�n� kaybetmi�tir. Ek olarak, Spinraza veya sham-kontrol grubundaki hi�bir hastada s�rekli ventilasyon kullan�m�na gerek olmam��t�r. �nfantil-ba�lang��l� SMA'l� 13 hastada, Spinraza grubundaki 9 hastan�n 7'si (%78; %95 CI:
45,94) ve sham grubundaki 4 hastan�n 0'� (%0; %95 CI: 0,60) motor kilometre ta�� cevab� i�in gerekli kriteri kar��lam��t�r (Hammersmith Infant Neurological Examination (HINE) b�l�m 2'ye g�re: tekme kabiliyeti (ya da azami skorda) ≥2 puan art��, YA DA ba��n kontrol�, yuvarlanma, oturma, emekleme, ayakta durma ve y�r�me motor kilometre ta�lar�nda ≥1 puan art��, VE motor kilometre ta�lar�nda k�t�le�me olandan daha fazla kategoride iyile�me olmas�). Ge�-ba�lang��l� SMA'l� 8 hastan�n, Spinraza grubundaki 5 hastan�n 4'� (% 80; % 95 CI: 38,96) ve sham-kontrol grubundaki 3 hastan�n 2'si (% 67; % 95 CI: 21,94) bu cevab�n tan�m�n� kar��lam��t�r.
Pre-semptomatik yenido�anlar
�al��ma CS5 (NURTURE) genetik olarak tan� alm�� SMA'l� pre-semptomatik 6 haftal�k ve daha k���k infantlarla yap�lan a��k etiketli bir �al��mad�r. Bu �al��madaki hastalar, muhtemel Tip I ve ya II SMA hastas� kabul edilmektedir. �lk doz al�nd���ndaki medyan ya� 22 g�nd�r.
Hastalar �al��man�n medyan 27.1. ay�nda (15,1-35,5 ay) ve son vizitte medyan 26 ayl�k (14,0- 34,3 ay) ya�ta iken bir ara analiz yap�ld�. Ara analizde 25 hastan�n hepsi (2 SMN2 gen kopya say�l�, n=15, 3 SMN2 gen kopya say�l�, n=10) kal�c� ventilasyon ihtiyac� g�stermeden hayattayd�. Birincil son nokta, �l�m zaman� veya solunum yolu ile m�dahale (ard���k ≥ 7g�n boyunca ≥ 6 saat/g�n s�rekli invaziv ya da non-invaziv ventilasyon VEYA trakeostomi olarak tan�mlanm��t�r) �ok az vaka oldu�u i�in tahmin edilememi�tir. Bir akut geri d�n��l� (reversible) hastal�k s�ras�nda ventilat�r deste�i ba�lat�lan d�rt hasta (2 SMN2 kopyas�) ard���k ≥ 7g�n boyunca > 6 saat/g�n s�rekli solunum yolu ile m�dahaleye ihtiya� duymu�tur.
Hastalar, normal geli�ime daha uygun olan ve Tip I ve II SMA i�in beklenmeyen kilometre ta�lar�n� ba�arm��t�r. Ara analizde, 25 hastan�n t�m� (% 100) WHO (D�nya Sa�l�k �rg�t�) motor kilometre ta�lar�nda desteksiz oturmay�, 22 hasta (%88) destekli y�r�meyi ba�arm��t�r. Daha ya�l� hastalar aras�nda WHO'nun beklenen ba�ar� ya�� i�in tan�mlanm�� penceresinden (y�zde 95), 22'sinin 17'si yaln�z y�r�meyi ba�arm��t�r. Son de�erlendirmedeki ortalama CHOP INTEND puan� 2 SMN2 kopyaya sahip hastalar aras�nda 61,0 (46 - 64) ve 3 SMN2 kopyaya sahip hastalar aras�nda 62,6 (58 - 64) idi. Son de�erlendirmede HINE b�l�m 1'deki azami skoru tutturan 22 (% 88) infantlarla birlikte t�m hastalar emme ve yutma yetene�ine sahipti.
Ara analizde 700. g�ne eri�en hastalar aras�nda klinik olarak ortaya ��kan SMA geli�en hastalar�n oran� de�erlendirildi (n=16). Klinik olarak belirgin SMA'n�n protokolde tan�mlanm�� kriterleri ya�a g�re ayarlanm�� a��rl���n WHO 5. persentilinin alt�nda olmas�, 2 ya da daha fazla temel a��rl�k geli�im e�risi persentili d����, perk�tan�z gastrik t�p yerle�tirilmesi, ve/veya ya�a uygun WHO kilometre ta�lar�n� ba�aramama (ba��ms�z oturma, yard�mla ayakta durma, el ve dizler �st�nde emekleme, destekle y�r�me, yaln�z ayakta durma ve yaln�z y�r�me). 700'�nc� g�nde, 2 SMN2 gen kopyas� olan 11 hastadan 7'si (% 64) ve 3 SMN2 kopyas� olan 5 hastan�n 0'� (% 0) klinik olarak ortaya konulan SMA'n�n protokol tan�ml� kriterlerini kar��lad�, ancak bu hastalar kilo al�yordu ve Tip IA SMA ile uyumlu olmayan WHO kilometre ta�lar�na eri�iyordu.
Semptomatik yenido�an ba�lang��l� SMA ve pre-semptomatik SMA hastalar� aras�nda motor kilometre ta�lar� ba�ar�s�n�n kar��la�t�r�lmas� �ekil 3'de g�sterilmi�tir.
�ekil 3: �al��ma CS3B (tedavi ve sham-kontrol), CS3A ve CS5 i�in HINE motor kilometre ta�lar� ve �al��ma g�nlerinin de�i�imi
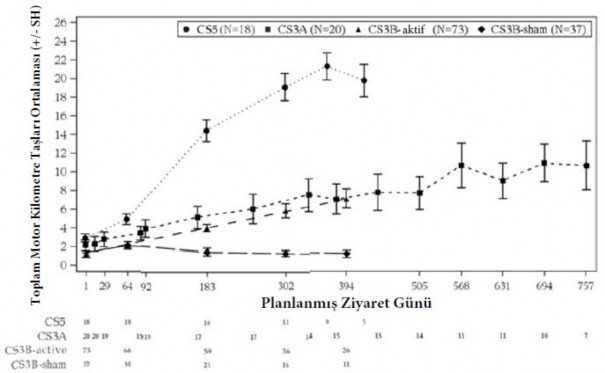
�ekilde kullan�lan pop�lasyon: CS5 – ge�ici etkinlik seti, CS3A – t�m dozlananlar, CS3B etkinlik seti Her bir �al��ma i�in, n<5 olan ziyaretler �izilmemi�tir
5.2. Farmakokinetik �zellikler
Genel �zellikler:�ntratekal enjeksiyon ile ygulanan nusinersenin tek ve �oklu doz farmakokineti�i (FK), SMA tan�s� alan pediatrik hastalarda incelenmi�tir.
Emilim:
Nusinersenin BOS'a intratekal enjeksiyonu, nusinersenin BOS'dan hedef merkezi sinir sistemi (MSS) dokular�na tamamen da��l�m�n� m�mk�n k�lar. Nusinersenin ortalama en d���k BOS konsantrasyonlar�, �oklu y�kleme ve idame dozlar�n�n ard�ndan yakla��k 1,4 ila 3 kat biriktive yakla��k 24 ay i�inde kararl� duruma ula�m��t�r. �ntratekal uygulaman�n ard�ndan nusinersenin en d���k plazma konsantrasyonlar�, en d���k BOS konsantrasyonuna g�re nispeten d���kt�r. Medyan plazma Tde�eri 1,7'den 6,0 saate de�i�mektedir. Ortalama plazma Cve EAA de�erleri, takriben doz art��� ile orant�l� olarak artm��t�r. �oklu dozlardan sonra plazma maruziyet �l��mlerinde (Cve EAA) hi�bir birikim olmam��t�r.
Da��l�m:
Hastalardan elde edilen otopsi verileri (n=3) intratekal uygulanan nusinersenin BOS i�inde
yayg�n bir �ekilde da��larak hedef omurilik dokular�nda terap�tik seviyelere ula�t���n� g�stermektedir. Nusinersenin varl���, beyin ve omurilikteki n�ronlarda ve di�er h�cre tiplerinin yan�nda iskelet kaslar�, karaci�er ve b�brek gibi periferal dokularda da g�sterilmi�tir.
Biyotransformasyon:
Nusinersen yava��a ve a��rl�kl� olarak ekzon�kleaz (3'- ve 5') arac�l� hidroliz yoluyla metabolize olmaktad�r ve CYP450 enziminin substrat�, inhibit�r� ya da ind�kleyicisi de�ildir.
Eliminasyon:
BOS'ta ortalama terminal eliminasyon yar� �mr� 135 ila 177 g�n olarak tahmin edilmektedir. Ba�l�ca eliminasyon yolunun, nusinersen ve metabolitlerinin idrarla at�l�m� oldu�u d���n�lmektedir.
Etkile�imler:
�n vitro �al��malar, nusinersenin CYP450- arac�l� oksidatif metabolizman�n bir ind�kleyicisi ya da inhibit�r� olmad���n� g�stermi�tir. Bu nedenle, bu metabolik yolaklar i�in di�er t�bbi �r�nlerle kar��mamal�d�r. Nusinersen, insan BCRP, P-gp, OAT1, OAT3, OCT1, OCT2, OATP1B1, OATP1B3 ya da BSEP ta��y�c�lar�n�n substrat� ya da inhibit�r� de�ildir.
Hastalardaki karakteristik �zellikler
B�brek ve karaci�er yetmezli�i:
B�brek ve karaci�er yetmezli�i olan hastalarda nusinersenin farmakokineti�ine ili�kin �al��ma yap�lmam��t�r. FK modelinin sunuldu�u pop�lasyonda klinik olarak ili�kili karaci�er ve b�brek yetmezli�i g�r�len hastalar�n nadir bulunmas� nedeniyle e� de�i�kenleri olarak hepatik ve renal yetmezli�in etkileri detayl� olarak incelenememi�tir. Pop�lasyon FK analizleri, hepatik ve renal klinik kimya belirte�leri ve hastalar aras� de�i�kenlik aras�nda belirgin bir korelasyon olmad���n� ortaya koymu�tur.
Irk:
Hastalar�n b�y�k k�sm� beyaz �rktand�. Pop�lasyon FK analizleri, �rk�n nursinersenin farmakokineti�ini etkilemesinin olas� olmad���n� ortaya koymu�tur.
5.3. Klinik �ncesi g�venlilik verileri
Karsinogenez
Nursinersenin karsinojenik potansiyelini de�erlendirmek i�in uzun s�reli hayvan �al��malar� yap�lmam��t�r.
Mutagenez
Nusinersenin genotoksisitesine ili�kin hi�bir kan�t yoktur. �reme toksisitesi
�reme toksikolojisi �al��malar�, fare ve tav�anlarda nursinersenin subk�tan uygulamas� kullan�larak y�r�t�lm��t�r. Erkek ya da di�i fertilitesine veya embriyo-fetal geli�ime ya da pre/post-natal geli�ime hi�bir etkisi g�zlenmemi�tir.
Toksikoloji
Yavru cynomolgus maymunlar�na intratekal uygulaman�n tekrarl� doz toksisite �al��malar�nda (14 hafta ve 53 hafta) nursinersen iyi tolere edilmi�tir. �stisnas�, her �al��mada en y�ksek doz d�zeylerinde (doz ba��na 3 ya da 4 mg; hastada her intratekal doz ba��na 30 ya da 40 mg'a e�de�erdir) alt spinal reflekslerde ortaya ��kan akut, ge�ici bir kay�pt�r. Bu etkiler dozdan sonraki birka� saat i�inde g�zlemlenmi� ve genellikle 48 saat i�inde ��z�lm��t�r.
Cynomolgus maymunlar�ndaki 53 haftal�k intratekal doz �al��mas�nda, �nerilen y�ll�k klinik idame dozunun 14 kat� kadar seviyelerde toksik etki g�r�lmemi�tir.
Uygulamadan hemen �nce, plastik kapa�� ��kar�n ve ��r�nga i�nesini �st contan�n ortas�ndan flakon i�ine sokarak uygun hacimde s�v�y� �ekin. SP�NRAZA seyreltilmemelidir. Harici filtrelerin kullan�m�na gerek yoktur.
6. FARMAS�T�K �ZELL�KLER
6.1. Yard�mc� maddelerin listesi
Sodyum dihidrojen fosfat dihidrat Disodyum fosfat
Sodyum klor�r Potasyum klor�r Kalsiyum klor�r dihidrat
Magnezyum klor�r hekzahidrat Sodyum hidroksit (pH ayarlamas� i�in) Hidroklorik asit (pH ayarlamas� i�in) Enjeksiyonluk su
6.2. Ge�imsizlikler
Ge�erli de�il.
6.3. Raf �mr�
36 ay
6.4. Saklamaya y�nelik �zel tedbirler
2°C - 8°C aras�nda buzdolab�nda saklay�n�z. Dondurmay�n�z.
Flakonlar� ���ktan korumak i�in kutusunda saklay�n�z.
E�er so�utucu mevcut de�ilse, SP�NRAZA kendi orijinal kutusunda, 30°C ve alt�ndaki s�cakl�klarda ���ktan korunarak 14 g�ne kadar saklanabilir.
Uygulama �ncesinde, a��lmam�� SP�NRAZA flakonlar� gerekirse buzdolab�ndan al�nabilir veya geri buzdolab�na konulabilir. E�er, orijinal ambalaj�ndan ��kar�ld�ysa, buzdolab�n�n d���nda kald��� toplam s�re 30 saati ge�memeli ve s�cakl�k 25°C'yi a�mamal�d�r.
6.5. Ambalaj�n niteli�i ve i�eri�i
Bromob�til kau�uk t�pal�, al�minyum �st contal� ve plastik kapakl� 5 ml'lik Tip I cam flakon. Her bir kutu 1 adet flakon i�ermektedir.
6.6. Be�eri t�bbi �r�nden arta kalan maddelerin imhas� ve di�er �zel �nlemler
Tek kullan�ml�kt�r.
Uygulamadan �nce t�bbi �r�n�n haz�rlanmas� i�in talimatlar
Uygulama �ncesinde SP�NRAZA flakonu partik�ller bak�m�ndan kontrol edilmelidir. E�er partik�l g�zlenirse ve/veya flakon i�indeki s�v� berrak ve renksiz de�ilse, flakon kullan�lmamal�d�r.
Enjekt�re �ekilen ��zelti 6 saat i�inde kullan�lmazsa at�lmal�d�r.
 Parkinson Hastal���
Hastal�k ilk kez 1817 de �ngiliz doktor James Parkinson taraf�ndan tan�mlanm�� ve Dr. Parkinson hastal��� “sallay�c� fel�” olarak kaleme alm��.
Parkinson Hastal���
Hastal�k ilk kez 1817 de �ngiliz doktor James Parkinson taraf�ndan tan�mlanm�� ve Dr. Parkinson hastal��� “sallay�c� fel�” olarak kaleme alm��. |
 �nme
�nme, beynin hasar g�rmesinin sonucudur. Bu hasar, beynin bir k�sm�ndaki ya bir kanama
ya da akut kan eksikli�i nedeniyle o k�sm�n ge�ici ya da kal�c� olarak i�levini yapamamas�na
yol a�ar.
�nme
�nme, beynin hasar g�rmesinin sonucudur. Bu hasar, beynin bir k�sm�ndaki ya bir kanama
ya da akut kan eksikli�i nedeniyle o k�sm�n ge�ici ya da kal�c� olarak i�levini yapamamas�na
yol a�ar. |
 |
Asperger Sendromu Asperger sendromu, otistik gurubun bir b�l�m� olan bir �z�rd�r. Bu genelde, gurubun daha ”y�ksek” taraf�nda yer ald��� d���n�len ki�ilere uygun bir tan�d�r. |
 |
Do�um Sonras� Depresyonu Do�um sonras� depresyonu, do�umdan sonra her on kad�ndan biri taraf�ndan tecr�be edilen stresli bir durumdur. |
 |
Belso�uklu�u, Chlamydia ve Frengi Belso�uklu�u, bakterilerin sebep oldu�u bir enfeksiyondur. Cinsel ili�ki yoluyla bula��r ve d�lyata�� boynunda, idrar yollar�nda, an�ste, makatta ve bo�azda enfeksyona sebep olabilir. |
�LA� GENEL B�LG�LER�
Gen �la� Ve Sa�l�k �r�nleri San. Ve Tic. Ltd. Sti.
| Sat�� Fiyat� | TL |
| �nceki Sat�� Fiyat� | |
| Original / Jenerik | Original �la� |
| Re�ete Durumu | K�rm�z� Re�eteli bir ila�d�r. |
| Barkodu | 8699783770389 |
| Etkin Madde | Nusinersen |
| ATC Kodu | M09AX07 |
| Birim Miktar | 12 |
| Birim Cinsi | MG |
| Ambalaj Miktar� | 1 |
| Kas �skelet Sistemi > Kas �skelet �la�lar� |
| �thal ( ref. �lke : Almanya ) ve Be�eri bir ila�d�r. |