SIMBRINZA 10 mg/ml + 2 mg/ml g�z damlas�. s�spansiyon (5 ml) K�sa �r�n Bilgisi
{ Brinzolamid + Brimonidin Tartarat }
1. BE�ER� TIBB� �R�N�N ADI
S�MBR�NZA 10 mg/ml + 2 mg/ml G�z Damlas�, S�spansiyon Steril
2. KAL�TAT�F VE KANT�TAT�F B�LE��M
Etkin madde
1 ml s�spansiyon;
Brinzolamid 10mg/ml
Brimonidin tartarat 2mg/ml (1.3 mg brimonidin e�de�eri)
Yard�mc� maddeler
Benzalkonyum klor�r 0,03mg/ml Yard�mc� maddelerin tam listesi i�in 6.1'e bak�n�z.
3. FARMAS�T�K FORMU
G�z damlas�, s�spansiyon.
Beyaz ila k�r�k beyaz homojen s�spansiyon, pH 6,5 (yakla��k).
4. KL�N�K �ZELL�KLER
4.1. Terap�tik endikasyonlar
A��k a��l� glokom veya g�z (ok�ler) hipertansiyonu olan, monoterapi ile yeterli g�z i�i bas�nc� d����� sa�lanamayan yeti�kin hastalarda, g�z i�i bas�nc�n� (G�B) d���rmek amac�yla kullan�lmaktad�r.
4.2. Pozoloji ve uygulama �ekli
Ya�l�lar dahil yeti�kinlerde ,
�nerilen doz etkilenmi� olan g�ze (g�zlere) g�nde iki kere bir damla S�MBR�NZA'd�r.
Atlanan doz,
Bir doz atlan�rsa tedavi sonraki dozla planland��� �ekilde s�rd�r�lmelidir.
Uygulama �ekli:
Ok�ler (G�z) kullan�m i�indir.
Kullanmadan �nce �i�e iyice �alkalanmal�d�r.
Nazolakrimal kapama i�in punktumlar t�kand���nda ve g�zkapaklar� 2 dakika kapat�ld���nda

sistemik emilim azal�r. Bu da sistemik yan etkilerde bir azalma ve lokal aktivitede bir art��la ssonu�lanabilir (bkz. B�l�m 4.4).
Damlal�k ucunun ve sol�syonun kirlenmesini �nlemek i�in, �i�enin damlal�k ucunun g�z kapaklar�na, g�z�n etraf�na ya da di�er b�lgelere de�dirilmemesine dikkat edilmelidir. Kullan�lmad��� zaman �i�e s�k�ca kapal� olarak saklanmal�d�r.
S�MBR�NZA g�z i�i bas�nc�n� (G�B) azaltmak amac�yla di�er topikal oftalmik t�bbi �r�nlerle e�zamanl� kullan�labilir. E�er birden fazla topikal oftalmik ila� kullan�l�yorsa, ila�lar�n uygulanmas� aras�nda en az 5 dakika s�re olmal�d�r.
�zel pop�lasyonlara ili�kin ek bilgiler :
Karaci�er/B�brek yetmezli�i:
S�MBR�NZA karaci�er yetmezli�i olan hastalar �zerinde �al���lmam��t�r ve dolay�s�yla bu pop�lasyonda dikkatli olunmas� �nerilir. (bak�n�z B�l�m 4.4).
S�MBR�NZA ciddi b�brek yetmezli�i (kreatinin klirensi < 30 ml/dak) ya da hiperkloremik asidozu olan hastalar �zerinde �al���lmam��t�r. S�MBR�NZA brinzolamid bile�eni ve metaboliti a��rl�kl� olarak b�breklerden at�ld��� i�in, S�MBR�NZA bu hastalarda kontrendikedir (bkz. B�l�m 4.3).
Pediyatrik pop�lasyon:
S�MBR�NZA'n�n g�venlili�i ve etkilili�i 2 ila 17 ya� hastalarda belirlenmemi�tir ve bu konuda herhangi bir veri bulunmamaktad�r.
S�MBR�NZA g�venlik endi�eleri nedeniyle monoterapinin yetersiz g�z i�i bas�nc� (G�B) azalmas� sa�lad��� a��k a��l� glokom veya ok�ler hipertansiyon g�r�len yeni do�anlarda ve 2 ya��ndan k���k bebeklerde artm�� �OB'nin azalt�lmas�nda kontrendikedir (bkz. B�l�m 4.3).
Geriyatrik pop�lasyon:
�nerilen doz etkilenmi� olan g�ze (g�zlere) g�nde iki kere bir damla S�MBR�NZA'd�r.
4.3. Kontrendikasyonlar
Etkin madde
4.4. �zel kullan�m uyar�lar� ve �nlemleri
Bu t�bbi �r�n enjekte edilmemelidir. Hastalar S�MBR�NZA'y� yutmamalar� konusunda bilgilendirilmelidir.
Ok�ler etkiler
S�MBR�NZA dar a��l� glokomlu hastalar �zerinde ara�t�r�lmam��t�r ve bu hastalarda kullan�m� tavsiye edilmez.
Brinzolamidin korneal endotelyal fonksiyon �zerindeki olas� etkisi, korneal bozuklu�u olan hastalarda ara�t�r�lmam��t�r (bilhassa d���k endotel h�cre say�l� hastalarda). �zellikle, kontakt lens kullanan hastalar �zerinde �al���lmam�� olup; karbonik anhidraz inhibit�rleri korneal hidrasyonu etkileyebilece�inden ve kontakt lens kullan�lmas� korneal riski art�rabilece�inden, brinzolamid kullan�m� �nerildi�inde, bu hastalar�n dikkatle g�zlenmesi tavsiye edilmektedir (kontakt lens kullan�m�na ili�kin daha fazla talimat i�in a�a��daki “Benzalkonyum klor�r” b�l�m�n� inceleyiniz). Ayn� �ekilde, diabetes mellitus'u veya korneal distrofileri olan hastalar gibi, korneal bozuklu�u olan hastalarda, dikkatli bir g�zlem tavsiye edilmektedir.
Brimonidin tartarat ok�ler alerjik reaksiyonlara yol a�abilir. E�er alerjik reaksiyonlar g�zlenirse, tedavi sonland�r�lmal�d�r. Brimonidin tartarat ile ilgili ge� ok�ler hipersensitivite reaksiyonlar� bildirilmi� olup baz� vakalarda bu durum G�B art��� ile ili�kilidir.
S�MBR�NZA ile yap�lan tedavinin kesilmesinden sonra potansiyel etkiler �al���lmam��t�r; S�MBR�NZA'n�n G�B d���r�c� etki s�resi �al���lmamakla birlikte, brinzolamidin G�B d���r�c� etkisinin 5 ila 7 g�n boyunca s�rmesi beklenir. Brimonidinin G�B-d���r�c� etkisi daha uzun olabilir.
Sistemik etkiler
S�MBR�NZA karbonik anhidraz inhibit�r� bir s�lfonamid olan brinzolamid i�erir ve topikal olarak uygulanmas�na ra�men sistemik yoldan emilir. S�lfonamidlere atfedilebilen Stevens- Johnson sendromu (SJS) ve toksik epidermal nekroliz (TEN) dahil olmak �zere ayn� tip advers ila� reaksiyonlar� topikal uygulama ile de g�r�lebilir. Re�eteleme s�ras�nda, hastalara belirtiler ve semptomlar hakk�nda bilgi verilmeli ve deri reaksiyonlar� a��s�ndan yak�ndan izlenmelidir. Ciddi reaksiyon belirtileri veya hipersensitivite ortaya ��karsa, ilac�n kullan�m� derhal kesilmelidir.
Kardiyak bozukluklar
S�MBR�NZA uygulamas�n� takiben, baz� hastalarda kan bas�nc�nda k���k miktarda azalmalar g�zlenmi�tir. Dolay�s�yla, S�MBR�NZA ile birlikte antihipertansif ve/veya kardiyak glikozitler gibi t�bbi �r�nler kullan�ld���nda veya a��r veya stabil olamayan ve kontrol edilemeyen kardiyovask�ler hastal��� olanlarda kullan�ld���nda dikkatli olunmal�d�r (bkz. B�l�m 4.5)
Depresyon, serebral veya koroner yetmezlik, Raynaud fenomeni, ortostatik hipotansiyon veya tromboanjiitis obliterans olan hastalarda S�MBR�NZA dikkatli kullan�lmal�d�r.
Asit/baz bozukluklar�
Oral karbonik anhidraz inhibit�rleri ile asit-baz bozukluklar� rapor edilmi�tir. S�MBR�NZA bir karbonik anhidraz inhibit�r� olan brinzolamid i�erir ve topikal olarak uygulanmas�na ra�men sistemik olarak emilir. Oral karbonik anhidraz inhibit�rlerine atfedilebilen ayn� tip advers reaksiyonlar (mesela asit baz bozukluklar�) topikal uygulama ile de g�r�lebilir. (bkz. B�l�m 4.5).
S�MBR�NZA, renal yetmezlik riski olan hastalarda metabolik asidoz riski nedeniyle dikkatli bir �ekilde kullan�lmal�d�r. S�MBR�NZA ciddi b�brek yetmezli�i olanlarda kontrendikedir (bkz. B�l�m 4.3).
Hepatik yetmezlik
![]()
S�MBR�NZA karaci�er yetmezli�i olan hastalar �zerinde �al���lmam��t�r ve bu hastalar tedavi
edilirken dikkatli olunmal�d�r (bkz. B�l�m 4.2).
Zihinsel uyan�kl�k
Oral karbonik anhidraz inhibit�rleri, ya�l� hastalarda zihinsel uyan�kl��� ve/veya fiziksel koordinasyon gerektiren i�leri yapabilme yetene�ini bozabilir. S�MBR�NZA sistemik olarak emilmektedir ve bu nedenle topikal uygulamayla bu durum olu�abilir. (bkz. B�l�m 4.7).
Pediyatrik pop�lasyon
2-17 ya� �ocuk ve ergenlerde S�MBR�NZA'n�n g�venlilik ve etkilili�i tespit edilmemi�tir. Brimonidin g�z damlas�n�n konjenital glokomun t�bbi tedavisinin bir par�as� olarak kullan�ld��� durumlarda, brimonidin alan yenido�anlar ve bebeklerde bilin� kayb�, hipotansiyon, hipotoni, bradikardi, hipotermi, siyanoz ve apne gibi doz a��m� semptomlar� bildirilmi�tir. Dolay�s�yla, S�MBR�NZA 2 ya� alt� �ocuklarda kontrendikedir (bkz. B�l�m 4.3).
Merkezi sinir sistemi ile ilgili yan etki potansiyelinden �t�r� 2 ya� ve �zerindeki �ocuklar (�zellikle 2-7 ya� grubu) ve/veya 20 kg veya alt�nda olan �ocuklar�n bu ila�la tedavi edilmesi �nerilmez. (bkz. B�l�m 4.9).
Benzalkonyum klor�r
S�MBR�NZA g�z iritasyonuna ve kontakt lensin renginin solmas�na neden olabilen benzalkonyum klor�r i�ermektedir. Yumu�ak kontakt lenslerle temas�ndan ka��n�lmal�d�r. Bu nedenle, kontakt lensler tak�l� halde iken S�MBR�NZA uygulanmamal�d�r ve hastalar lenslerini ��kard�ktan sonra S�MBR�NZA uygulamas�n�n ard�ndan kontakt lensi yeniden takmadan �nce 15 dakika beklenilmesi konusunda bilgilendirilmelidir.
Benzalkonyum klor�r�n g�z tahri�ine ve kuru g�z semptomlar�na neden oldu�u ve g�zya�� filmini ve kornea y�zeyini etkileyebilece�i bildirilmi�tir. Kuru g�z sorunu olan hastalarda ve korneas� kompromize olabilecek hastalarda dikkatle kullan�lmal�d�r. Hastalar uzun s�reli kullan�m durumunda takip edilmelidir.
4.5. Di�er t�bbi �r�nler ile etkile�imler ve di�er etkile�im �ekilleri
S�MBR�NZA'n�n di�er t�bbi ila�larla spesifik etkile�im �al��malar� yap�lmam��t�r.
Monoamin oksidaz inhibit�r tedavisi alan hastalar ve noradrenerjik iletimi etkileyen antidepresanlar� (�rn. trisiklik antidepresanlar ve mianserin) kullanan hastalarda S�MBR�NZA kontrendikedir (bkz. B�l�m 4.3). Trisiklik antidepresanlar S�MBR�NZA'n�n ok�ler hipotansif yan�t�n� azaltabilir.
MSS depresanlar� (alkol, barbit�ratlar, opiatlar, sedatifler veya anestezikler) ile birlikte kullan�ld���nda aditif veya g��lendirici etki olas�l��� g�z �n�ne al�narak dikkatli olunmas� �nerilir.
S�MBR�NZA uygulamas�ndan sonra dola��mdaki katekolaminlerin d�zeyi ile ilgili veri yoktur. Ancak, dola��mdaki aminlerin metabolizmas� ve al�m�n� etkileyebilecek t�bbi �r�nleri (klorpromazin, metilfenidat, rezerpin, serotonin-norepinefrin gerial�m inhibit�rleri) kullanan hastalarda dikkatli olunmas� tavsiye edilir.
Alfa adrenerjik agonistler (mesela brimonidin tartarat), bir s�n�f olarak, nab�z ve kan bas�nc�n� azaltabilir. S�MBR�NZA uyguland�ktan sonra baz� hastalarda kan bas�nc�nda k���k miktarda d����ler g�zlenmi�tir. S�MBR�NZA ile birlikte antihipertansifler ve/veya kardiyak glikozidler gibi ila�lar kullan�l�rken dikkatli olunmas� tavsiye edilir.

Alfa-adrenerjik agonistlerle etkile�ebilecek veya bunlar�n etkinliklerine engel olabilecek (izoprenalin ve prazosin gibi adrenerjik resept�r agonist veya antagonistler) sistemik bir ajanla (farmas�tik formdan ba��ms�z olarak) birlikte kullanmaya ba�land���nda dikkatli olunmas� tavsiye edilir.
Brinzolamid bir karbonik anhidraz inhibit�r�d�r ve topikal olarak uygulanmas�na ra�men sistemik olarak emilir. Oral karbonik anhidraz inhibit�rleri ile asit-baz bozukluklar� rapor edilmi�tir. S�MBR�NZA kullanan hastalarda etkile�im potansiyeline dikkat edilmelidir.
Oral karbonik anhidraz inhibit�r� ve topikal brinzolamid kullanan hastalarda karbonik anhidraz inhibisyonunun bilinen sistemik etkileri �zerine aditif etki potansiyeli mevcuttur. S�MBR�NZA ve oral karbonik anhidraz inhibit�rlerinin birlikte kullan�m� �nerilmemektedir.
CYP3A4 (ba�l�ca), CYP2A6, CYP2B6, CYP2C8 ve CYP2C9 dahil olmak �zere sitokrom P-
450 izoenzimleri brinzolamid metabolizmas�ndan sorumludur. Ketokonazol, itrakonazol, klotrimazol, ritonavir ve troleandomisin gibi CYP3A4 inhibit�rlerinin, brinzolamid metabolizmas�n� CYP3A4 ile inhibe etmeleri beklenir. CYP3A4 inhibit�rlerinin e� zamanl� verilmesi durumunda dikkat edilmesi �nerilmelidir. Ancak, renal eliminasyonun maj�r yol olmas�ndan dolay�, brinzolamid birikimi olas� de�ildir. Brinzolamid sitokrom P-450 izoenzimlerinin bir inhibit�r� de�ildir.
�zel pop�lasyonlara ili�kin ek bilgiler:
Pediyatrik pop�lasyon
Pediyatrik pop�lasyonlara ili�kin veri bulunmamaktad�r.
4.6. Gebelik ve laktasyon
Gebelik kategorisi : C
�ocuk do�urma potansiyeli bulunan kad�nlar/Do�um kontrol� ( Kontrasepsiyon ) Topikal ok�ler S�MBR�NZA uygulamas�n�n insan do�urganl��� �zerine herhangi bir etkisi bulundu�una dair veri yoktur.
S�MBR�NZA do�um kontrol� uygulamayan �ocuk do�urma potansiyeline sahip kad�nlarda �nerilmez. �ocuk do�urma potansiyeline sahip kad�nlar etkili bir do�um kontrol y�ntemi kullanmal�d�r.
Gebelik d�nemi
Hayvanlar �zerinde yap�lan �al��malar, gebelik /ve-veya/ embriyonal/fetal geli�im /ve- veya/ do�um /ve-veya/ do�um sonras� geli�im �zerindeki etkiler bak�m�ndan yetersizdir (bkz. B�l�m 5.3). �nsanlara y�nelik potansiyel risk bilinmemektedir. S�MBR�NZA hekimin zaruri g�rd��� �artlar haricinde gebelik d�neminde kullan�lmamal�d�r.
Laktasyon d�nemi
Topikal S�MBR�NZA'n�n insan s�t�ne ge�ip ge�medi�i bilinmemektedir. Mevcut farmakodinamik/toksikolojik hayvan verileri ile ortaya koyuldu�u �zere, oral uygulamay� takiben, minimal seviyede brinzolamid anne s�t�ne ge�mektedir. Brimonidin oral uyguland���nda anne s�t�ne ge�mektedir. S�MBR�NZA emzirme d�neminde kullan�lmamal�d�r.
�reme yetene�i/ Fertilite
Klinik d��� veriler brinzolamid veya brimonidinin fertilite �zerine herhangi bir etkisini g�stermemi�tir. Topikal ok�ler S�MBR�NZA uygulamas�n�n insan fertilitesi �zerine herhangi bir etkisi bulundu�una dair veri yoktur.
4.7. Ara� ve makine kullan�m� �zerindeki etkiler
S�MBR�NZA ara� ve makine kullanma becerisi �zerinde orta dereceli etkiye sahiptir.
S�MBR�NZA ara� veya makine kullan�m� becerisini etkileyecek �ekilde ba� d�nmesi, yorgunluk ve/veya sersemli�e neden olabilir.
Ge�ici bulan�k g�rme veya di�er g�rsel rahats�zl�klar ara� ya da makine kullan�m�n� etkileyebilir. Uygulamadan sonra g�rmede bulan�kl�k meydana gelmesi durumunda, ara� veya makine kullan�lmadan �nce g�rme bulan�kl��� d�zelinceye kadar beklenmelidir.
Oral karbonik anhidraz inhibit�rleri, ya�l� hastalarda zihinsel uyan�kl��� ve/veya fiziksel koordinasyon gerektiren i�leri yapabilme yetene�ini bozabilir. (bkz. B�l�m 4.4).
4.8. �stenmeyen etkiler
G�venlik profilinin �zeti
G�nde iki kez S�MBR�NZA dozu ile yap�lan klinik �al��malarda en s�k advers reaksiyonlar ok�ler hiperemi ve ok�ler alerjik reaksiyonlar olup hastalar�n yakla��k %6-7 kadar�nda g�zlenmi�tir ve disguzi (uygulama sonras� ac� veya al���lmam�� bir a��z tad�) hastalar�n yakla��k %3 kadar�nda g�zlenmi�tir.
Advers reaksiyonlar�n tablolu �zeti
A�a��daki advers reaksiyonlar klinik �al��malarda g�nde iki kere S�MBR�NZA dozuyla ve ayr�ca her bir bile�enin (brinzolamid ve brimonidin) ayr� ayr� uyguland��� klinik �al��malar ve pazarlama sonras� s�rveyans �al��malar�nda bildirilmi�tir. A�a��daki s�rayla s�n�fland�r�lm��lard�r: �ok yayg�n (≥ 1/10), yayg�n (≥ 1/100 - <1/10), yayg�n olmayan (≥1/1.000 - <1/100), seyrek (≥1/10.000
- <1/1.000), �ok seyrek (<1/10.000) veya bilinmiyor (eldeki verilerle hesaplanam�yor). Her s�kl�k grubunda, advers reaksiyonlar azalan �iddet s�ras�yla sunulmu�tur.
Sistem Organ S�n�f� | Advers reaksiyonlar |
Enfeksiyonlar ve enfestasyon hastal�klar� | Yayg�n olmayan: nazofarenjit, farenjit, sin�zit Bilinmiyor: rinit |
Kan ve lenf sistemi hastal�klar� | Yayg�n olmayan: k�rm�z� kan h�crelerinde azalma, kan klor�r seviyesi art��� |
Ba����kl�k sistemi hastal�klar� | Yayg�n olmayan: hipersensitivite |
Psikiyatri hastal�klar� | Yayg�n olmayan: apati, depresyon, depresif ruh hali, insomnia, libido azalmas�, kabus, sinirlilik |
Sinir sistemi hastal�klar� | Yayg�n: somnolans, ba� d�nmesi, disguzi Yayg�n olmayan: ba� a�r�s�, motor disfonksiyon, amnezi, bellek bozuklu�u, parestezi �ok seyrek: senkop Bilinmiyor: tremor, hipoestezi, aguzi |
G�z hastal�klar� | Yayg�n: g�z alerjisi, keratit, g�z a�r�s�, ok�ler rahats�zl�k, bulan�k g�rme, anormal g�rme, ok�ler hiperemi, konjonktivada solukla�ma Yayg�n olmayan: korneal erozyon, korneal �dem, blefarit, korneal depozitler (keratik presipitat), konjonktival bozukluk (papillalar), fotofobia, fotopsi, g�zde �i�me, g�z kapa��nda �dem, konjonktival �dem, g�zde kuruluk, g�zde ak�nt�, g�rme keskinli�inde azalma, lakrimasyon art���, ptergium, g�z kapa��nda eritem, meibomianitis, diplopia, parlama, g�zde hipoestezi, skleral pigmentasyon, subkonjonktival kist, g�zde anormal his, astenopia �ok seyrek: uveitis, miyozis Bilinmiyor: g�rme bozukluklar�, madarosis |
Kulak ve i� kulak hastal�klar� | Yayg�n olmayan: vertigo, tinitus |
Kardiyak sistem hastal�klar� | Yayg�n olmayan: kardiyo-respiratuvar distress, anjina pektoris, aritmi, �arp�nt�, d�zensiz kalp h�z�, bradikardi, ta�ikardi |
Vask�ler sistem hastal�klar� | Yayg�n olmayan: hipotansiyon �ok seyrek: hipertansiyon |
Solunum, g���s ve mediastinal sistem hastal�klar� | Yayg�n olmayan: dispne, bron�iyal hiperaktivite, faringolaringeal a�r�, bo�azda kuruluk, �ks�r�k, epistaksis, �st solunum yolunda konjesyon, nazal konjesyon, rinore, bo�azda tahri�, burunda kuruluk, postnazal ak�nt�, hap��rma Bilinmiyor: ast�m |
Gastrointestinal sistem hastal�klar� | Yayg�n: a��z kurulu�u Yayg�n olmayan: dispepsi, �zofajit, abdominal rahats�zl�k, ishal, kusma, bulant�, ba��rsak hareketlerinde art��, flatulans, oral hipoestezi, oral parestezi |
Hepato-bilier sistem hastal�klar� | Bilinmiyor: anormal karaci�er fonksiyon testleri |
Deri ve derialt� doku hastal�klar� | Yayg�n olmayan: kontakt dermatit, �rtiker, d�k�nt�, mak�lopap�ler d�k�nt�, genel ka��nt� , alopesi, deride sertle�me Bilinmiyor: Stevens-Johnson sendromu (SJS)/toksik epidermal nekroliz (TEN) (bkz. b�l�m 4.4), y�zde �dem, dermatit, eritem |
Kas-iskelet, ba� doku ve kemik hastal�klar� | Yayg�n olmayan: s�rt a�r�s�, kas spazmlar�, kas a�r�s� Bilinmiyor: artalji, ekstremitelerde a�r� |
B�brek ve �riner sistem hastal�klar� | Yayg�n olmayan: renal a�r� Bilinmiyor: pollak�ri |
�reme sistemi ve meme hastal�klar� | Yayg�n olmayan: erektil disfonksiyon |
Genel hastal�klar ve uygulama b�lgesine ili�kin rahats�zl�klar | Yayg�n olmayan: a�r�, g���ste rahats�zl�k gergin hissetme, sinirlilik, , ila� kal�nt�s� Bilinmiyor: g���s a�r�s�, periferik �dem |
Se�ilmi� advers reaksiyonlar�n tan�m�
![]()
Disguzi, S�MBR�NZA kullan�m� ile ili�kilendirilen, en yayg�n ortaya ��kan sistemik advers reaksiyondur (%3.,4). G�z damlas�n�n nazolakrimal kanal yoluyla nazofarenksten ge�mesiyle olu�mas� muhtemeldir ve b�y�k �l��de S�MBR�NZA'n�n brinzolamid bile�eninden kaynaklan�r. Nazolakrimal t�kama veya ila� damlat�ld�ktan sonra g�z kapa��n�n hafif�e kapat�lmas� bu etkinin geli�imini azaltmaya yard�mc� olabilir (bak�n�z B�l�m 4.2).
S�MBR�NZA karbonik anhidraz�n bir s�lfonamid inhibit�r� olan ve sistemik olarak emilen brinzolamid i�erir. Gastrointestinal, sinir sistemi, hematolojik, renal ve metabolik etkiler genellikle sistemik karbonik anhidraz inhibit�rleri ile ili�kilendirilir. Oral karbonik anhidraz inhibit�rlerine atfedilen ayn� tipteki advers reaksiyonlar topikal uygulama ile ortaya ��kabilir.
Genellikle S�MBR�NZA'n�n brimonidin bile�eninden kaynaklanan advers reaksiyonlar ok�ler alerjik tip reaksiyonlar, halsizlik ve/veya sersemlik ve a��z kurulu�udur. Brimonidin kullan�m� kan bas�nc�nda minimal azalmaya yol a�abilir. S�MBR�NZA dozu uygulanan baz� hastalarda, brimonidin monoterapisinde g�zlenene benzer kan bas�nc�nda azalma ortaya ��kabilir.
��pheli advers reaksiyonlar�n bildirilmesi
Bu t�bbi �r�ne ait ��pheli advers reaksiyonlar�n�n bildirilmesi b�y�k �nem ta��maktad�r. Bildirim yap�lmas�, t�bbi �r�n�n yarar/risk dengesinin s�rekli olarak izlenmesine olanak sa�lar. Sa�l�k mesle�i mensuplar�n�n herhangi bir ��pheli advers reaksiyonu EK V'deki ulusal bildirim sistemiyle bildirmeleri gerekmektedir.
4.9. Doz a��m� ve tedavisi
E�er S�MBR�NZA ile doz a��m� olu�ursa, tedavi, semptomatik ve destekleyici olmal�d�r. Hastan�n hava yollar� a��k tutulmal�d�r.
S�MBR�NZA'n�n brinzolamid bile�enine ba�l�, elektrolit dengesizli�i, asidoz geli�mesi ve olas� santral sinir sistemi etkileri g�r�lebilir. Serum elektrolit seviyeleri (�zellikle potasyum) ve kan pH de�erleri takip edilmelidir.
Yeti�kinlerde S�MBR�NZA brimonidin bile�eninin kazara yutulmas�yla ilgili �ok s�n�rl� veri mevcuttur. G�n�m�ze kadar raporlanan tek advers reaksiyon hipotansiyondur. Hipotansiyon epizodunu takiben rebound hipertansiyon rapor edilmi�tir.
Di�er alfa2-agonistlerin oral doz a��m�nda hipotansiyon, asteni, kusma, letarji, sedasyon, bradikardi, aritmi, miyozis, apne, hipotoni, hipotermi, solunum depresyonu ve n�betler gibi semptomlar bildirilmi�tir.
Pediyatrik pop�lasyon
S�MBR�NZA'n�n brimonidin bile�eninin �ocuklar taraf�ndan kazara al�nmas�n� takiben ortaya ��kan ciddi advers reaksiyonlar bildirilmi�tir. Bu olgularda, CNS depresyonu semptomlar�, tipik
ge�ici koma veya d���k bilin� d�zeyi, letarji, somnolans, hipotoni, bradikardi, hipotermi, solukluk, solunum depresyonu ve apne ortaya ��km��t�r ve yo�un bak�m �nitesine yat�� gerekli olmu�tur (endike oldu�unda ent�basyonla birlikte). B�t�n olgular�n genellikle 6- 24 saat i�inde tam olarak iyile�ti�i bildirilmi�tir.
5. FARMAKOLOJ�K �ZELL�KLER
5.1. Farmakodinamik �zellikler
Farmakoterap�tik grup: Duyu organlar�, Oftalmolojik, Antiglokom ila�lar ve miyotikler, karbonik anhidraz intibit�rleri, brinzolamid, kombinasyonlar�
ATC kodu: S01EC54
Etki mekanizmas�
S�MBR�NZA iki etkin madde i�ermektedir: brinzolamid ve brimonidin tartarat. Bu iki bile�en g�zde siliyer s�re�lerde h�mor ak�z olu�umunu bask�layarak a��k a��l� glokom (OAG) ve ok�ler hipertansiyon (OHT) hastalar�nda g�z i�i bas�nc�n� (G�B) d���r�rler. Bu iki bile�en (brinzolamid ve brimonidin) h�mor ak�z sekresyonunu azaltarak y�kselmi� G�B'i d���rmekle birlikte de�i�ik mekanizmalar arac�l���yla bu etkiyi g�sterirler.
Brinzolamid, siliyer epitelde karbonik anhidraz enzimini (CA-II) inhibe ederek etki g�stermekte, b�ylelikle bikarbonat iyonlar�n�n yap�m�n�n azalmas�yla beraber siliyer epitelden sodyum ve s�v� ge�i�i ve sonu� olarak h�mor ak�z olu�umu azalmaktad�r. Alfa 2 adrenerjik agonisti olan brimonidin, adenilat siklaz enzimini inhibe ederek, h�mor ak�z�n cAMP ba��ml� olu�umunu bask�lar. Ayr�ca, brimonidin uygulamas� uveoskleral ak��� art�r�r.
Farmakodinamik etkiler Klinik etkililik ve g�venlik Monoterapi
6-ayl�k, kontroll�, bile�enlerin katk�s� klinik �al��mas�nda a��k a��l� glokomu (ps�doeksfolyasyon veya pigment dispersiyon bile�eni dahil) ve/veya ok�ler hipertansiyonu olan 560 hasta, ara�t�rmac�n�n karar�na g�re, monoterapiyle yeterince kontrol alt�na al�nmad���nda veya halihaz�rda G�B d���r�c� birden fazla ila� kullan�yorsa, ortalama ba�lang�� diurnal G�B 26 mmHg iken, S�MBR�NZA'n�n ortalama diurnal G�B d���r�c� etkisi yakla��k 8 mmHg idi. �al��ma boyunca t�m vizitlerde, g�nde iki kez brinzolamid 10 mg/ml veya brimonidin 2 mg/ml ile kar��la�t�r�ld���nda, S�MBR�NZA ile g�zlenen ortalama diurnal G�B azalmalar� istatistiksel olarak daha fazlayd� (�ekil 1).
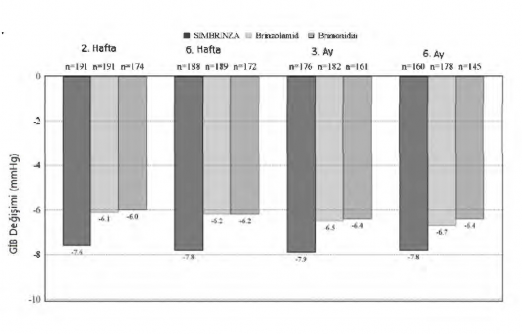
�ekil 1. Ba�lang��tan itibaren ortalama diurnal (Sabah saat 9, +2 saat, +7 saat) G�B de�i�imi (mmHg)-Bile�enlerin katk�s� �al��mas�
T�m tedavi farkl�l�klar� (S�MBR�NZA ile her bir bile�enin kar��la�t�rmas�nda) istatistiksel olarak anlaml� derecedeydi: p=0,0001 veya daha az.
Ortalama G�B azalmalar� ba�lang�ca k�yasla her vizitte her zaman noktas�nda brinzolamid (5 - 7 mmHg) veya brimonidin (4 - 7 mmHg) monoterapilerine k�yasla S�MBR�NZA (6 - 9 mmHg) ile daha fazlayd�. Ba�lang�ca k�yasla ortalama % G�B azalmalar� S�MBR�NZA ile % 23 – 34 aras�ndayd�. G�B �l��mleri 18 mmHg alt�nda olan hasta y�zdeleri 6. aydan itibaren 12 �l��m�n 11 tanesinde Brinzolamid grubuna k�yasla S�MBR�NZA grubunda daha y�ksekti ve 6. aydan itibaren 12 �l��m�n 12 tanesinde Brimonidin grubuna k�yasla S�MBR�NZA grubunda daha y�ksekti. + 2 saat zaman noktas�nda (sabah etkinlik pikine kar��l�k gelen zaman) birincil etkinlik vizit i�in 3.ayda, G�B �l��mleri 18 mmHg alt�nda olan hasta y�zdeleri S�MBR�NZA grubunda
%68,8, Brinzolamid grubunda %42,3 ve Brimonidin grubunda %44 idi.
6-ayl�k, kontroll�, non-inferiyorite klinik �al��mas�nda, a��k a��l� glokomu (ps�doeksfolyasyon veya pigment dispersiyon bile�eni dahil) ve/veya ok�ler hipertansiyonu olan 890 hasta, ara�t�rmac�n�n karar�na g�re, monoterapiyle yeterince kontrol alt�na al�namad���nda veya halihaz�rda G�B d���r�c� birden fazla ila� kullan�yorsa, ortalama ba�lang�� diurnal G�B 26 -27 mmHg iken, ba�lang�ca g�re ortalama diurnal G�B azalmas� a��s�ndan S�MBR�NZA'n�n brinzolamid 10 mg/mL + brimonidin 2 mg/mL e�zamanl� uygulamas�na non-inferiyoritesi �al��ma boyunca t�m vizitlerde g�sterilmi�tir. (Tablo 1).
Tablo 1. Ba�lang��tan itibaren ortalama diurnal G�B (mmHg) de�i�imlerin kar��la�t�rmas�– Non-inferiyorite �al��mas�
Vizit | S�MBR�NZA Ortalama | Brinzolamid + Brimonidine Ortalama | Fark Ortalama (%95 CI) |
2. Hafta | -8,4 (n=394) | -8,4 (n=384) | -0 (-0,4, 0,3) |
6. hafta | -8,5 (n=384) | -8,4 (n=377) | -0.1 (-0,4, 0,2) |
3. Ay | -8,5 (n=384) | -8,3 (n=373) | -0.1 (-0,5, 0,2) |
6. Ay | -8,1 (n=346) | -8,2 (n=330) | 0.1 (-0,3, 0,4) |
Ortalama G�B azalmalar� ba�lang�ca k�yasla her vizitte her zaman noktas�nda S�MBR�NZA ve ayn� anda uygulanan iki bile�en ile birbirine benzerdi (7 - 10 mmHg). Ba�lang�ca k�yasla ortalama y�zde G�B azalmalar� S�MBR�NZA ile %25 – 37 aras�ndayd�. G�B �l��mleri 18 mmHg alt�nda olan hasta y�zdeleri 6. aydan itibaren t�m �al��ma vizitlerinde ayn� zaman noktas� i�in S�MBR�NZA ve Brinzolamid + Brimonidin gruplar�nda benzerdi. + 2 saat zaman noktas�nda (sabah etkinlik pikine kar��l�k gelen zaman�) birincil etkinlik vizit i�in 3.ayda, G�B �l��mleri 18 mmHg alt�nda olan hasta y�zdesi her iki grup i�in %71,6 olmu�tur.
Ek tedavi
Prostaglandin analoglar�na (PGA) ek olarak S�MBR�NZA kullan�m� ile ilgili klinik veriler, tek ba��na PGA ile kar��la�t�r�ld���nda S�MBR�NZA + PGA'n�n �st�n G�B d���r�c� etkinli�ini de g�stermi�tir. CQVJ499A2401 �al��mas�nda S�MBR�NZA + PGA (yani travoprost, latanoprost veya bimatoprost), 6 haftal�k tedaviden sonra, ta��y�c� + PGA ile kar��la�t�r�ld���nda, tedavi ba�lang�c�ndaki de�erden �st�n G�B d���r�c� etkinlik g�stermi�, diurnal G�B'de tedavi ba�lang�c�na g�re modele uyarlanm�� ortalama de�i�iklik bak�m�ndan tedaviler aras� fark -3,44 mmHg olmu�tur (%95 GA, 4,2, 2,7; p de�eri <0,001).
Travoprost-timolol maleat sabit doz kombinasyonlu g�z damlas�, ��zeltiye ek S�MBR�NZA kullan�m� ile ilgili klinik veriler, tek ba��na travoprost-timolol maleat ile kar��la�t�r�ld���nda, S�MBR�NZA + travoprost-timolol maleat g�z damlalar�n�n �st�n G�B d���r�c� etkinli�i de ortaya koymu�tur. CQVJ499A2402 �al��mas�nda, S�MBR�NZA + travoprost-timolol maleat g�z damlalar�, 6 haftal�k tedaviden sonra, ta��y�c� + travoprost-timolol maleat g�z damlalar� ile kar��la�t�r�ld���nda, tedavi ba�lang�c�ndaki de�erden �st�n G�B d���r�c� etkinlik g�stermi�, diurnal G�B'de tedavi ba�lang�c�na g�re modele uyarlanm�� ortalama de�i�iklik bak�m�ndan tedaviler aras� fark -2,15 mmHg bulunmu�tur (%95 GA, 2,8, 1,5; p-de�eri <0,001).
Ek tedavide S�MBR�NZA'n�n g�venlik profili, S�MBR�NZA monoterapisinde g�zlenene benzer olmu�tur.
Ek tedavi i�in 6 haftan�n �tesinde etkililik ve g�venlilik verisi bulunmamaktad�r.
Pediyatrik pop�lasyon
Avrupa �la� Ajans�, pediyatrik pop�lasyonun t�m alt k�melerinde S�MBR�NZA ile glokom ve ok�ler hipertansiyon tedavisi �al��malar�n�n bulgular�n�n sunulmas� zorunlu�undan feragat etmi�tir. (bkz. B�l�m 4.2 pediyatrik kullan�m ile ilgili bilgiler).
5.2. Farmakokinetik �zellikler
Genel �zellikler:
Emilim:
Brinzolamid topikal ok�ler uygulamay� takiben korneadan emilir. Madde sistemik dola��ma ge�erek k�rm�z� kan h�crelerinde (KKH) g��l� bir �ekilde karbonik anhidraza ba�lan�r. Plazma konsantrasyonlar� �ok d���kt�r. Tam kan eliminasyon yar� �mr�, KKH karbonik anhidraz ba�lanmas�ndan �t�r� insanlarda uzundur (>100 g�n).
�nsanda g�ze topikal uygulamay� takiben, brimonidin h�zla emilir. Tav�anlarda maksimum ok�ler konsantrasyonlara �o�u vakada bir saatten daha az s�rede eri�ilir. Maksimum insan plazma konsantrasyonlar� < 1 ng/mL olarak bulunmu�tur ve < 1 saatte bu seviyeye eri�ilir. Plazma seviyeleri yakla��k 2-3 saatlik yar� �m�rle azal�r. Kronik uygulama s�ras�nda birikimi olmaz.
G�nde iki veya �� kez S�MBR�NZA uygulamas�n�n sistemik farmakokineti�ini ayn� pozolojiyle uygulanan brinzolamid ve brimonidin monoterapileriyle kar��la�t�ran topikal ok�ler klinik �al��mada, kararl� durum tam kan brinzolamid ve N-desetilbrinzolamid farmakokinetikleri kombinasyon �r�n� ve brinzolamid monoterapisi i�in benzerdi. Ayn� �ekilde, kombinasyondaki brimonidinin kararl� durum plazma farmakokineti�i, g�nde iki kez S�MBR�NZA grubu d���nda brimonidin monoterapisine benzerdi. G�nde iki kez SIMBRINZA grubunda ise ortalama EAA, g�nde iki kez brimonidin monoterapisine k�yasla yakla��k
% 25 daha d���kt�.
Da��l�m:
Tav�an �al��malar�na g�re topikal uygulaman�n ard�ndan maksimum brinzolamid ok�ler konsantrasyonlar� kornea, konjonktiva, h�mor ak�z ve iris-siliyer cisim gibi �n dokulardad�r. Ok�ler dokulardaki birikim karbonik anhidraz ba�lamas� nedeniyle uzundur. Brinzolamidin insan plazma proteinlerine ba�lanmas� orta derecelidir (yakla��k %60).
Brimonidin bilinen melanin ba�lama �zelliklerinden �t�r� pigmentli ok�ler dokular, �zellikle iris-siliyer cisim i�in affinite g�sterir. Bununla birlikte, klinik ve klinik d��� g�venlik verileri kronik uygulamada iyi tolere edildi�ini ve g�venilir oldu�unu g�stermektedir.
Biyotransformasyon:
Brinzolamid hepatik sitokrom P450 izoenzimleriyle �zellikle CYP3A4, CYP2A6, CYP2B6, CYP2C8 ve CYP2C9 ile metabolize olmaktad�r. Ana metaboliti N-desetilbrinzolamiddir ve bunu N-desmetoksipropil ve O-desmetil metabolitlerinin yan� s�ra O-desmetil brinzolamidin N- propil yan zincirinin oksidasyonuyla olu�an N-propiyonik asit analo�u takip eder. Brinzolamid ve N-desetilbrinzolamid maksimum sistemik seviyelerinin en az 100 misli konsantrasyonlara dek sitokrom P450 izoenzimlerini inhibe etmezler.
Brimonidin hepatik aldehit oksidazla kapsaml� bir bi�imde metabolize edilir ve maj�r metabolitler 2-oksobrimonidin, 3-oksobrimonidin ve 2,3-dioksiobrimonidin olu�ur. �midazolin halkas�n�n 5-bromo-6-guanidinoquinoksaline oksidatif ayr�lmas� g�zlenmi�tir.
Eliminasyon :
Brinzolamid esas olarak idrarla de�i�meden at�l�r. �nsanlarda, �riner brinzolamid ve N- desetilbrinzolamid s�ras�yla dozun %60 ve %6's�ndan sorumludur. S��an verileri biraz biliyer at�l�m g�stermektedir (%30 kadar, �ncelikle metabolitler olarak).
Brimonidin esas olarak idrarla metabolitler olarak at�l�r. S��anlarda ve maymunlarda �riner
metabolitler oral veya intraven�z dozlar�n %60-75 kadar�ndan sorumludur.
Do�rusall�k/Do�rusal Olmayan Durum
Brinzolamid farmakokineti�i tam kanda ve �e�itli dokularda karbonik anhidraza doygun �ekilde ba�land���ndan do�as� gere�i do�rusal de�ildir. Kararl� durum maruziyeti dozla orant�l� �ekilde artmamaktad�r.
Tam aksine, brimonidin klinik terap�tik doz aral���nda do�rusal farmakokinetik sergilemektedir.
Farmakokinetik/farmakodinamik ili�kiler
S�MBR�NZA g�zde lokal etki yaratmak i�in kullan�lmaktad�r. Etkili dozlarda insan ok�ler maruziyetinin de�erlendirilmesi olas� de�ildir. G�B d���rme a��s�ndan insanlarda farmakokinetik/farmakodinamik ili�kisi saptanmam��t�r.
Di�er �zel pop�lasyonlar
![]()
![]()
S�MBR�NZA ile ya�, �rk, renal ve hepatik yetmezli�in etkilerini belirlemeye y�nelik �al��malar yap�lmam��t�r. Japonlarla Japon olmayanlar� kar��la�t�ran bir brinzolamid �al��mas� her iki grupta benzer sistemik farmakokinetik g�stermi�tir. Renal yetmezli�i olan g�n�ll�lerde yap�lan brinzolamid �al��mas�na g�re, normal ve orta derecede b�brek bozuklu�u olan g�n�ll�lerde brinzolamid ve N-desetilbrinzolamid sistemik maruziyetinde 1.,6- ila 2.,8 kat art�� olmu�tur.
Maddeyle alakal� materyalin kararl� durum RBC konsantrasyonlar�ndaki bu art�� RBC karbonik anhidraz aktivitesini sistemik yan etkilere yol a�an seviyelere dek inhibe etmemi�tir. Bununla birlikte, ciddi b�brek yetmezli�i (kreatinin klirensi <30 mL/dakika) olanlara kombinasyon �r�n� �nerilmemektedir.
Brimonidinin C, AUC ve eliminasyon yar� �mr� 65 ya� �zerindeki ki�ilerde ve gen� yeti�kinlerde benzerdir. Renal ve hepatik yetmezli�in brimonidinin sistemik farmakokineti�i �zerindeki etkileri incelenmemi�tir. Topikal ok�ler uygulamay� takiben brimonidinin sistemik maruziyeti d���k oldu�undan, plazma maruziyetindeki de�i�ikliklerin klinik �neminin olmas� beklenmemektedir.
Pediyatrik Pop�lasyon:
Pediyatrik hastalarda brinzolamid ve brimonidinin tek ba��na veya kombinasyon halinde sistemik farmakokineti�i �al���lmam��t�r.
5.3. Klinik �ncesi g�venlilik verileri
Brinzolamid
Geleneksel g�venlilik farmakolojisi, tek doz toksisite, tekrarl� doz toksisite, karsinojenik potansiyel ve genotoksisite �al��malar�ndan elde edilen klinik d��� verilere g�re brinzolamid, insanlar i�in �zel bir tehlike olu�turmaz.
Klinik d��� �reme ve geli�im toksisitesi �al��malar�ndaki etkiler sadece maksimum insan maruziyetini a�an dozdaki maruziyetlerde g�zlenmi�tir, dolay�s�yla bunlar�n klinik kullan�mda �nemi �ok azd�r. Tav�anlarda, oral, maternal toksik 6 mg/kg/g�n brinzolamid dozlar� (�nerilen g�nl�k klinik doz 23 mcg/kg/g�n�n 261 misli) fetal geli�im �zerinde etkiye yol a�mam��t�r. S��anlarda 18 mg/kg/g�n dozlar (�nerilen g�nl�k klinik dozun 783 misli) fet�slerde kafatas� ve sternebra ossifikasyonlar�n� biraz azaltm��t�r ama 6 mg/kg/g�n ile b�yle bir etki g�zlenmemi�tir. Bu bulgular metabolik asidoz ile ili�kilidir, annelerde kilo al�m� ve fetal a��rl�k azalm��t�r. Fetal a��rl�kta dozla ili�kili azalmalar 2 - 18 mg/kg/g�n verilen annelerin yavrular�nda g�zlenmi�tir. Emzirme s�ras�nda, yavrulardaki herhangi bir advers etkinin g�zlenmedi�i seviye 5 mg/kg/g�nd�r.
Brimonidin
Geleneksel g�venlilik farmakolojisi, tekrarl� doz toksisitesi, karsinojenik potansiyel ve �reme ve geli�im toksisitesi �al��malar�ndan elde edilen klinik d��� verilere g�re brimonidin, insanlar i�in �zel bir tehlike olu�turmaz.
6. FARMAS�T�K �ZELL�KLER
6.1. Yard�mc� maddelerin listesi
Benzalkonyum klor�r Propilen glikol Karbomer 974P Borik asit
Mannitol Sodyum klor�r Tiloksapol
Hidroklorik asit ve/veya sodyum hidroksit (pH ayar� i�in) Saf su
6.2. Ge�imsizlikler
Yeterli veri yoktur.
6.3. Raf �mr�
24 ay.
�lk a��lmas�ndan sonra 4 hafta.
6.4. Saklamaya y�nelik �zel tedbirler
25 C alt�ndaki oda s�cakl���nda saklanmal�d�r.
A��ld�ktan sonra 25 ºC' nin alt�nda tutularak 4 hafta i�inde kullan�lmal�d�r.
6.5. Ambalaj�n niteli�i ve i�eri�i
LDPE damlal�k ucu ve beyaz polipropilen vidal� kapak ile 8 mL yuvarlak opak d���k yo�unluklu polietilen (LDPE) �i�e i�inde 5 mL s�spansiyon.
6.6. Be�eri t�bbi �r�nden arta kalan maddelerin imhas� ve di�er �zel �nlemler
Kullan�lmam�� olan �r�nler ya da at�k materyaller “T�bbi �r�nlerin Kontrol� Y�netmeli�i” ve “Ambalaj At�klar�n�n Kontrol� Y�netmeli�i”ne uygun olarak imha edilmelidir.
 Grip, So�uk Alg�nl��� ve �ks�r�k
Grip ve so�uk alg�nl��� (nezle) semptomlar� aras�ndaki fark� bilmek �nemlidir. So�uk alg�nl��� gripten daha hafif belirtiler g�steren bir solunum yolu hastal���d�r.
Grip, So�uk Alg�nl��� ve �ks�r�k
Grip ve so�uk alg�nl��� (nezle) semptomlar� aras�ndaki fark� bilmek �nemlidir. So�uk alg�nl��� gripten daha hafif belirtiler g�steren bir solunum yolu hastal���d�r. |
 Tiroid Kanseri
En s�k g�r�len tiroid kanseri t�r� olan papiller tiroid kanseri, t�m tiroid kanserlerinin yakla��k %70'ini olu�turur.
Tiroid Kanseri
En s�k g�r�len tiroid kanseri t�r� olan papiller tiroid kanseri, t�m tiroid kanserlerinin yakla��k %70'ini olu�turur. |
 |
Diyabet Hastal��� Diyabet, ins�lin hormonu ile ilgili problemlerden kaynaklanan bir hastal�kt�r. |
 |
D�� Gebelik D�� gebelik, her 100 gebelikten birini etkileyen, s�k g�r�len ve �l�me sebep olabilecek bir durumdur. Bu, d�llenen yumurta, rahimin d���na yerle�irse, olu�an bir durumdur. Gebelik ilerledik�e, a�r�ya ve kanamalara sebep olur. |
 |
Ruh ve Ak�l Sa�l���m�z� Geli�tirmek �yi ak�l ve ruh sa�l��� sahip olmaktan ziyade, yapt���n�z �eylerdir. Ak�l ve ruhsal olarak sa�l�kl� olmak i�in kendinize de�er vermeli ve kendinizi kabul etmelisiniz. |
�LA� GENEL B�LG�LER�
Novartis Sa�l�k,G�da ve Tar�m �r�nleri San. Tic. A.�.
| Sat�� Fiyat� | 305.16 TL [ 4 May 2026 ] |
| �nceki Sat�� Fiyat� | 305.16 TL [ 27 Apr 2026 ] |
| Original / Jenerik | Original �la� |
| Re�ete Durumu | Normal Re�eteli bir ila�d�r. |
| Barkodu | 8699504710175 |
| Etkin Madde | Brinzolamid + Brimonidin Tartarat |
| ATC Kodu | S01EC54 |
| Birim Miktar | 10+2 |
| Birim Cinsi | ML |
| Ambalaj Miktar� | 5 |
| Duyu Organlar� > G�z Tansiyonu �la�lar� (Glokom) ve Miyotikler |
| �thal ( ref. �lke : Yunanistan ) ve Be�eri bir ila�d�r. |