NOVOMIX 50 FLEXPEN 100 IU / ml 3 ml kull. haz�r dolu enj. kalemI i�inde s�spansiyon.5 FLEXPEN K�sa �r�n Bilgisi
{ Insulin Aspart }
1. BE�ER� TIBB� �R�N�N ADI
NovoMix50 FlexPen100 U/mL enjeksiyonluk s�spansiyon i�eren kullan�ma haz�r kalem Steril
2. KAL�TAT�F VE KANT�TAT�F B�LE��M
Etkin madde
��z�n�r ins�lin aspart*/protamin-kristalize ins�lin aspart* (50/50 oran�nda, 100 �nite/mL)
*Saccharomyces cerevisiae'den rekombinant DNA teknolojisi ile �retilmi� bir proteindir. 1 �nite ins�lin aspart 6 nmol, 0.035 mg tuzsuz anhidr ins�lin asparta e�de�erdir.
1 kullan�ma haz�r kalem 300 �niteye e�de�er 3 mL s�spansiyon i�erir.
Yard�mc� maddeler
Sodyum klor�r 1.17 mg/mL
Disodyum fosfat dihidrat… 1.25 mg/mL
Sodyum hidroksit (pH ayar� i�in) 1.9 mg/mL
Yard�mc� maddeler i�in 6.1'e bak�n�z.
3. FARMAS�T�K FORMU
Enjeksiyon i�in s�spansiyon.
NovoMix50 FlexPenbulan�k, beyaz renkli, sulu bir s�spansiyondur.
4. KL�N�K �ZELL�KLER
4.1. Terap�tik endikasyonlar
Eri�kinlerde diyabetes mellitus hastal���n�n tedavisinde endikedir.
4.2. Pozoloji ve uygulama �ekli
�nsan ins�lini internasyonal �nite olarak ifade edilirken, ins�lin aspart dahil, ins�lin analoglar�n�n etkinli�i �nite olarak ifade edilir.
NovoMix50 FlexPen'in dozu bireylere �zg�d�r ve hastan�n ihtiyac�na ba�l� olarak belirlenmelidir. Optimal glisemik kontrol� sa�layabilmek i�in kan glukoz izlemesi ve ins�lin doz ayarlamalar� �nerilir.
Bireysel ins�lin gereksinimi genellikle 0.5 ve 1.0 �nite/kg/g�n aras�ndad�r. NovoMix50 FlexPen bu gereksinimi tamamen veya k�smen kar��layabilir.
Tip 2 diyabetli hastalarda, NovoMix50 FlexPenmonoterapi olarak veya tek ba��na, metformin tedavisi ile kan glukozunun yeterli kontrol edilemedi�i durumlarda metformin ile kombine halde kullan�labilir.
Hasta, fiziksel aktivitesini art�r�rsa, genel diyetini de�i�tirirse ya da ba�ka hastal�klar da varsa, doz ayarlamas� yapmak gerekebilir.
Di�er ins�lin t�bbi �r�nlerinden ge�i�:
Di�er ins�lin preparatlar�ndan NovoMix50 FlexPen'e ge�i�, doz ve uygulama zaman�n�n ayarlanmas�n� gerektirebilir. Ge�i� ve ge�i�ten sonraki ilk haftalarda s�k� glukoz g�zetimi �nerilmektedir (bkz. b�l�m 4.4).
Uygulama �ekli:
NovoMix50 FlexPen, ins�lin analogu olan ins�lin aspart�n bifazik s�spansiyonudur. S�spansiyon, 50/50 oran�nda h�zl� etkili ve orta etkili ins�lin aspart i�ermektedir.
NovoMix50 FlexPensadece deri alt� uygulama i�indir.
NovoMix50 FlexPenkar�n duvar� veya uyluk b�lgesine deri alt�na enjekte edilerek kullan�l�r. E�er uygunsa kal�a veya deltoid b�lgeleri kullan�labilir. Lipodistrofi ve kutan�z amiloidoz riskini azaltmak i�in enjeksiyonlar, ayn� b�lge i�inde olmak ko�uluyla, farkl� yerlere yap�lmal�d�r (bkz. B�l�m 4.4 ve 4.8). De�i�ik enjeksiyon b�lgelerinin NovoMix50 FlexPen'in emilimine etkisi ara�t�r�lmam��t�r. Etki s�resi doza, enjeksiyon b�lgesine, kan ak�m�na, �s� ve fiziksel aktivitenin derecesine ba�l� olarak de�i�iklik g�sterecektir.
NovoMix50 FlexPen'in etki ba�lang�c� bifazik insan ins�lininden daha h�zl�d�r ve genellikle yemekten hemen �nce verilmelidir. Gerekli oldu�unda, NovoMix50 FlexPenyemekten hemen sonra verilebilir.
Detayl� kullan�c� talimatlar� i�in, kullanma talimat�na bak�n�z. FlexPenile uygulama:
NovoMix50 FlexPen, NovoFineveya NovoTwisti�ne u�lar� ile kullan�lmak �zere tasarlanm�� bir kullan�ma haz�r (renk kodlu) kalemdir. FlexPen1'er �nitelik art��larla 1-60 �nite sa�lar. NovoMix50 FlexPensadece subk�tan enjeksiyon i�in uygundur. E�er ��r�nga ile uygulama gerekli ise, bir flakon kullan�lmal�d�r.
�zel pop�lasyonlara ili�kin ek bilgiler:
B�brek/Karaci�er yetmezli�i:
B�brek ve karaci�er yetmezlikleri hastan�n ins�lin ihtiyac�n� azaltabilir.
B�brek veya karaci�er yetmezli�i olan hastalarda, glukoz g�zetimi artt�r�lmal� ve ins�lin aspart dozu bireye �zg� olarak ayarlanmal�d�r.
Pediyatrik Pop�lasyon
18 ya��n alt�ndaki �ocuklarda NovoMix 50 FlexPen'in etkililik ve g�venlili�i kan�tlanmam��t�r. Veri mevcut de�ildir.
Geriyatrik Pop�lasyon
Ya�l� hastalarda (≥ 65 ya�) glukoz g�zetimi artt�r�lmal� ve ins�lin aspart dozu bireye �zg� olarak ayarlanmal�d�r.
4.3. Kontrendikasyonlar
�ns�lin aspart veya yard�mc� maddelerden herhangi birisine a��r� duyarl�l�k durumlar� (bkz. b�l�m 6.1).
4.4. �zel kullan�m uyar�lar� ve �nlemleri
NovoMix50 FlexPen, ciddi hipoglisemi ile sonu�lanabilece�inden damar i�ine uygulanmamal�d�r. Kas i�ine uygulamadan ka��n�lmal�d�r. NovoMix50 FlexPenins�lin inf�zyon pompalar�nda kullan�lmamal�d�r.
De�i�ik zaman dilimleri aras�nda yolculuk, hastan�n ins�lini ve ���nleri farkl� zamanda almas�n� gerektirebilece�inden, seyahat �ncesinde doktora dan���lmal�d�r.
Hiperglisemi
Yetersiz dozlarda kullan�m� veya tedaviye ara verilmesi, �zellikle tip I diyabette hiperglisemiye ve diyabetik ketoasidoza yol a�abilir. Genellikle hipergliseminin ilk belirtileri saatler veya g�nler i�inde giderek artar. Susuzluk, idrar yapma s�kl���nda art��, bulant�, kusma, ba� d�nmesi, k�zar�k-mor kuru deri, a��z kurulu�u, i�tah kayb�na ilaveten nefesin aseton kokmas�n� i�erir. Tip I diyabette, tedavi edilmeyen hiperglisemik vakalar en sonunda diyabetik ketoasidoza yol a�abilir, bu potansiyel olarak �l�mc�ld�r.
Hipoglisemi
Bir ana ���n�n atlanmas� veya plans�z, a��r fiziksel egzersiz yap�lmas� hipoglisemiye yol a�abilir.
E�er ins�lin dozu gerekli ins�line g�re �ok y�ksekse hipoglisemi olu�abilir. Hipoglisemi durumunda veya hipoglisemiden ��phelenilirse, NovoMix50 FlexPenenjekte edilmemelidir. Doz ayarlamas�, hastan�n kan �ekeri sabitlendikten sonra d���n�lmelidir (bkz. b�l�m 4.2, 4.8 ve 4.9).
�ntensif ins�lin tedavisi gibi tedavilerle kan glukoz kontrol� b�y�k �l��de sa�lanm�� olan hastalarda al���lm�� hipoglisemi uyar�c� semptomlar�nda de�i�iklik olabilece�inden hastalar bu konuda bilgilendirilmelidir. Uzun s�redir diyabeti olan hastalarda genel uyar�c� semptomlar yok olabilir.
NovoMix50 FlexPen'in yemekler ile �ok yak�n zamanda uygulanmas� gerekti�inden, g�dalar�n emiliminde bir gecikme beklenebilecek ba�ka hastal�klar� olan veya birlikte ba�ka ila�lar kullanmakta olan hastalarda, preparat�n etkisinin h�zl� ba�layaca�� dikkate al�nmal�d�r.
E�lik eden ba�ka hastal�k; �zellikle enfeksiyon hastal�klar� ve ate� yapan durumlar genellikle hastan�n ins�lin gereksinimini art�r�r. B�brekteki, karaci�erdeki ya da b�brek�st�, hipofiz veya tiroit bezlerini etkileyen hastal�klar ins�lin dozunda de�i�iklik gerektirebilir.
Hastalar de�i�ik tipte ins�linlere transfer edildi�inde, hipogliseminin erken uyar�c� semptomlar� �nceki ins�linle ya�ad�klar�ndan farkl� olabilir veya daha az belirgin hale gelebilir.
Di�er ins�lin t�bbi �r�nlerinden transfer
Hastalar�n yeni bir �e�it veya marka ins�line transfer edilmesi s�k� bir t�bbi g�zetim alt�nda yap�lmal�d�r. Dozaj, marka (�retici), �e�it, orijin (hayvan ins�lini, insan ins�lini veya ins�lin analogu) ve/veya �retim metodundaki (hayvan kaynakl� ins�lin yerine rekombinant DNA) de�i�iklikler doz de�i�ikliklerini gerektirebilir. NovoMix50 FlexPen'e transfer edilen hastalar�n daha �nce kulland�klar� ins�line g�re g�nl�k enjeksiyon say�s�nda art�� veya dozunda de�i�iklik yapmalar� gerekebilir. Doz ayarlamas� gerekti�inde, bu bazen ilk dozda bazen de ilk birka� hafta veya ay i�inde yap�labilir.
Enjeksiyon yeri reaksiyonlar�
Herhangi bir ins�lin tedavisi s�ras�nda a�r�, k�zar�kl�k, �rtiker, enflamasyon, morarma, �i�me ve ka��nt� gibi enjeksiyon b�lgesi reaksiyonlar� olu�abilir. Belirli bir b�lgede enjeksiyon yerinin devaml� de�i�tirilmesi bu reaksiyonlar�n olu�ma riskini azalt�r. Reaksiyonlar genellikle birka� g�n ila birka� haftada d�zelir. Enjeksiyon yeri reaksiyonlar� nadiren NovoMix50 FlexPen'in b�rak�lmas�n� gerektirebilir.
Deri ve deri alt� doku hastal�klar�
Hastalara, lipodistrofi ve kutan�z amiloidoz geli�me riskini azaltmak i�in enjeksiyon b�lgesini s�rekli rotasyona tabi tutmalar� konusunda talimat verilmelidir. Bu reaksiyonlar�n g�r�ld��� b�lgelerde ins�lin enjeksiyonlar�n� takiben gecikmi� ins�lin emilimi ve k�t�le�mi� glisemik kontrol riski vard�r. Enjeksiyon yerinde ani de�i�iklik yap�p, ciltte etkilenmemi� bir b�lgeye enjeksiyon yapman�n hipoglisemiye neden oldu�u bildirilmi�tir. Enjeksiyon yerinde etkilenen bir b�lgeden etkilenmeyen bir b�lgeye de�i�iklik yap�ld�ktan sonra kan �ekerinin izlenmesi �nerilir ve antidiyabetik ila�lar�n doz ayarlamas� d���n�lebilir.
NovoMix50 FlexPen ile pioglitazon kombinasyonu
�zellikle kalp yetmezli�i geli�imi riski y�ksek olan hastalarda, pioglitazon ile ins�lin kombine kullan�ld���nda kalp yetmezli�i vakalar� bildirilmi�tir. Bu, pioglitazon ve NovoMix50 FlexPen'in kombine tedavisi d���n�ld���nde ak�lda tutulmal�d�r. E�er bu kombinasyon kullan�l�rsa, hastalar kalp yetmezli�i, kilo al�m� ve �demin semptom ve belirtileri i�in incelenmelidir. Pioglitazon, kardiyak semptomlarda herhangi bir k�t�le�me oldu�unda kesilmelidir.
Kazayla olu�an kar���kl�klar�n/ t�bbi hatalar�n engellenmesi
NovoMix50 FlexPenile di�er ins�lin �r�nlerinin yanl��l�kla kar��t�r�lmas�n� �nlemek �zere hastalara, her enjeksiyon �ncesinde her zaman ins�lin etiketini kontrol etmeleri tavsiye edilmelidir.
�ns�lin antikorlar�
�ns�lin uygulamas� ins�lin antikorlar�n�n olu�mas�na neden olabilir. Hiperglisemi ya da hipoglisemi e�ilimini kontrol alt�na almak i�in, ins�lin antikorlar�n�n varl��� nadir durumlarda ins�lin dozunun ayarlanmas�n� gerektirebilir.
Hipokalemi
�ns�lin aspart dahil t�m ins�lin ila�lar�, ekstrasel�lerden intrasel�ler bo�lu�a potasyum ge�i�ine neden olarak hipokalemiye yol a�ar. Tedavi edilmeyen hipokalemi, solunum felcine, ventrik�ler aritmiye ve �l�me neden olabilir. Hipokalemi riski olan hastalarda (�rn. potasyum d���r�c� ila�lar kullanan hastalar, serum potasyum konsantrasyonuna duyarl� ila�lar alan hastalar) potasyum d�zeyleri izlenmelidir.
Takip edilebilirlik
Biyoteknolojik �r�nlerin takip edilebilirli�inin sa�lanmas� i�in uygulanan �r�n�n ticari ismi ve seri numaras� mutlaka hasta dosyas�na kaydedilmelidir.
Bu t�bbi �r�n her “doz”unda 1 mmol (23 mg)'dan daha az sodyum ihtiva eder; yani asl�nda “sodyum i�ermez”.
4.5. Di�er t�bbi �r�nler ile etkile�imler ve di�er etkile�im �ekilleri
Baz� ila�lar�n glukoz metabolizmas� ile etkile�ime girdi�i bilinmektedir. A�a��daki maddeler hastan�n ins�lin ihtiyac�n� azaltabilir:Oral antidiyabetik ila�lar, monoamin oksidaz inhibit�rleri (MAO�), beta blokerler, anjiyotensin d�n��t�r�c� enzim (ADE) inhibit�rleri, salisilatlar, anabolik steroidler ve s�lfonamidler.
A�a��daki maddeler hastan�n ins�lin ihtiyac�n� art�rabilir:
Oral kontraseptifler, tiyazidler, glukokortikoidler, tiroit hormonlar�, sempatomimetikler, b�y�me hormonu ve danazol.
Beta blokerler hipoglisemi semptomlar�n� maskeleyebilirler.
Oktreotid/ lanreotit ins�lin ihtiyac�n� hem artt�rabilir hem de azaltabilir. Alkol, ins�linin hipoglisemik etkisini yo�unla�t�rabilir veya azaltabilir. �zel pop�lasyonlara ili�kin ek bilgiler
�zel pop�lasyonlarda etkile�imlere dair bir �al��ma y�r�t�lmemi�tir.
Pediyatrik pop�lasyon:
Pediyatrik pop�lasyonda etkile�imlere dair bir �al��ma y�r�t�lmemi�tir.
4.6. Gebelik ve laktasyon
Gebelik kategorisi: C
�ns�lin aspart�n gebelikte kullan�m� ile ilgili klinik deneyimler s�n�rl�d�r.
�ocuk do�urma potansiyeli bulunan kad�nlar/Do�um kontrol� (Kontrasepsiyon)
Herhangi bir bilgi bulunmamaktad�r.
Gebelik D�nemi
NovoMix50 FlexPen'in gebe kad�nlarda kullan�m�na ili�kin klinik �al��ma s�n�rl�d�r.
Hayvanlar �zerinde yap�lan �al��malar, gebelik /ve-veya/ embriyonal/fetal geli�im /ve-veya/ do�um /ve-veya/ do�um sonras� geli�im �zerindeki etkiler bak�m�ndan yetersizdir. �ns�lin aspart ile ilgili konvansiyonel g�venlilik farmakolojisi, tekrarlayan doz toksisitesi, �reme �zerine genotoksisite ve toksisite �al��malar�na dayanan klinik olmayan veriler insanlar i�in hi�bir �zel zarar g�stermemektedir (bkz. B�l�m 5.3).
Genelde, diyabetli gebe kad�nlar�n gebelikleri s�resince ve gebe kalmay� d���nenlerde kan glukozunun yo�un �ekilde takip edilmesi ve kontrol� �nerilmektedir. �ns�lin gereksinimi genellikle gebeli�in ilk trimesterinde azalmakta ve ikinci ve ���nc� trimesterde giderek artmaktad�r. Do�umdan sonra, ins�lin gereksinimi h�zla gebelik �ncesi d�neme d�ner.
Laktasyon d�nemi
Laktasyon d�neminde NovoMix50 FlexPentedavisi i�in herhangi bir k�s�tlama yoktur. Emziren annelerin ins�lin kullanmas�n�n bebek i�in hi�bir riski yoktur. Bununla birlikte NovoMix50 FlexPendozunun ayarlanmas� gerekebilir.
�reme yetene�i/Fertilite
Hayvan �reme �al��malar� fertilite a��s�ndan ins�lin aspart ve insan ins�lini aras�nda herhangi bir fark ortaya ��karmam��t�r.
4.7. Ara� ve makine kullan�m� �zerindeki etkiler
Hastan�n konsantre olma ve reaksiyon g�sterme becerisi hipogliseminin bir sonucu olarak bozulabilir. Bu durum, bu becerilerin �zel �nem ta��d��� ko�ullarda risk olu�turabilir (�rn. araba s�rme veya makine kullanma).
Hastalar�n araba s�rme veya makine kullanma esnas�nda hipoglisemiye girmemeleri i�in gerekli �nlemleri almalar� �nerilmelidir. Bu durum �zellikle hipogliseminin uyar�c� belirtilerini az olarak farkeden veya hi� farketmeyen ki�iler i�in ya da s�k s�k hipoglisemi ata�� ge�iren hastalar i�in �nemlidir. Bu gibi durumlarda ara� veya makine kullan�m�n�n uygunlu�u de�erlendirilmelidir.
4.8. �stenmeyen etkiler
G�venlilik Profilinin �zeti
NovoMix50 FlexPenkullan�m� s�ras�nda hastalarda g�r�len advers ila� reaksiyonlar� genellikle ins�lin aspart�n farmakolojik etkilerinden dolay� g�r�l�r.
Tedavi s�ras�nda en �ok rapor edilen istenmeyen etki hipoglisemidir. Hipogliseminin s�kl���, hasta pop�lasyonuna, dozaja ve glisemik kontrol�n seviyesine g�re de�i�ebilir, l�tfen a�a��daki “Se�ilmi� istenmeyen etkilerin tan�m�” b�l�m�ne bak�n�z.
�ns�lin tedavisinin ba�lang�c�nda k�r�lma anomalileri, �dem ve enjeksiyon yeri reaksiyonlar� (enjeksiyon yerinde a�r�, k�zar�kl�k, �rtiker, inflamasyon, morarma, �i�me ve ka��nma) olu�abilir. Bu reaksiyonlar genellikle ge�ici t�rdedir. Kan glukoz kontrol�ndeki h�zl� iyile�me, genellikle geri d�n���ml� olan akut a�r�l� n�ropatiye neden olabilir. Uzun s�reli geli�mi� glisemik kontrol diyabetik retinopatinin ilerleme riskini azalt�rken, glisemik kontrol�n ani geli�imi ile ins�lin terapisinin yo�unlu�u, diyabetik retionapatinin ge�ici olarak k�t�le�mesi ile ba�lant�l� olabilir.
4.8. �stenmeyen etkiler
Klinik �al��malarda g�r�len ve ins�lin asparta ba�l� olarak de�erlendirilen advers ila� reaksiyonlar�n�n s�kl��� a�a��da s�ralanm��t�r. S�kl�klar �u �ekilde tan�mlanm��t�r:
�ok yayg�n (≥1/10); yayg�n (≥1/100 ila <1/10); yayg�n olmayan (≥1/1,000 ila <1/100); seyrek (≥1/10,000 ila <1/1,000); �ok seyrek (<1/10,000); bilinmiyor (eldeki verilerden hareketle tahmin edilemiyor).
Her bir s�kl�k gruplamas�nda, istenmeyen etkiler azalan ciddiyet s�ras�na g�re sunulmaktad�r.
Ba����kl�k sistemi hastal�klar�
Yayg�n olmayan: �rtiker, d�k�nt�, erupsiyonlar �ok seyrek: Anafilaktik reaksiyonlar*
Metabolizma ve beslenme hastal�klar�
�ok yayg�n: Hipoglisemi*
Sinir sistemi hastal�klar�
Seyrek: Periferal n�ropati (a�r�l� n�ropati)
G�z hastal�klar�
Yayg�n olmayan: K�r�lma bozukluklar�,diyabetik retinopati
Deri ve deri alt� doku hastal�klar� Yayg�n olmayan: Lipodistrofi* Bilinmiyor: Kutan�z amiloidoz*†
Genel bozukluklar ve uygulama b�lgesine ili�kin hastal�klar
Yayg�n olmayan: �dem, enjeksiyon yeri reaksiyonlar�
*Bkz. b�l�m ”Se�ilmi� istenmeyen etkilerin tan�m�”
†Pazarlama sonras� kaynaklardan elde edilen advers reaksiyon. Se�ilmi� istenmeyen etkilerin tan�m�
Anafilaktik reaksiyonlar:
Genel a��r� duyarl�l�k reaksiyonlar�n�n ( yayg�n deri d�k�nt�s�, ka��nma, terleme, gastrointestinal bozukluk, anjiyono�rotik �dem, nefes almada zorluk, �arp�nt� ve d���k kan bas�nc�n� i�eren) olu�umu �ok seyrektir ancak potansiyel olarak hayat� tehdit edebilir.
Hipoglisemi:
En �ok rapor edilen istenmeyen etki hipoglisemidir. Hipoglisemi, ins�lin dozu ins�lin ihtiyac�na g�re �ok y�ksekse olu�abilir. Ciddi hipoglisemi durumunda �uur kayb� ve/veya konv�lziyon olu�abilir ve beyin fonksiyonlar�nda ge�ici veya kal�c� hasarla hatta �l�mle sonu�lanabilir. Hipogliseminin semptomlar� genelde aniden belirir. Bunlar, so�uk terleme, so�uk soluk deri, yorgunluk, sinirlilik veya titreme, endi�e hissi, anormal derecede yorgunluk veya bitkinlik, kafa kar���kl���, konsantrasyon g��l���, sersemlik, a��r� a�l�k hissi, g�rme de�i�iklikleri, ba� a�r�s�, bulant� ve �arp�nt�d�r.
Klinik �al��malarda hipoglisemi s�kl���, hasta pop�lasyonu, dozaj ve glisemik kontrol�n seviyesine g�re de�i�mi�tir. Klinik �al��malar s�ras�nda hipogliseminin g�r�lme oranlar�, insan ins�lini ve ins�lin aspart aras�nda de�i�kenlik g�stermemi�tir.
Deri ve deri alt� doku hastal�klar�:
Lipodistrofi (lipohipertrofi, lipoatrofiyi i�eren) ve kutan�z amiloidoz enjeksiyon b�lgesinde olu�abilir ve lokal ins�lin absorpsiyonunu geciktirebilir. Belli bir alan i�indeki enjeksiyon yerinin devaml� de�i�tirilmesi bu reaksiyonlar�n olu�ma riskini azaltabilir veya �nleyebilir (bkz. B�l�m 4.4.).
�zel pop�lasyonlara ili�kin ek bilgiler:
Pediyatrik pop�lasyon
18 ya� alt�ndaki �ocuklarda NovoMix50 FlexPen'in etkililik ve g�venlili�i kan�tlanmam��t�r. Veri mevcut de�ildir.
Di�er �zel pop�lasyonlar
Pazarlama sonras� kaynaklara ve klinik �al��malara dayanarak, ya�l� hastalarda ve b�brek veya karaci�er yetmezli�i olan hastalarda g�zlemlenen istenmeyen etkilerin s�kl���, tipi ve ciddiyeti genel pop�lasyondaki kapsaml� deneyimlerden hi�bir farkl�l�k g�stermemi�tir.
��pheli advers reaksiyonlar�n raporlanmas�
Ruhsatland�rma sonras� ��pheli ila� advers reaksiyonlar�n�n raporlanmas� b�y�k �nem ta��maktad�r. Raporlama yap�lmas�, ilac�n yarar/risk dengesinin s�rekli olarak izlenmesine olanak sa�lar. Sa�l�k mesle�i mensuplar�n�n herhangi bir ��pheli advers reaksiyonu T�rkiye Farmakovijilans Merkezi (T�FAM)'ne bildirmeleri gerekmektedir. (www.titck.gov.tr; e- posta: tufam@titck.gov.tr; tel: 0 800 314 00 08; faks: 0 312 218 35 99)
4.9. Doz a��m� ve tedavisi
�ns�lin i�in spesifik olarak bir doz a��m� tan�mlanamaz ancak hastan�n ihtiyac�na g�re �ok y�ksek dozlarda verilirse birbirini takip eden evreler sonucunda hipoglisemi geli�ebilir:
Hafif hipoglisemi ataklar� oral yoldan glukoz veya �ekerli g�dalar al�narak tedavi edilebilir. Bu nedenle diyabetli hastalar�n beraberlerinde s�rekli �ekerli g�dalar bulundurmalar� �nerilmektedir.
5. FARMAKOLOJ�K �ZELL�KLER
5.1. Farmakodinamik �zellikler
Farmakoterap�tik grup: Diyabet tedavisinde kullan�lan ila�lar. H�zl� etkililer ile kombine orta ya da uzun etkili ins�linler ve analoglar�, enjektabl.
ATC kodu A10AD05.
NovoMix50 FlexPen, % 50 ��z�n�r ins�lin aspart (h�zl� etkili insan ins�lin analogu) ve %
50 protamin-kristalize ins�lin aspart�n (orta etkili insan ins�lin analogu) bifazik s�spansiyonudur.
Etki mekanizmas� ve farmakodinamik etkiler
�ns�lin aspart�n kan �ekerini d���r�c� etkisi, kas ve ya� h�crelerindeki resept�rlere ba�lanarak glukozun h�cre i�ine giri�ini kolayla�t�racak molek�lleri harekete ge�irmesi ile ortaya ��kar ve e� zamanl� olarak karaci�erden glukoz a���a ��kmas�n� da inhibe eder.
NovoMix50 FlexPen, % 50 ��z�n�r ins�lin aspart i�eren bir bifazik ins�lindir. ��z�n�r insan ins�linine g�re etki ba�lang�c� h�zl�d�r, bu nedenle yeme�e yak�n bir zamanda verilebilir (yeme�in ilk 0-10 dakikas� i�inde). Kristal faz� (% 50) etki profili insan NPH ins�linine benzeyen aktif profile sahip protamin-kristalize ins�lin aspart i�ermektedir.
NovoMix50 FlexPen'in etkisi s�bkutan enjeksiyonunu takiben 10-20 dakika i�inde ba�lar. Maksimum etki, enjeksiyondan sonra 1-4 saat i�inde elde edilir. Etki s�resi 14 ile 24 saat aras�ndad�r.(�ekil 1)
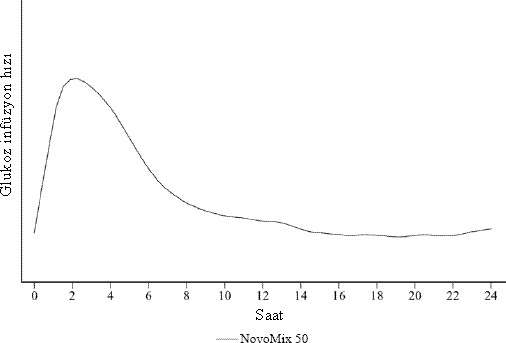
�ekil 1: Sa�l�kl� bireylerde NovoMix50 FlexPen'in aktivite profili
Molar bazda ins�lin aspart insan ins�linine e�de�er etkinliktedir.
5.2. Farmakokinetik �zellikler
Genel �zellikler��z�n�r insan ins�lini ile k�yasland��� zaman, ins�lin aspartta B28 pozisyonundaki aspartik asit ile prolin amino asidinin yer de�i�tirmesi, hekzamer olu�um e�ilimini azaltmaktad�r.
Emilim:
NovoMix50 FlexPen'in ��z�n�r faz� olan ins�lin aspart, total ins�linin %50'sini olu�turmaktad�r.
�ns�lin aspart, deri alt� dokusundan bifazik insan ins�lininin ��z�n�r ins�lin komponentinden daha h�zl� emilir. Geri kalan %50'lik k�sm� kristal form olan protamin-kristalize ins�lin asparttan olu�ur. �ns�lin aspart protamin, insan NPH ins�linine benzer uzam�� emilim profiline sahiptir.
Da��l�m:
Sa�l�kl� g�n�ll�lerde 445±135 pmol/l'lik bir ortalama maksimum serum konsantrasyonuna
0.30 �nite/kg (v�cut a��rl���) subk�tan doz uygulamas�ndan yakla��k 60 dakika sonra ula��l�r. Tip 2 diyabetli hastalarda, maksimum konsantrasyona uygulamadan yakla��k 95 dakika sonra ula��l�r.
Eliminasyon:
Herhangi bir bilgi bulunmamaktad�r.
Biyotransformasyon:
�ns�lin aspart�n bozunmas� insan ins�linine benzer, olu�an t�m metabolitleri inaktiftir.
Hastalardaki karakteristik �zellikler
NovoMix50 FlexPen'in farmakokinetik �zellikleri ya�l�larda, �ocuklarda veya b�brek ya da karaci�er yetmezli�i olan hastalarda ara�t�r�lmam��t�r.
5.3. Klinik �ncesi g�venlilik verileri
�ns�lin aspart ile ilgili konvansiyonel g�venlilik farmakolojisi, tekrarlayan doz toksisitesi, �reme �zerine genotoksisite ve toksisite �al��malar�na dayanan klinik olmayan veriler insanlar i�in hi�bir �zel zarar g�stermemektedir.
�ns�lin ve IGF-1 resept�r b�lgelerine ba�lanma ve h�cre b�y�mesi �zerine olan etkileri de dahil olmak �zere in vitro testlerde ins�lin aspart�n insan ins�linine benzer bir �ekilde davran�� g�sterdi�i belirlenmi�tir. �al��malar ayn� zamanda, ins�lin aspart�n ins�lin resept�r�ne ba�lanmas�ndaki ayr�l���n insan ins�linine e�de�er oldu�unu g�stermi�tir.
6. FARMAS�T�K �ZELL�KLER
6.1. Yard�mc� maddelerin listesi
Gliserol Fenol Metakrezol �inko klor�r
Sodyum klor�r Disodyum fosfat dihidrat
Protamin s�lfat (somon bal���ndan elde edilir) Sodyum hidroksit (pH ayar� i�in)
Hidroklorik asit (pH ayar� i�in) Enjeksiyonluk su
6.2. Ge�imsizlikler
Ge�imlilikle ilgili �al��malar olmad���ndan, bu t�bbi �r�n di�er t�bbi �r�nlerle kar��t�r�lmamal�d�r.
6.3. Raf �mr�
A��lmadan �nce: 24 ay.
Kullan�m s�ras�nda veya yedek olarak ta��n�rken: En fazla 4 hafta i�inde t�ketilmelidir.
6.4. Saklamaya y�nelik �zel tedbirler
A��lmadan �nce: Buzdolab�nda dondurucu k�s�mdan uzakta (2°C - 8°C) saklanmal�d�r. Dondurulmamal�d�r.
Kullan�m s�ras�nda veya yedek olarak ta��n�rken: 30°C'nin alt�nda saklanmal�d�r. Buzdolab�nda saklanmamal�d�r. Dondurulmamal�d�r.
NovoMix50 FlexPen'i ���ktan korumak i�in kalemin kapa�� kapal� tutulmal�d�r.
6.5. Ambalaj�n niteli�i ve i�eri�i
Polipropilenden yap�lm�� �ok dozlu kullan�ma haz�r kalemin i�inde bir piston (bromobutil) ve bir lastik kapak (bromobutil/poliizopren) ile kapat�lm�� cam (Tip 1) bir kartu� bulunur. Kartu� 3 ml s�spansiyon i�erir. Kartu�un i�inde s�spansiyonun kar��mas�n� kolayla�t�ran bir cam top bulunur.
Paketlerde 5 adet (3 ml) kalem bulunur.
6.6. Be�eri t�bbi �r�nden arta kalan maddelerin imhas� ve di�er �zel �nlemler
Kullan�lmam�� olan �r�nler ya da at�k maddeler “T�bbi At�klar�n Kontrol� Y�netmeli�i” ve “Ambalaj At�klar�n�n Kontrol� Y�netmeli�i” gereklerine uygun olarak imha edilmelidir.
NovoMix50 FlexPenbuzdolab�ndan ��kar�ld�ktan sonra, ins�lin ilk kez kullan�laca�� zaman tarif edildi�i bi�imde, kar��t�r�lmadan �nce NovoMix50 FlexPen'in oda s�cakl���na ula�mas� beklenmelidir.
Kar��t�r�lan s�v�n�n e�it oranda beyaz, bulan�k ve sulu olmad��� farkedilirse bu t�bbi �r�n kullan�lmamal�d�r.
Kullanmadan hemen �nce NovoMix50 FlexPens�spansiyonunun iyice kar��t�r�lmas�n�n gerekti�i hastalara �zellikle vurgulanmal�d�r.
Donmu� NovoMix50 FlexPenkullan�lmamal�d�r.
Hastalar, her enjeksiyon sonras� i�ne ucunu atmalar� konusunda uyar�lmal�d�r. NovoMix50 FlexPenve i�ne u�lar� yaln�z bir ki�inin kullan�m� i�indir.
Kartu� yeniden doldurulmamal�d�r.
 Belso�uklu�u, Chlamydia ve Frengi
Belso�uklu�u, bakterilerin sebep oldu�u bir enfeksiyondur. Cinsel ili�ki
yoluyla bula��r ve d�lyata�� boynunda, idrar yollar�nda, an�ste, makatta ve
bo�azda enfeksyona sebep olabilir.
Belso�uklu�u, Chlamydia ve Frengi
Belso�uklu�u, bakterilerin sebep oldu�u bir enfeksiyondur. Cinsel ili�ki
yoluyla bula��r ve d�lyata�� boynunda, idrar yollar�nda, an�ste, makatta ve
bo�azda enfeksyona sebep olabilir. |
 Kalp Krizi
Kalbe giden kan ak��� durdu�unda kalp krizi meydana gelir.
Kalp Krizi
Kalbe giden kan ak��� durdu�unda kalp krizi meydana gelir. |
�LA� E�DE�ERLER�
| E�de�er �la� Ad� | Barkodu | �la� Fiyat� |
|---|---|---|
| HUMULIN-M | 8699673954172 | 1,086.32TL |
| MIXTARD | 8699676950447 | 939.77TL |
| NOVOMIX | 8699676950706 | 1,411.50TL |
| NOVORAPID | 8699676770656 | 609.83TL |
| Di�er E�de�er �la�lar |
 |
Diyabet Hastal��� Diyabet, ins�lin hormonu ile ilgili problemlerden kaynaklanan bir hastal�kt�r. |
 |
Diyabet Hastal��� Diyabet, ins�lin hormonu ile ilgili problemlerden kaynaklanan bir hastal�kt�r. |
 |
Artrit Artrit, olduk�a yayg�n bir hastal�kt�r ancak iyi anla��lamam��t�r. Asl�nda �artrit� tek bir hastal���n ad� de�ildir; eklem a�r�s� veya eklem hastal�klar�n� adland�rman�n gayri resmi yoludur. |
�LA� GENEL B�LG�LER�
Novo Nordisk Sa�l�k �r�nleri Tic. Ltd. �ti.
| Geri �deme Kodu | A11702 |
| Sat�� Fiyat� | 1275.69 TL [ 4 May 2026 ] |
| �nceki Sat�� Fiyat� | 1275.69 TL [ 27 Apr 2026 ] |
| Original / Jenerik | Original �la� |
| Re�ete Durumu | Normal Re�eteli bir ila�d�r. |
| Barkodu | 8699676950829 |
| Etkin Madde | Insulin Aspart |
| ATC Kodu | A10AD30 |
| Birim Miktar | 100 |
| Birim Cinsi | IU |
| Ambalaj Miktar� | 5 |
| Sindirim Sistemi ve Metabolizma > �ns�linler ve Analoglar� > Insulin aspart |
| �thal ( ref. �lke : Ispanya ) ve Be�eri bir ila�d�r. |