DESOLETT 150 mcg/30 mcg tablet K�sa �r�n Bilgisi
{ Desogestrel + Etinilestradiol }
1. BE�ER� TIBB� �R�N�N ADI
DESOLETT 150mcg/30mcg tablet
2. KAL�TAT�F VE KANT�TAT�F B�LE��M
Etkin madde
Her bir tablet 150 mikrogram desogestrel ve 30 mikrogram etinilestradiol i�ermektedir.
Yard�mc� maddeler
Laktoz (ineklerden elde edilmi�tir); 80 mg tablet a��rl���na ula��lana kadar. Yard�mc� maddeler i�in 6.1'e bak�n�z.
3. FARMAS�T�K FORMU
Tablet
Bir y�z�nde 5'in �zerinde “TR” bask�s� ve di�er taraf�nda “ORGANON” yazan yuvarlak, bikonveks, 6 mm �ap�nda, beyaz renkte tablet.
ALT y�kselmeleri
Hepatit C vir�s� enfeksiyonlar� (HCV) i�in ribavirin ya da dasabuvir i�eren veya i�ermeyen ombitasvir / paritaprevir / ritonavir i�eren t�bbi �r�nlerle tedavi edilen hastalarda yap�lan klinik �al��malar s�ras�nda, normal �st s�n�r�n�n (N�S) 5 kat�ndan daha fazla transaminaz (ALT) y�kselmeleri, kombine hormonal kontraseptifler (KHK'ler) gibi etinilestradiol i�eren ila�lar kullanmakta olan kad�nlarda anlaml� olarak daha s�kl�kla olu�mu�tur. Ayr�ca glekaprevir / pibrentasvir ile tedavi edilen hastalarda da, KHK gibi etinilestradiol i�eren ila�lar kullanan kad�nlarda ALT y�kselmeleri g�zlenmi�tir (bkz. B�l�m 4.3 ve 4.5).
4. KL�N�K �ZELL�KLER
4.1. Terap�tik endikasyonlar
Oral kontrasepsiyon (Do�um kontrol�)
DESOLETT re�etelenme karar�nda kad�n�n mevcut risk fakt�rleri, �zellikle ven�z tromboembolizm (VTE) i�in risk fakt�rleri ve DESOLETT kullan�m�yla VTE riskinin di�er kombine hormonal kontraseptiflerle (KHK) kar��la�t�rmas� g�z �n�nde bulundurulmal�d�r (bkz. b�l�m 4.3 ve 4.4).
4.2. Pozoloji ve uygulama �ekli
DESOLETT nas�l kullan�lmal�d�r
Tabletler paketin �zerinde belirtilen s�rayla, her g�n yakla��k ayn� saatlerde yeterli miktarda su ile al�nmal�d�r. 21 ard���k g�n boyunca g�nde bir tablet al�nacakt�r. Bir sonraki pakete, genellikle �ekilme kanamas�n�n ger�ekle�ti�i 7 g�nl�k tablet al�nmayan aradan sonra ba�lanacakt�r. Kanama genellikle son tablet al�nd�ktan 2-3 g�n sonra ba�lar ve bir sonraki pakete ba�land���nda bitmemi� olabilir.
DESOLETT kullanmaya nas�l ba�lanacakt�r
Daha �nce hormonal do�um kontrol� uygulanmam��sa (ge�en ay i�erisinde)
Tercihen ilk paketten tablet al�m�na adet d�neminin birinci g�n�nde (adet kanamas�n�n ilk g�n�) ba�lanmas� �nerilir; bu durumda ilave do�um kontrol �nlemlerine gerek yoktur.
E�er adet kanamas� ba�lam��sa (2, 3 veya 4 g�n �nce), tablet al�m�na menstr�al periyodun 5. g�n� ba�lanmal�d�r. Bu durumda tablet kullan�lan ilk 7 g�n s�resince ilave do�um kontrol �nlemlerinin al�nmas� �nerilmektedir.
E�er adet kanamas� ba�layal� 5 g�nden fazla zaman olmu�sa, hastaya DESOLETT tableti
almadan �nce bir sonraki adet d�nemine kadar beklemesi s�ylenmelidir.
21 g�nl�k hap veya ba�ka bir 22 g�nl�k haptan DESOLETT'e ge�i�:
Eski paketteki t�m tabletler bitirilmelidir. �lk DESOLETT tablet ertesi g�n al�nmal�d�r; yani tabletlerin al�m� aras�nda hi� bo�luk b�rak�lmaz ve hastan�n adet d�neminin ba�lamas�n� beklemesine gerek yoktur. Tabletler “DESOLETT nas�l kullan�lmal�d�r” ba�l��� alt�nda verilen talimatlara g�re al�nmal�d�r. �lave do�um kontrol �nlemlerinin al�nmas� gerekmez. Hasta ilk DESOLETT paketinin sonuna kadar adet kanamas� ya�amayacakt�r; ancak bunun zarar� yoktur ve tablet al�nan g�nlerde bir miktar kanama olursa bunun da zarar� yoktur.
Ba�ka bir kombine her g�n al�nan haptan (28 g�nl�k tabletler) DESOLETT'e ge�i�: DESOLETT'e her g�n al�nan hap paketindeki son aktif tablet al�nd�ktan sonra (yani 21 veya 22 tablet al�nd�ktan sonra) ba�lanmal�d�r. �lk DESOLETT tablet ertesi g�n al�n�r; yani tabletlerin al�m� aras�nda hi� bo�luk b�rak�lmaz ve hastan�n adet d�neminin ba�lamas�n� beklemesine gerek yoktur. Kesintisiz olarak 21 g�n boyunca her g�n yakla��k ayn� saatte bir tablet al�n�r ve bunu 7 g�nl�k tabletsiz d�nem izler. Sonraki her pakete 7 g�nl�k tabletsiz d�nem bitince ba�lan�r. �lave do�um kontrol �nlemlerinin al�nmas� gerekmez. Her g�n al�nan hap paketinde kalan tabletler at�lmal�d�r. Hasta ilk DESOLETT paketinin sonuna kadar adet kanamas� ya�amayacakt�r; ancak bunun zarar� yoktur ve tablet al�nan g�nlerde bir miktar kanama olursa bunun da zarar� yoktur.
Sadece progestojen i�eren bir tabletten (Mini Hap) DESOLETT'e ge�i�:
�lk DESOLETT tablet, adet kanamas�n�n ilk g�n�nde (o g�n kad�n bir mini hap alm�� olsa bile) al�nmal�d�r. Kesintisiz olarak 21 g�n boyunca her g�n yakla��k ayn� saatte bir tablet al�n�r ve bunu 7 g�nl�k tabletsiz d�nem izler. Sonraki her pakete 7 g�nl�k tabletsiz d�nem dolduktan sonra ba�lan�r. Daha sonra ilave do�um kontrol �nlemlerinin al�nmas� gerekmez. Mini hap paketinde kalan t�m sadece progestojen i�eren haplar at�lmal�d�r.
E�er kad�n bir mini hap almaktaysa, her zaman adet kanamas� ya�amayabilir (�zellikle emzirme d�neminde). �lk DESOLETT tablet, mini hap�n b�rak�ld��� g�n�n ertesi g�n� al�nmal�d�r. Mini hap paketinde kalan t�m haplar at�lmal�d�r. �lk 7 g�n boyunca ilave do�um kontrol �nlemleri al�nmal�d�r.
Sadece progestojen i�eren enjeksiyon, implant veya progestojen salan bir rahim i�i sistemden ge�i�
Kad�n implanttan herhangi bir g�nde, rahim i�i sistemden bu sistemin b�rak�ld��� g�n ve enjektabl bir �r�nden sonraki enjeksiyon zaman� geldi�inde ge�i� yapabilir. �lk 7 g�n boyunca ilave do�um kontrol �nlemleri al�nmal�d�r.
Do�umdan Sonra Uygulama
Bebek do�duktan sonra, emzirmeyen annelere hormonal kontraseptif uygulamas�na do�umdan 21 g�n sonra ba�lanmal�d�r; bu durumda hi�bir ilave do�um kontrol �nlemine gerek yoktur. E�er do�umdan sonra cinsel ili�ki ger�ekle�mi�se, hormonal kontraseptif kullan�m� adet kanamas�n�n ilk g�n�ne kadar ertelenmelidir.
DESOLETT'in do�um sonras� uygulanmas�na do�umun ard�ndan 21 g�nden sonra ba�lan�rsa, ilk 7 g�n ilave kontraseptif �nlemler gereklidir.
Not: Emziren annelere kombine hap kullanmamalar� tavsiye edilmelidir; ��nk� kombine hap anne s�t�n�n miktar�n� azaltabilir; onun yerine sadece progestojen i�eren bir hap kullanmalar� �nerilmelidir.
D���k veya k�rtajdan sonra uygulamaya derhal ba�lanmal�d�r; bu durumda hi�bir ilave do�um kontrol �nlemine gerek yoktur.
�lave do�um kontrol �nlemleri
�lave do�um kontrol �nlemleri gerekirse, hastaya ya hi� cinsel ili�kiye girmemesi ya da diyafram ile birlikte spermisit kullanmas� ya da e�inin prezervatif kullanmas� tavsiye edilmelidir.
Takvim y�ntemleri �nerilmemelidir ��nk� hap do�al menstr�asyon d�ng�s�yle ili�kili ola�an siklus de�i�ikliklerini (�rn., servikal mukusta ve v�cut s�cakl���nda de�i�iklikler) olumsuz etkiler.
Bir adet d�nemi nas�l atlan�r?
Bir adet d�nemini atlamak i�in, yeni DESOLETT paketine mevcut paket bitirildikten sonraki g�n ba�lanmal�d�r (hasta tabletsiz g�nleri atlar). Tablet al�m�na ola�an �ekilde devam edilmelidir. �kinci paketin kullan�m� s�ras�nda kad�n hafif lekelenme veya ara kanama ya�ayabilir; ancak hi�bir tablet atlanmad��� s�rece ilave do�um kontrol y�ntemine ihtiya� yoktur. Sonraki DESOLETT paketine, adet kanamas� tamamen bitmi� olsun veya olmas�n, ola�an 7 g�nl�k tabletsiz d�nemden sonra ba�lan�r.
Tablet kullan�m� unutuldu�unda yap�lmas� gerekenler:
Tablet al�m�n�n unutulmas� durumunda �neriler
Tabletlerin al�m� unutulursa DESOLETT'in g�venilirli�i azalabilir:
Unutulan tablet 12 saat i�erisinde al�n�rsa, ilave hi�bir �nleme gerek yoktur; sonraki tabletler
normal zaman�nda al�nmal�d�r.
Kullan�c�n�n tablet almay� unutmas�ndan itibaren 12 saatten fazla bir s�re ge�mi�se, gebeli�e kar�� koruyucu etki azalm�� olabilir. Kad�n, almay� unuttu�u son tableti almal� (ayn� g�n iki tablet al�nmas� anlam�na gelse bile) ve ard�ndan tabletleri normal zaman�nda almaya devam etmelidir. Sonraki 7 g�n boyunca ilave do�um kontrol �nlemleri al�nmal� ve hasta “7 g�n kural�n�” uygulamal�d�r.
7 G�n Kural�
Herhangi bir tabletin al�m� 12 saatten uzun s�re unutulursa, Kad�n 12 saatten daha uzun s�ren kusma veya diyare ya�arsa,
Kad�n “Di�er t�bbi �r�nler ile etkile�imler” b�l�m�nde listelenen ila�lardan herhangi birini al�yorsa:
Kad�n tabletleri ola�an �ekilde almaya devam etmeli ve sonraki 7 g�n boyunca ilave do�um kontrol �nlemleri al�nmal�d�r.
Ancak, bu 7 g�nl�k s�re mevcut paketin bitiminden sonras�na uzarsa, sonraki pakete mevcut paket bitti�i anda ba�lanmal�d�r; yani paketler aras�nda hi� bo�luk b�rak�lmamal�d�r (Bu, tablet al�m�nda olu�acak uzun s�reli bir aray� �nler; uzun s�reli ara ov�lasyon riskini artt�rabilir ve dolay�s�yla kontraseptif korumay� azaltabilir). Kad�n 2 paket bitene kadar adet kanamas� ya�amayabilir; ancak bunun zarar� yoktur ve tablet al�nan g�nlerde bir miktar kanama olursa bunun da zarar� yoktur.
Kusma veya �iddetli diyare durumunda �neriler
�iddetli gastrointestinal bozukluklarda, emilim tam olarak ger�ekle�meyebilir ve ilave do�um kontrol hap� almak gerekebilir. Diyare a��r� derecede �iddetli olmad�k�a, steroid emilimini etkilemez.
Tablet al�nd�ktan sonra 3-4 saat i�erisinde kusma meydana gelirse veya �iddetli veya uzun s�reli diyare durumlar�nda, unutulan tabletlerle ilgili �nerilere uyulmas� gerekmektedir. Normal tablet al�m takviminin de�i�tirilmesi arzu edilmiyorsa ba�ka bir paketten ekstra tablet(ler)in al�nmas� gerekmektedir.
Uygulama �ekli:
A��zdan yeterli miktarda su ile al�nmal�d�r.
�zel pop�lasyonlara ili�kin ek bilgiler:
B�brek/Karaci�er yetmezli�i:
Herhangi bir etkililik ve g�venlilik �al��mas� yap�lmam��t�r.
Karaci�er fonksiyon testlerinin sonu�lar� anormal olursa, tedavi b�rak�lmal�d�r. �lave bilgi i�in bkz. b�l�m 4.3. ve b�l�m 4.4.
Pediyatrik pop�lasyon:
18 ya��n alt�ndaki ad�lesanlarda desogestrelin g�venlili�i ve etkilili�i bilinmemektedir. Herhangi bir veri mevcut de�ildir. Pediyatrik pop�lasyonda kullan�m� uygun de�ildir.
Geriyatrik pop�lasyon:
Herhangi bir etkililik ve g�venlilik �al��mas� yap�lmam��t�r.
4.3. Kontrendikasyonlar
Etkin madde
KHK'ler a�a��da listelenen durumlar�n herhangi birinin varl���nda kullan�lmamal�d�r. A�a��da belirtilen durumlardan herhangi biri KHK kullan�m� s�ras�nda ilk defa ortaya ��karsa, �r�n kullan�m� hemen durdurulmal�d�r:
Mevcut ven�z tromboembolizm (VTE) veya VTE riski
VTE – mevcut VTE (antikoag�lan kullan�rken) veya VTE �yk�s� (�rn. derin ven trombozu [DVT] veya pulmoner emboli [PE])
APC direnci (Fakt�r V Leiden dahil), antitrombin III eksikli�i, protein C eksikli�i, protein S eksikli�i gibi ven�z tromboembolizm i�in bilinen kal�tsal veya edinilmi� predispozisyon
4.4. �zel kullan�m uyar�lar� ve �nlemleri
Uyar�lar:
A�a��da de�inilen durum ya da risk fakt�rlerinden herhangi birinin varl���nda, DESOLETT'in uygunlu�u kad�n ile tart���lmal�d�r.
Bu durumlardan veya risk fakt�rlerinden herhangi birinin �iddetlenmesi veya ilk kez g�r�lmesi durumunda, DESOLETT kullan�m�n�n durdurulup durdurulmayaca��na karar vermek i�in derhal doktoru ile temasa ge�mesi kad�na tavsiye edilmelidir.
Dola��m Bozukluklar�
Dola��m bozukluklar� ile ilgili advers etkilerin ortaya ��kma riski �zellikle 35 ya� �zeri ve sigara i�en kad�nlarda y�ksektir.
VTE riski
Herhangi bir KHK kullan�m� hi� kullan�m olmamas�na k�yasla VTE riskini art�r�r. Levonorgestrel, norgestimat veya noretisteron en d���k VTE riskiyle ili�kilendirilmi�tir. DESOLETT gibi di�er �r�nlerde risk seviyesi bunun iki kat�na kadar olabilir. En d���k VTE riski olan �r�n d���nda herhangi bir �r�n�n kullan�lmas�na, DESOLETT'le VTE riskinin ne oldu�u, mevcut risk fakt�rlerinin riski nas�l etkiledi�i ve kullan�m�n ilk y�l�nda VTE riskinin en fazla oldu�u kad�nla konu�ulduktan sonra karar verilmelidir. Buna ek olarak, 4 hafta veya daha uzun s�re KHK kullan�m�ndan sonra ara verilip tekrar ba�land���ndan, riskin artt���na dair bulgular vard�r.
KHK kullanmayan veya hamile olmayan kad�nlarda, bir y�l i�inde 10.000 kad�ndan 2'sinde VTE ger�ekle�ir. Ancak, altta yatan risk fakt�rlerine (bkz. a�a��daki b�l�m) ba�l� olarak, bir kad�ndaki ki�isel risk �ok daha y�ksek olabilir.
Desogestrel i�eren KHK kullanan 10.000 kad�ndan yakla��k 9 ila 12'sinde bir y�l i�erisinde VTE geli�ece�i tahmin edilmektedir; bu, bir y�lda levonorgestrel i�eren KHK kullanan
10.000 kad�ndan 6's�na kar��l�k gelmektedir.
Her iki durumda da bir y�ldaki VTE say�s�, hamile olan veya postpartum d�nemdeki kad�nlarda beklenen say�dan daha d���kt�r.
Vakalar�n %1 ila 2'sinde VTE �l�mc�l olabilir.
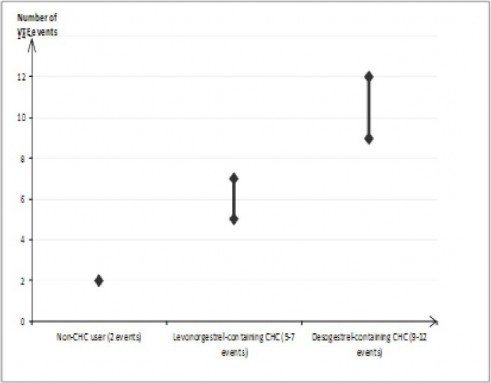
Bir y�lda 10.000 kad�nda VTE olaylar�n�n say�s�
KHK kullan�c�lar�nda hepatik, mezenterik, renal ya da retinal venler ve arterler gibi di�er kan damarlar�nda son derece seyrek olarak tromboz bildirilmi�tir.
VTE i�in risk fakt�rleri
KHK kullanan, ilave risk fakt�rleri olan bir kad�nda, �zellikle birden fazla risk fakt�r� varsa (bkz. a�a��daki tablo) ven�z tromboembolik komplikasyon riski b�y�k oranda artabilir.
Birden fazla risk fakt�r� nedeniyle y�ksek ven�z tromboembolizm riski olan kad�nlarda DESOLETT kontrendikedir (bkz. b�l�m 4.3). Bir kad�nda birden fazla risk fakt�r� varsa, risk art���, fakt�rlerin teker teker risk toplam�ndan daha y�ksek olabilir – bu durumda kad�n�n toplam VTE riski de�erlendirilmelidir. Risk yarar dengesi negatif olarak de�erlendiriliyorsa, KHK re�etelenmemelidir (bkz. b�l�m 4.3).
Tablo: VTE i�in risk fakt�rleri
Risk fakt�r� | Yorum |
Obezite (v�cut kitle indeksi [VK�] 30 kg/m'nin �zerinde) | VK� artt�k�a risk b�y�k oranda artar. Di�er risk fakt�rleri de mevcutsa �zellikle g�z �n�nde bulundurulmas� �nemlidir. |
Uzun s�reli hareketsiz kalma, maj�r cerrahi, bacak veya pelvise yap�lan herhangi bir | Bu durumlarda bant/tablet/halkan�n b�rak�lmas� (elektif cerrahi durumunda en |
cerrahi m�dahale, n�ro�ir�rji veya maj�r travma.
Not: �zellikle di�er risk fakt�rleri de mevcutsa, 4 saatten uzun havayolu seyahati dahil ge�ici hareketsiz kalma, VTE i�in bir risk fakt�r� olabilir. | az�ndan 4 hafta �nceden b�rak�lmas�) ve tekrar hareketlilik sa�land�ktan 2 hafta sonras�na kadar ba�lanmamas� tavsiye edilir. �stenmeyen gebeli�i engellemek i�in ba�ka bir do�um kontrol y�ntemi kullan�lmal�d�r.
DESOLETT �nceden b�rak�lmad�ysa antitrombotik tedavi d���n�lmelidir. |
Pozitif aile �yk�s� (karde� veya ebeveynlerde VTE, �zellikle 50 ya� �ncesi gibi erken ya�larda) | Kal�tsal predispozisyondan ��pheleniliyorsa, KHK kullan�m�na karar vermeden �nce kad�n bir uzmana y�nlendirilmelidir. |
VTE ile ili�kili di�er t�bbi durumlar | Kanser, sistemik lupus eritematozus, hemolitik �remik sendrom, kronik inflamatuar barsak hastal��� (Crohn hastal��� veya �lseratif kolit) ve orak h�cre anemisi |
Artan ya� | �zellikle 35 ya� �zeri |
Ven�z trombozun ba�lang�c� veya progresyonunda varikoz venlerin veya s�perfisyal tromboflebitin olas� rol� hakk�nda fikir birli�i yoktur.
Hamilelik s�ras�nda, �zellikle do�um sonras� 6 haftal�k d�nemde, artm�� tromboembolizm riski
g�z �n�nde bulundurulmal�d�r (gebelik ve laktasyon bilgileri i�in bkz. b�l�m 4.6).
VTE'nin semptomlar� (derin ven trombozu ve pulmoner emboli)
Kad�nlara semptomlar g�r�ld��� takdirde acil t�bbi yard�ma ba�vurmalar� ve ilgili sa�l�k �al��an�na KHK kulland�klar�n� belirtmeleri gerekti�i s�ylenmelidir.
Derin ven trombozunun (DVT) semptomlar� a�a��dakileri i�erir:
Her iki bacak ve/veya ayakta ya da bacakta bir vende �i�me;
Bacakta, yaln�zca aya�a kalkarken veya y�r�rken hissedilebilen a�r� veya hassasiyet;
Di�er durumlar
Hipertrigliseridemisi veya bu rahats�zl��a ili�kin bir aile �yk�s� olan kad�nlarda, KHK
kullan�ld���nda pankreatit riskinde art�� olabilmektedir.
Eksojen �strojenler, kal�tsal ve edinilmi� anjiyo�dem semptomlar�n� ind�kleyebilir veya
�iddetlendirebilir.
KHK kullanan bir�ok kad�n�n kan bas�nc�nda k���k art��lar g�r�lmekle birlikte, klinik a��dan anlaml� art��lar nadirdir. KHK kullan�m� ile klinik hipertansiyon aras�nda herhangi bir ili�ki saptanmam��t�r. Fakat KHK kullan�m� s�ras�nda klinik a��dan anlaml�, kal�c� bir hipertansiyon geli�irse, doktorun KHK kullan�m�n� kesmesi ve hipertansiyona y�nelik tedavi uygulamas� tedbirli bir davran�� olacakt�r. Uygun oldu�u d���n�ld���nde, antihipertansif tedavi ile normal kan bas�nc� de�erlerine ula��ld�ktan sonra KHK kullan�m�na tekrar ba�lanabilir.
A�a��da s�ralanan durumlar�n hem gebelik hem de KHK kullan�m� ile birlikte olu�tu�u veya k�t�le�ti�i bildirilmi�tir, ancak KHK kullan�m� ile ba�lant�s� kan�tlanmam��t�r: Kolestaza ba�l� sar�l�k ve/veya ka��nt�; safra ta�� olu�umu; porfiri; sistemik lupus eritematozus; hemolitik-�remik sendromu; Sydenham's kore; herpes gestationis; otoskleroza ba�l� i�itme kayb�.
KHK'lerin periferik ins�lin direnci ve glukoz tolerans� �zerinde bir etkisi olmakla birlikte, KHK kullanan diyabetik hastalar�n tedavi rejiminin de�i�tirilmesi gerekti�ine dair hi�bir kan�t mevcut de�ildir. Fakat diyabetik kad�nlar KHK kullan�rken dikkatli bir �ekilde g�zlem alt�nda tutulmal�d�rlar.
Karaci�er fonksiyonunun akut veya kronik rahats�zl�klar�, kararaci�er fonksiyonu normale d�nene kadar KHK kullan�m�n�n kesilmesini gerekterebilir. Daha �nceden gebelik s�ras�nda ya da seks hormonlar�n�n kullan�m� s�ras�nda meydana gelen kolestatik sar�l���n tekrarlanmas� KHK kullan�m�n�n durdurulmas�n� gerektirir.
�lseratif kolit ve Crohn hastal���, KHK kullan�m� ile ili�kilendirilmi�tir.
�zellikle kloazma gravidarum (gebelik maskesi) �yk�s� olan kad�nlarda nadiren kloazma olu�abilir. Kloazmaya e�ilimi olan kad�nlar, bu ilac� kullan�rken g�ne� veya ultraviyole ���nlar�na maruz kalmamaya �zen g�stermelidirler.
4.5. Di�er t�bbi �r�nler ile etkile�imler ve di�er etkile�im �ekilleri
Etkile�imler:
Oral kontraseptifler ile di�er medikal �r�nler aras�ndaki etkile�imler ani kanamalara ve/veya yetersiz kontrasepsiyona yol a�abilir. A�a��daki etkile�imler bildirilmi�tir:
Karaci�er metabolizmas�:
Seks hormonlar�n�n plazma konsantrasyonlar�n� d���r�c� artm�� klerense sebep olan mikrozomal enzimleri, �zellikle sitokrom P450 enzimlerini (CYP) ind�kleyen medikal veya bitkisel �r�nlerle etkile�imler ortaya ��kabilir ve DESOLETT de dahil, kombine oral kontraseptiflerin etkilili�ini azaltabilir. Bu �r�nler, fenitoin, fenobarbital, primidon, bosentan, karbamazepin, rifampisin, rifabutin ve muhtemelen de okskarbazepin, modafinil, topiramat, felbamat, griseofulvin, baz� HIV proteaz inhibit�rleri (�rn., ritonavir) ve nonn�kleosit revers transkriptaz inhibit�rleri (�rn. efavirenz) ve bitkisel bir ila� olan St. John's wort (Sar� Kantaron Otu) i�eren �r�nleri i�erir.
Enzim ind�ksiyonu tedaviden birka� g�n sonra ger�ekle�ebilir. Maksimal enzim ind�ksiyonu genellikle birka� hafta i�inde g�zlemlenir. �la� tedavisinin bitiminden sonra enzim ind�ksiyonu 28 g�n kadar s�rebilir.
Yukar�da bahsedilen herhangi bir hepatik enzim-ind�kleyici medikal veya bitkisel �r�n kullanan kad�nlara DESOLETT'in etkilili�in azalabilece�i konusunda bilgi verilmelidir. Hepatik enzim-ind�kleyici medikal �r�n�n kullan�lmas� s�ras�nda ve hepatik enzim-ind�kleyici medikal �r�n�n tedavi bitiminden sonra 28 g�n i�in, DESOLETT'e ek olarak bir bariyer do�um kontrol y�ntemi kullan�lmal�d�r.
E�er, birlikte ila� kullan�m�na mevcut KHK paketindeki tabletlerin biti�inden sonra ba�lan�rsa, bir sonraki KHK paketine genellikle yap�lan, tabletin al�nmad��� aral�k yap�lmadan ba�lanmal�d�r.
Enzim ind�kleyici medikal �r�nlerle uzun s�reli terapi alan kad�nlar i�in, enzim ind�kleyici medikal �r�nlerden etkilenmeyen alternatif bir kontrasepsiyon y�ntemi d���n�lmelidir.
Hormonal kontraseptifler, HIV proteaz inhibit�rleri (�rn., Nelfinavir) ve non-n�kleozid revers transkriptaz inhibit�rlerinin (�rn., Nevirapin) bir�ok kombinasyonu ve / veya Hepatit C vir�s� (HCV) t�bbi �r�nleri (�rn., Boceprevir, telaprevir) ile kombinasyonlar� birlikte uyguland���nda, etonogestrel, desogestrelin aktif metaboliti veya �strojenler dahil olmak �zere progestinlerin plazma konsantrasyonlar�n� art�rabilir veya azaltabilir. Bu de�i�ikliklerin net etkisi, baz� vakalarda klinik olarak ili�kili olabilir.
-G��l� CYP3A4 inhibit�rlerinin (�rn., ketokonazol, itrakonazol, klaritromisin) veya orta
dereceli CYP3A4 inhibit�rlerinin (�rn., flukonazol, diltiazem, eritromisin) birlikte
uygulanmas� desogestrelin aktif metaboliti etonogestrel dahil �strojen veya progesteron serum konsantrasyonlar�n� y�kseltebilir.
-Oral kontraseptifler di�er ila�lar�n metabolizmas� ile etkile�ebilir. Buna g�re, plazma ve doku konsantrasyonlar� hem artabilir (�rn. siklosporin) hem de azalabilir (�rn. lamotrigin).
Not: Potansiyel etkile�imleri tan�mlamak i�in e� zamanl� kullan�lan ila�lar�n �r�n bilgisine
ba�vurulmal�d�r.
�zel pop�lasyonlara ili�kin ek bilgiler:
Pediyatrik pop�lasyon:
18 ya��ndan k���k adolesanlarda etkililik ve g�venlili�e ili�kin hi�bir klinik veri mevcut de�ildir.
Farmakodinamik etkile�imler
Ribavirin veya glekaprevir / pibrentasvir i�eren veya i�ermeyen, ombitasvir / paritaprevir / ritonavir ve dasabuvir i�eren t�bbi �r�nlerle e� zamanl� kullan�m, ALT y�kselme riskini art�rabilir (bkz. B�l�m 4.3 ve 4.4). Bu nedenle, DESOLETT kullan�c�lar�, bu kombinasyon ila� rejimiyle tedaviye ba�lamadan �nce alternatif bir kontrasepsiyon y�ntemine (�rn., sadece progestojen kontrasepsiyon veya hormonal olmayan y�ntemler) ge�melidir. DESOLETT, bu kombinasyon ila� rejimi ile tedavinin tamamlanmas�ndan 2 hafta sonra yeniden ba�lat�labilir.
Laboratuvar Testleri:
Kontraseptif steroidlerin kullan�lmas�, karaci�er, tiroid, adrenal ve renal fonksiyonlara ili�kin biyokimyasal parametreleri, kortikosteroid ba�lay�c� glob�lin ve lipit/lipoprotein fransiyonlar� gibi ta��y�c� proteinlerin plazma d�zeylerini, karbohidrat metabolizmas� parametrelerini ile koag�lasyon ve fibrinoliz parametreleride dahil olmak �zere baz� laboratuvar tetkiklerinin sonu�lar�n� etkileyebilmektedir. De�i�iklikler genellikle normal laboratuvar s�n�rlar� i�erisinde kal�r.
4.6. Gebelik ve laktasyon
Gebelik kategorisi X'tir.
�ocuk do�urma potansiyeli bulunan kad�nlar/Do�um kontrol� (Kontrasepsiyon)
DESOLETT, do�um kontrol� amac�yla kullan�lmaktad�r.
Gebelik d�nemi
DESOLETT'in gebelik s�resince kullan�m� endike de�ildir. DESOLETT kullan�m� s�ras�nda
gebelik ger�ekle�irse kullan�ma devam edilmemelidir.
Ancak �o�u epidemiyolojik �al��malar, ne gebelik �ncesinde KHK kullanan kad�nlar�n �ocuklar�nda do�um kusurlar�nda bir y�kselme, ne de KHK'lerin erken gebelik d�neminde yanl��l�kla al�nmas� neticesinde herhangi bir teratojenik etki g�r�lmedi�ini ortaya koymu�tur.
Do�um sonras� d�nemde DESOLETT kullan�m�na tekrar ba�lan�rken VTE riskinin art��� g�z �n�nde bulundurulmal�d�r (bkz. B�l�m 4.2 ve 4.4).
Laktasyon d�nemi
KHK'ler, anne s�t�n�n kalitesini azaltt�klar� ve bile�imini de�i�tirdikleri i�in emzirme etkilenebilir. Dolay�s�yla KHK kullan�m� genel olarak bebe�in tamamen s�tten kesilmesine
kadar �nerilmemektedir. S�t ile birlikte k���k miktarlarda kontraseptif steroidlerin ve/veya bunlar�n metabolitlerinin salg�lanmas� m�mk�n olmakla birlikte, bu durumun bebe�in sa�l��� �zerinde olumsuz bir etkiye sahip oldu�una ili�kin herhangi bir kan�t mevcut de�ildir.
�reme yetene�i/Fertilite
Bu t�bbi �r�n�n endikasyonu kontrasepsiyon oldu�u i�in bu ba�l�k ge�erli de�ildir.
4.7. Ara� ve makine kullan�m� �zerindeki etkiler
Ara� ve makine kullan�m� �zerine herhangi bir etkisi g�zlenmemi�tir.
4.8. �stenmeyen etkiler
Se�ilmi� advers reaksiyonlar�n tan�m�
T�m KHK'lardaki gibi, �zellikle kullan�m�n ilk aylar�nda, vajinal kanama d�zeninde de�i�iklik g�r�lebilir. Bu de�i�iklikler kanama s�kl���nda (hi�, az, daha s�k veya devaml�), yo�unlu�unda (azalan veya artan) ve s�resindeki de�i�iklikleri i�erebilir.
KHK kullanan kad�nlarda, miyokard infarkt�s�, inme, ge�ici iskemik atak, ven�z tromboz ve pulmoner emboli dahil, arteriyel ve ven�z trombotik ve tromboembolik olay riskinde art�� g�zlenmi�tir; b�l�m 4.4'te daha detayl� olarak bunlardan bahsedilmektedir.
DESOLETT veya KHK kullan�c�lar�nda genel olarak raporlanm�� muhtemelen ba�lant�l� istenmeyen etkiler a�a��da listelenmi�tir. �stenmeyen olaylar a�a��da sistem organ s�n�f�na g�re listelenmi�tir. S�kl�klar �u �ekilde tan�mlanm��t�r: �ok yayg�n (≥1/10); yayg�n (≥1/100 ila
≤1/10); yayg�n olmayan (≥1/1.000 ila ≤1/100); seyrek (≥1/10.000 ila ≤1/1.000); �ok seyrek
(≤1/10.000); bilinmiyor (eldeki verilerden hareketle tahmin edilemiyor).
Ba����kl�k sistemi hastal�klar�:
Seyrek: Hipersensitivite
Bilinmiyor: Kal�tsal ve edinilmi� anjiyo�dem semptomlar�n�n �iddetlenmesi
Metabolizma ve beslenme hastal�klar�:
Yayg�n olmayan: S�v� tutulumu
Psikiyatrik hastal�klar:
Yayg�n: Depresif ruh hali, de�i�ken ruh hali
Yayg�n olmayan: Libido azalmas� Seyrek: Libido art���
Sinir sistemi hastal�klar�:
Yayg�n: Ba� a�r�s� Yayg�n olmayan: Migren
G�z hastal�klar�:
Seyrek: Kontakt lens intolerans�
Vask�ler hastal�klar:
Seyrek: Ven�z tromboembolizm, arteriyel tromboembolizm
Gastrointestinal hastal�klar: Yayg�n: Bulant�, kar�nda a�r� Yayg�n olmayan: Kusma, diyare
Deri ve deri alt� doku hastal�klar�:
Yayg�n olmayan: D�k�nt�, �rtiker
Seyrek: Eritema nodosum, eritema multiforme
�reme sistemi ve meme hastal�klar�:
Yayg�n: Memede a�r�, meme hassasiyeti Yayg�n olmayan: Memede b�y�me Seyrek: Vajinal ak�nt�, memede ak�nt�
Ara�t�rmalar:
Yayg�n: Kiloda art�� Seyrek: Kiloda azalma
��pheli advers reaksiyonlar�n raporlanmas�
Ruhsatland�rma sonras� ��pheli ila� advers reaksiyonlar�n�n raporlanmas� b�y�k �nem ta��maktad�r. Raporlama yap�lmas�, ilac�n yarar/risk dengesinin s�rekli olarak izlenmesine olanak sa�lar. Sa�l�k mesle�i mensuplar�n�n herhangi bir ��pheli advers reaksiyonu T�rkiye Farmakovijilans Merkezi (T�FAM)'ne bildirmeleri gerekmektedir (www.titck.gov.tr; e- posta:tufam@titck.gov.tr; tel: 0 800 314 00 08; faks: 0 312 218 35 99)
4.9. Doz a��m� ve tedavisi
Doz a��m�na ba�l� ciddi zararl� etkilere ili�kin herhangi bir rapor mevcut de�ildir. Bu duruma ba�l� olarak olu�abilen semptomlar �unlard�r: Bulant�, kusma ve hafif bir vajinal kanama. Antidot mevcut de�ildir ve semptomatik tedavi uygulanmal�d�r.
5. FARMAKOLOJ�K �ZELL�KLER
Farmokodinamik �zellikler
Farmakoterap�tik grup: Progestojen ve �strojen kombinasyonlar� (Sabit kombinasyonlar) ATC kodu: G03AA09
DESOLETT 150 mikrogram desogestrel ile 30 mikrogram etinilestradiol i�eren bir oral
kontraseptif kombinasyonudur.
Etinil estradiol iyi bilinen bir sentetik �strojendir.
Desogestrel sentetik bir progestojendir. Oral uygulamadan sonra, ov�lasyonu g��l� bi�imde bask�lay�c� aktivite ve g��l� bir progestasyonel ve anti-�strojenik aktivite g�sterir. �strojenik aktiviteye sahip de�ildir. Androjenik/anabolizan aktivitesi zay�ft�r.
Pediyatrik pop�lasyon:
18 ya� alt� adolesanlarda etkililik ve g�venlilikle ilgili klinik veri yoktur.
5.2. Farmakokinetik �zellikler
Genel �zelliklerDesogestrel
Emilim:
Oral olarak uygulanan desogestrel h�zl� ve tam olarak emilmekte ve etonogestrele d�n��t�r�lmektedir. Doruk serum konsantrasyonlar�na yakla��k 1,5 saat i�erisinde ula��l�r. Biyoyararlan�m % 62-81 aras�ndad�r.
Da��l�m:
Etonogestrel serum alb�minine ve seks hormon ba�lay�c� glob�line (SHBG) ba�lan�r. Toplam serum ila� konsantrasyonunun yaln�zca % 2-4'� serbest steroid olarak bulunmaktad�r ve % 40- 70'i spesifik olarak SHBG'ye ba�l�d�r. SHBG d�zeyinde etinilestradiol nedenli art��, �teki serum proteinlerinin da��l�m�n� etkilemekte ve SHBG'ye ba�l� fraksiyonu art�r�p alb�mine ba�l� fraksiyonu azalt�r. Desogestrelin sanal da��l�m hacmi 1,5 L/kg d�zeyindedir.
Biyotransformasyon:
Etonogestrel, sitokrom P450 3A4 dahil olmak �zere steroid metabolizmas�n�n bilinen yollar� �zerinden tamamen metabolize olmaktad�r. Serumdan metabolik klerens oran� yakla��k 2 mL/dak/kg d�zeyindedir. Birlikte uygulanan etinilestradiol ile herhangi bir etkile�im saptanmam��t�r.
Eliminasyon:
Etonogestrel serum seviyesi iki fazda azalmaktad�r. Terminal dispozisyon faz�, yakla��k 30 saatlik bir yar�lanma �mr� ile karakterizedir. Desogestrel ve bunun metabolitleri, yakla��k 6:4'l�k bir idrar / safra oran� ile at�lmaktad�r.
Do�rusall�k/Do�rusal olmayan durum:
Etonogestrel farmakokineti�i, etinilestradiol taraf�ndan �� kat�na ��kar�lan SHBG d�zeyinin etkisi alt�ndad�r. G�nl�k oral al�m� takiben, ila� serum d�zeyleri iki ile �� kat aras�nda art�� g�stermekte ve uygulama siklusunun ikinci yar�s� i�erisinde dura�an durum ko�ullar�na ula�maktad�r.
Etinilestradiol
Emilim:
Oral yoldan uygulanan etinilestradiol h�zl� ve tam olarak emilmektedir. Doruk serum konsantrasyonlar�na 1-2 saat i�erisinde ula��lmaktad�r. Presistemik konj�gasyon ve ilk ge�i� metabolizmas� sonucunda mutlak biyoyararlan�m yakla��k % 60 d�zeyindedir.
Da��l�m:
Etinilestradiol serum alb�minine y�ksek d�zeyde, fakat spesifik olmayan bi�imde ba�lanmaktad�r (yakla��k % 98,5) ve serumdaki SHBG konsantrasyonlar�nda art��a yol a�maktad�r. Yakla��k 5 L/kg d�zeyinde bir g�r�n�r da��l�m hacmi saptanm��t�r.
Biyotransformasyon:
Etinilestradiol, ince ba��rsak mukozas�nda ve karaci�erde presistemik konj�gasyona u�ramaktad�r. Etinilestradiol birincil olarak aromatik hidroksilasyon ile metabolize olmakla birlikte bir�ok hidroksillenmi� ve metillenmi� metabolitler olu�makta ve bunlar serbest metabolit veya glukuronidler ve s�lfatlarla konj�gatlar �eklinde bulunmaktad�r. Metabolik klerens h�z� yakla��k 5 mL/dak/kg d�zeyindedir.
Eliminasyon:
Etinilestradiol serum d�zeyleri iki fazda azalmaktad�r; terminal dispozisyon faz� yakla��k 24 saatlik bir yar�lanma �mr� ile karakterizedir. De�i�memi� ila� at�lmamakta, etinilestradiol metabolitleri 4:6 oran�nda idrar ve safra ile at�lmaktad�r. Metabolit at�l�m�n�n yar�lanma �mr� yakla��k 1 g�nd�r.
Do�rusall�k/Do�rusal olmayan durum:
Kararl� durum konsantrasyonlar�na, tek doza k�yasla serum ila� d�zeylerinin % 30-40 oran�nda daha y�ksek olmas� halinde 3-4 g�n sonra ula��lmaktad�r.
5.3. Klinik �ncesi g�venlilik verileri
5.3. Klinik �ncesi g�venlilik verileri
Ancak, seks steroidlerinin belli hormonal doku ve t�m�rlerin b�y�mesini artt�rd��� unutulmamal�d�r.
6. FARMAS�T�K �ZELL�KLER
6.1. Yard�mc� maddelerin listesi
All-rac-α-Tokoferol Patates ni�astas� Silika; koloidal susuz Povidon
Stearik asit
Laktoz monohidrat (ineklerden elde edilir) Saf su
Aseton
6.2. Ge�imsizlikler
Yoktur.
6.3. Raf �mr�
36 ay.
6.4. Saklamaya y�nelik �zel tedbirler
25°C alt�ndaki oda s�cakl���nda saklay�n�z. I��k ve rutubetten koruyunuz.
6.5. Ambalaj�n niteli�i ve i�eri�i
Al�minyum ile kapl� sa�e i�inde PVC/al�minyum blister. 21 beyaz tablet i�eren blister.
6.6. Be�eri t�bbi �r�nden arta kalan maddelerin imhas� ve di�er �zel �nlemler
�zel bir gereklilik yoktur.
Kullan�lmam�� olan �r�nler ya da at�k materyaller “T�bbi At�klar�n Kontrol� Y�netmeli�i” ve “Ambalaj At�klar� Kontrol� Y�netmeli�i”ne uygun olarak imha edilmelidir.
 Artrit
Artrit, olduk�a yayg�n bir hastal�kt�r ancak iyi anla��lamam��t�r. Asl�nda �artrit� tek bir hastal���n ad� de�ildir; eklem a�r�s� veya eklem hastal�klar�n� adland�rman�n gayri resmi yoludur.
Artrit
Artrit, olduk�a yayg�n bir hastal�kt�r ancak iyi anla��lamam��t�r. Asl�nda �artrit� tek bir hastal���n ad� de�ildir; eklem a�r�s� veya eklem hastal�klar�n� adland�rman�n gayri resmi yoludur. |
 G�da Alerjisi
Her y�l milyonlarca insan yiyeceklere alerji g�steriyor.
G�da Alerjisi
Her y�l milyonlarca insan yiyeceklere alerji g�steriyor. |
�LA� E�DE�ERLER�
| E�de�er �la� Ad� | Barkodu | �la� Fiyat� |
|---|---|---|
| MYRALON | 8683280337282 | 580.42TL |
| Di�er E�de�er �la�lar |
 |
Y�ksek Tansiyon Hipertansiyon s�rekli anormal derecede y�ksek olan kan bas�nc�d�r. Tansiyon atardamarlar�n�zdaki kan�n bas�nc�d�r. |
 |
Tiroid Kanseri En s�k g�r�len tiroid kanseri t�r� olan papiller tiroid kanseri, t�m tiroid kanserlerinin yakla��k %70'ini olu�turur. |
 |
Diyabet Hastal��� Diyabet, ins�lin hormonu ile ilgili problemlerden kaynaklanan bir hastal�kt�r. |
�LA� GENEL B�LG�LER�
Organon Turkey �la�lar� Ltd. �ti.
| Sat�� Fiyat� | TL |
| �nceki Sat�� Fiyat� | |
| Original / Jenerik | Original �la� |
| Re�ete Durumu | Normal Re�eteli bir ila�d�r. |
| Barkodu | 683280337077 |
| Etkin Madde | Desogestrel + Etinilestradiol |
| ATC Kodu | G03AA09 |
| Birim Miktar | 0,15+0,03 |
| Birim Cinsi | MG |
| Ambalaj Miktar� | 21 |
| �rogenital Sistem ve Cinsiyet Hormonlar� > Sistemik Hormonal Gebeli�i �nleyici �la�lar > Desogestrel + etinilestradiol |
| �thal ( ref. �lke : Fransa ) ve Be�eri bir ila�d�r. |