CANCIDAS 50 mg 1 flakon Klinik �zellikler
{ Kaspofungin Asetat }
4. KL�N�K �ZELL�KLER
4.1. Terap�tik endikasyonlar
CANCIDAS eri�kinlerde ve pediyatrik hastalarda (3 ayl�ktan b�y�k) a�a��daki durumlar i�in endikedir:
Ate�li, n�tropenik hastalarda ku�kulan�lan fungal enfeksiyonlar�n ampirik tedavisi,
4.2. Pozoloji ve uygulama �ekli
Pozoloji/Uygulama s�kl��� ve s�resi:Eri�kin hastalarda (18 ya� ve �zeri) �nerilen dozaj
Klasik doz g�nde bir kez 50 mg'dir (�o�u endikasyonda 70 mg y�kleme dozunun ard�ndan uygulan�r). G�nde 150 mg dozunun g�venlili�i ve etkilili�i (tedavi s�resi: 1-51 g�n; ortalama: 14 g�n) kandidemi ve di�er Candida enfeksiyonlar� olan 100 eri�kin hastada incelenmi�tir. Bu y�ksek dozda CANCIDAS'�n etkilili�i CANCIDAS'�n g�nde 50 mg dozunun etkilili�inden anlaml� olarak daha iyi de�ildi. CANCIDAS'�n endike oldu�u di�er eri�kin hastalarda g�nde 50 mg'dan y�ksek dozlar�n etkilili�i bilinmemektedir (bkz. b�l�m 5.2).
Ampirik Tedavi
1. g�nde tekli 70 mg y�kleme dozu ve ard�ndan g�nde 50 mg uygulanmal�d�r. Tedavi s�resi hastan�n klinik yan�t�na dayanmal�d�r. N�tropeni iyile�inceye kadar ampirik tedaviye devam edilmelidir. Fungal enfeksiyon saptanan hastalar en az 14 g�n tedavi edilmelidir; tedaviye hem
n�tropeni hem de klinik semptomlar ortadan kalkt�ktan sonra en az 7 g�n devam edilmelidir. 50 mg dozu iyi tolere edilir, fakat yeterli klinik yan�t sa�lanamazsa g�nl�k doz 70 mg'a ��kar�labilir.
Kandidemi ve di�er candida enfeksiyonlar�
1. g�nde tekli 70 mg y�kleme dozu ve ard�ndan g�nde 50 mg uygulanmal�d�r. Tedavi s�resi hastan�n klinik ve mikrobiyolojik yan�t�na g�re belirlenmelidir. Genel olarak, antifungal tedavi son pozitif k�lt�rden sonra en az 14 g�n devam etmelidir. N�tropenisi devam eden hastalarda n�tropeni iyile�inceye kadar daha uzun tedavi s�resi gerekebilir.
�zofajiyal kandidiyazis
Doz, semptomlar ortadan kalkt�ktan sonra 7-14 g�n s�reyle g�nde bir kez 50 mg'dir. Bu endikasyon i�in 70 mg y�kleme dozu incelenmemi�tir. HIV enfeksiyonlu hastalarda orofarenjiyal kandidiyazisin relaps riski mevcut oldu�undan, supresif oral tedavi d���n�lebilir (bkz. b�l�m 5.2).
�nvazif aspergilloz
1. g�nde tekli 70 mg y�kleme dozu ve ard�ndan g�nde 50 mg uygulanmal�d�r. Tedavi s�resi hastada altta yatan hastal���n �iddetine, imm�n supresyondan sonra iyile�meye ve klinik yan�ta ba�l� olarak belirlenmelidir.
�la� klerens ind�kleyicilerini e� zamanl� alan hastalar
Rifampin alan eri�kin hastalar g�nde 70 mg CANCIDAS almal�d�r. Nevirapin, efavirenz, karbamazepin, deksametazon veya fenitoin alan hastalarda CANCIDAS'�n g�nl�k dozunun 70 mg'ye ��kar�lmas� gerekebilir (bkz. b�l�m 4.5).
Tedavi s�resi, eri�kinlerde her bir endikasyon i�in tarif edilen �ekilde, endikasyona g�re belirlenmelidir (bkz. b�l�m 4.2). G�nde 50 mg/mdozu iyi tolere edilir; fakat yeterli klin ik yan�t sa�lamazsa, g�nl�k doz g�nde 70 mg/m'ye y�kseltilebilir (70 mg a��lmamal�d�r).
Uygulama �ekli:
Haz�rlama ve seyreltme i�lemlerinden sonra, CANCIDAS yakla��k 1 saat s�ren, yava� intraven�z
(IV) inf�zyonla uygulanmal�d�r. Haz�rlama talimatlar� i�in bkz. b�l�m 6.6.
CANCIDAS IV bolus �eklinde uygulanmamal�d�r.
Hem 70 mg hem de 50 mg flakonlar mevcuttur. Kaspofungin tekli g�nl�k inf�zyon �eklinde verilmelidir.
�zel pop�lasyonlara ili�kin ek bilgiler B�brek yetmezli�i
B�brek yetmezli�i olan hastalarda doz ayarlamas� gerekmez (bkz. b�l�m 5.2).
Karaci�er yetmezli�i
Hafif karaci�er yetmezli�i olan eri�kin hastalarda (Child-Pugh skoru 5 - 6) dozaj ayarlamas� gerekmez. Orta derecede karaci�er yetmezli�i olan hastalarda (Child-Pugh skoru 7- 9), farmakokinetik verilere dayanarak g�nde 35 mg CANCIDAS �nerilir. Ba�lang��ta 1. g�nde 70 mg y�kleme dozu uygulanmal�d�r. Ciddi karaci�er yetmezli�i olan eri�kin hastalarda (Child-Pugh skoru >9) ve herhangi bir derecede karaci�er yetmezli�i olan pediyatrik hastalarda klinik deneyim yoktur.
Pediyatrik pop�lasyon
CANCIDAS'�n yeni do�anlarda ve 12 ay alt� �ocuklardaki klinik �al��malarda g�venli�i ve etkilili�i yeterli oranda �al���lmam��t�r. Bu ya� grubuna uygulan�rken dikkatli olunmal�d�r. G�nde
25 mg/mCANCIDAS'�n yeni do�anlarda ve bebeklerde (�� aydan k���k) ve g�nde 50 mg/mCANCIDAS'�n �ocuklarda (3-11 ay) kullan�m�yla ilgili s�n�rl� veri vard�r (bkz. b�l�m 5.2).
Pediyatrik hastalarda (3 ay-17 ya� aras�) �nerilen dozaj
T�m endikasyonlarda 1. g�nde tekli 70 mg/my�kleme dozu ve ard�ndan g�nde 50 mg/muygulanmal�d�r. E�er g�nde 50 mg/mdozu iyi tolere edilir; fakat yeterli klinik yan�t� sa�lamaz sa, doz g�nde 70 mg/m'ye ��kar�labilir (ger�ek doz g�nde 70 mg'yi a�mamal�d�r. Hastan�n hesaplanan dozu ne olursa olsun, maksimum y�kleme dozu ve g�nl�k idame dozu olan 70 mg'� a�mamal�d�r. Pediyatrik hastalarda (3 ay-17 ya� aras�) dozaj hastan�n a�a��daki form�lle hesaplanan V�cut Y�zey Alan�na (VYA) g�re belirlenmelidir (bkz. Mosteller Formula- Ref: Mosteller RD: Simplified Calculation of Body Surface Area. N Engl J Med 1987 Oct 22;317(17 ): 1098 (letter)).
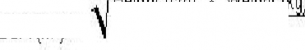
VYA(m) =
Boy (cm) x Kilo (kg) 3600
Hastan�n VYA's� hesapland�ktan sonra, miligram cinsinden y�kleme dozu VYA (m) x 70 mg/m �arp�m�yla hesaplanmal�d�r. Miligram cinsinden idame dozu VYA (m) x 50 mg/m�arp�m�yla hesaplanmal�d�r.
CANCIDAS pediyatrik hastalara ila� klirensinin ind�kleyicileriyle (rifampin, nevirapin, efavirenz, karbamazepin, deksametazon veya fenitoin) e� zamanl� olarak uygulan�rken CANCIDAS'�n g�nde 70 mg/mdozu d���n�lmelidir (70 mg a��lmamal�d�r) (bkz. b�l�m 4.2).
Geriyatrik pop�lasyon
Ya�l� hastalarda (65 ya� ve �zeri) e�ri alt�nda kalan alan (EAA) yakla��k %30 artar. Ancak sistematik doz ayarlamas� gerekmez. 65 ya� ve �zeri hastalarda tedavi deneyimi s�n�rl�d�r (bkz. b�l�m 5.2).
4.3. Kontrendikasyonlar
4.4. �zel kullan�m uyar�lar� ve �nlemleri
Kaspofungin uygulamas� s�ras�nda anaflaksi rapor edilmi�tir. Anaflaksi ortaya ��karsa kaspofungin kesilmeli ve uygun tedavi uygulanmal�d�r. D�k�nt�, y�zde �i�lik, anjiyo�dem, ka��nt�, s�cakl�k hissi veya bronkospazm gibi muhtemelen histamin arac�l� istenmeyen olaylar bildirilmi�tir; bu olaylar ilac�n kesilmesini ve/veya uygun tedavinin uygulanmas�n� gerektirebilir.
S�n�rl� veriler daha az yayg�n olan Candida d��� mayalar ve Aspergillus d��� k�flere kar�� kaspofunginin etkili olmad���n� g�stermektedir. Kaspofunginin bu fungal patojenlere kar�� etkilili�i belgelenmemi�tir.
Kaspofunginin siklosporin ile e� zamanl� uygulanmas� sa�l�kl� yeti�kin g�n�ll�lerde ve yeti�kin hastalarda de�erlendirilmi�tir.
Siklosporinin 3 mg/kg'l�k iki dozu ile birlikte kaspofungin alan baz� sa�l�kl� yeti�kin g�n�ll�lerin alanin transaminaz (ALT) ve aspartat transaminaz (AST) d�zeylerinde normalin �st s�n�r�n�n (ULN) 3 kat� ge�ici y�kselmeler g�r�lm�� ve tedavinin kesilmesiyle bu art��lar normale d�nm��t�r. Pazarlama sonras� d�nemde kaspofungin ve siklosporin ile 1-290 g�n aras�nda de�i�en s�relerle (medyan 17,5 g�n) tedavi edilen 40 hastan�n incelendi�i geriye d�n�k bir �al��mada ciddi
hi�bir hepatik istenmeyen olay kaydedilmemi�tir. Bu veriler siklosporin alan hastalarda kaspofunginin potansiyel yarar� potansiyel riskten fazla oldu�unda kullan�labilece�ini ortaya koymaktad�r. Kaspofungin ve siklosporin e� zamanl� uyguland���nda karaci�er enzimlerinin yak�ndan takip edilmesi gerekti�i g�z �n�ne al�nmal�d�r.
Hafif ve orta derecede karaci�er bozuklu�u olan yeti�kin hastalarda EAA s�ras�yla yakla��k % 20 ve %75 artar. Orta derecede karaci�er bozuklu�u olan yeti�kinlerde g�nl�k dozun 35 mg'ye d���r�lmesi tavsiye edilir. �iddetli karaci�er bozuklu�u olan yeti�kinlere veya herhangi bir derecede karaci�er bozuklu�u olan pediyatrik hastalara ili�kin klinik deneyim mevcut de�ildir. Bu hastalarda orta derecede karaci�er bozuklu�undakine k�yasla daha y�ksek maruz kal�m beklenir ve kaspofungin dikkatli kullan�lmal�d�r (bkz. b�l�m 4.2 ve 5.2).
Kaspofungin ile tedavi edilen sa�l�kl� g�n�ll�lerde ve yeti�kin ve pediyatrik hastalarda karaci�er fonksiyon testlerinde laboratuvar anormallikleri g�zlenmi�tir. Kaspofungin ile e� zamanl� �oklu ila� tedavisi g�ren ve altta yatan ciddi durumlar� olan baz� yeti�kin ve pediyatrik hastalarda, klinik olarak belirgin hepatik disfonksiyon, hepatit ve karaci�er yetmezli�i vakalar� rapor edilmi�tir ancak kaspofungin ile nedensel ili�ki ortaya konmam��t�r. Kaspofungin tedavisi s�ras�nda karaci�er fonksiyon testi anormalli�i geli�en hastalar, k�t�le�en hepatik fonksiyonun bulgular� y�n�nden izlenmeli ve kaspofungin tedavisine devam edilmesinin risk/yarar oran� tekrar de�erlendirilmelidir.
Kaspofunginin pazarlama sonras� d�nemde kullan�m�yla Stevens-Johnson sendromu (SJS) ve toksik epidermal nekroliz (TEN) vakalar� bildirilmi�tir. Alerjik deri reaksiyonu hikayesi olan hastalarda dikkatli olunmal�d�r (bkz. b�l�m 4.8).
Yard�mc� maddeler
Bu t�bbi �r�n her flakonunda 1 mmol (23 mg)'dan daha az sodyum ihtiva eder; yani esas�nda “sodyum i�ermez”.
Sukroz: Bu t�bbi �r�n her flakonunda 39 mg sukroz i�erir. Bu durum, diyabet hastalar�nda g�z �n�nde bulundurulmal�d�r.
4.5. Di�er t�bbi �r�nler ile etkile�imler ve di�er etkile�im �ekilleri
�n vitro �al��malar kaspofunginin sitokrom P450 (CYP) sistemine ait herhangi bir enzimin inhibit�r� olmad���n� g�stermektedir. Klinik �al��malarda kaspofungin di�er maddelerin CYP3A4 metabolizmas�n� ind�klememi�tir. Kaspofungin P-glikoproteinin bir substrat� de�ildir ve sitokro m P450 enzimlerinin zay�f bir substrat�d�r. Bununla birlikte, farmakolojik ve klinik �al��malarda kaspofunginin di�er t�bbi �r�nlerle etkile�ti�i g�sterilmi�tir (a�a��ya bkz.).
Sa�l�kl� yeti�kinlerde y�r�t�len iki klinik �al��mada, siklosporin (4 mg/kg'l�k 1 doz veya 12 saat arayla 3 mg/kg'l�k iki doz) kaspofunginin A'n�n EAA's�n� yakla��k %35 art�rm��t�r. Bu EAA art��lar� muhtemelen, kaspofunginin karaci�er taraf�ndan al�m�nda azalmaya ba�l�d�r. Kaspofungin siklosporinin plazma d�zeylerini y�kseltmemi�tir. Kaspofungin ve siklosporin birlikte uyguland���nda karaci�er ALT ve AST d�zeylerinde normalin �st s�n�r�n�n (ULN) 3 kat� ge�ici art��lar g�r�lm�� ve bunlar t�bbi �r�nlerin b�rak�lmas�yla normale d�nm��t�r. Pazarlama sonras� d�nemde kaspofungin ve siklosporin ile 1-290 g�n aras�nda de�i�en s�relerle (medyan 17 ,5 g�n) tedavi edilen 40 hastan�n incelendi�i geriye d�n�k bir �al��mada ciddi hi�bir hepatik istenmeyen olay kaydedilmemi�tir (bkz. b�l�m 4.4). Bu iki t�bbi �r�n e� zamanl� uyguland���nda karaci�er enzimlerinin yak�ndan takip edilmesi gerekti�i g�z �n�ne al�nmal�d�r.
Kaspofungin sa�l�kl� yeti�kin g�n�ll�lerde takrolimusun vadi konsantrasyonunu %26 oran�nda d���rm��t�r. Her iki ilac� alan hastalarda takrolimus kan konsantrasyonlar�n�n standart takibi ve takrolimus dozaj�nda uygun ayarlamalar yap�lmas� zorunludur.
Sa�l�kl� eri�kin g�n�ll�lerdeki klinik �al��malar kaspofunginin farmakokinetik parametrelerinin itrakonazol, amfoterisin B, mikofenolat, nelfinavir veya takrolimus ile klinik y�nden �nemli �l��de de�i�medi�ini g�stermektedir. Kaspofungin, itrakonazol, amfoterisin B, rif ampisin veya mikofenolat mofetilin farmakokinetik �zelliklerini etkilememi�tir. G�venlilik verileri s�n�rl� olmakla beraber, kaspofungin itrakonazol, amfoterisin B, rifampisin veya mikofenolat mofetil ile birlikte uygulan�rken �zel �nlemlerin al�nmas�na gerek yoktur.
Sa�l�kl� yeti�kin g�n�ll�lerde rifampisin ve kaspofungin birlikte ba�land���nda e� zamanl� uygulaman�n ilk g�n�nde, rifampisin kaspofunginin EAA's�nda %60 art�� ve vadi konsantrasyonunda %170 art��a yol a�m��t�r. Kaspofunginin vadi d�zeyleri tekrarl� uygulama sonras�nda kademeli olarak azalm��t�r. �ki hafta uygulamadan sonra, rifampisin EAA �zerinde s�n�rl� etki g�stermi� ancak vadi d�zeyleri tek ba��na kaspofungin alan yeti�kin hastalara k�yasla
%30 daha d���k bulunmu�tur. Bu etkile�imin muhtemel mekanizmas�, ta��ma proteinlerinin ba�lang��taki inhibisyonu ve sonraki ind�ksiyonudur. Metabolik enzimleri ind�kleyen di�er t�bbi �r�nler i�in de benzer bir etki beklenebilir. Pop�lasyon farmakokinetik �al��malar�n�n s�n�rl� verileri, kaspofunginin efavirenz ind�kleyicileri, nevirapin, efavirenz, rifampisin, karbamazepin, deksametazon veya fenitoin gibi ind�kleyici ajanlar ile birlikte uygulanmas�n�n kaspofungin EAA's�nda azalmaya neden olabildi�ini g�stermektedir. Yeti�kin hastalarda, kaspofungin metabolik enzimleri ind�kleyen ila�larla e� zamanl� uygulan�rken 70 mg y�kleme dozunun ard�ndan g�nl�k kaspofungin dozunun 70 mg'ye y�kseltilmesi d���n�lmelidir (bkz. b�l�m 4.2).
Yukar�da belirtilen t�m yeti�kin ila� etkile�imleri �al��malar� g�nde 50 mg veya 70 mg kaspofungin dozuyla y�r�t�lm��t�r. Kaspofunginin daha y�ksek dozlar�n�n di�er t�bbi �r�nler ile etkile�imi formel bi�imde �al���lmam��t�r.
Pediyatrik hastalarda, farmakokinetik verilerin regresyon analizlerinin sonu�lar�, kaspofungin ile e� zamanl� olarak deksametazon uygulanmas�n�n kaspofungin vadi konsantrasyonlar�nda klinik y�nden anlaml� azalmalara yol a�abildi�ini ortaya koymaktad�r. Bu bulgu, pediyatrik hastalarda da t�pk� yeti�kinlerde oldu�u gibi ind�kleyici ajanlara ba�l� benzer azalmalar olaca��n� g�stermektedir. Kaspofungin pediyatrik hastalara (12 aydan 17 ya�a kadar) ila� klerensinin ind�kleyicileriyle (rifampisin, nevirapin, efavirenz, karbamazepin, deksametazon veya fenitoin) e� zamanl� olarak uygulan�rken CANCIDAS'�n g�nde 70 mg/mdozu d���n�lmelidir (bir g�nde al�nan ger�ek doz 70 mg a��lmamal�d�r).
4.6. Gebelik ve laktasyon
Gebelik kategorisi C.
�ocuk do�urma potansiyeli bulunan kad�nlar/Do�um kontrol� (Kontrasepsiyon)
Kaspofungin i�in, gebeliklerde maruz kalmaya ili�kin klinik veri mevcut de�ildir. �ocuk do�urma potansiyeli bulunan kad�nlar uygun bir do�um kontrol� uygulamal�d�r.
Gebelik d�nemi
CANCIDAS'�n gebe kad�nlarda kullan�m�na ili�kin veriler yoktur veya s�n�rl�d�r. Gebelik d�neminde kaspofungin kesin gereklilik olmad�k�a kullan�lmamal�d�r. Hayvan �al��malar� geli�imsel toksisiteyi g�stermi�tir (bkz. b�l�m 5.3). Hayvan �al��malar�nda kaspofunginin plasenta bariyerini ge�ti�i g�sterilmi�tir.
Laktasyon d�nemi
Kaspofunginin anne s�t�ne ge�ip ge�medi�i bilinmemektedir. Hayvanlardan elde edilen farmakodinamik/ toksikoloji verileri kaspofunginin s�te ge�ti�ini g�stermi�tir. Kaspofungin alan kad�nlar emzirmemelidir.
�reme yetene�i/ Fertilite
Erkek ve di�i s��anlarda y�r�t�len �al��malarda kaspofungin fertilite �zerinde hi�bir etki g�stermemi�tir (bkz. b�l�m 5.3). Kaspofunginin fertilite �zerindeki etkisini de�erlendirmek i�in klinik veriler mevcut de�ildir.
4.7. Ara� ve makine kullan�m� �zerindeki etkiler
Ara� ve makine kullanma becerisi �zerine etkileri ile ilgili bir �al��ma yoktur.
4.8. �stenmeyen etkiler
A��r� duyarl�l�k reaksiyonlar� (anaflaksi ve muhtemelen histamin arac�l� advers reaksiyonlar) rapor edilmi�tir (bkz. b�l�m 4.4).
Ayr�ca, invazif aspergillozlu hastalarda akci�er �demi, yeti�kin solunum s�k�nt�s� sendromu (ARDS) ve radyografik infiltratlar da bildirilmi�tir.
Eri�kin hastalar
Klinik �al��malarda 1865 eri�kin hasta tekli veya �oklu dozlarda kaspofungin alm��t�r: 564 f ebril n�tropeni hastas� (ampirik tedavi �al��mas�), 382 invazif kandidiyazis hastas�, 228 invazif aspergilloz hastas�, 297 lokalize Candida enfeksiyonu hastas� ve Faz 1 �al��malara kat�lan 394 birey. Ampirik tedavi �al��mas�nda hastalar malignite i�in kemoterapi alm�� veya (39 allojenik transplantasyon dahil) hematopoetik k�k h�cre transplantasyonu ge�irmi�lerdir. Belgelenmi� Candida enfeksiyonlar� olan hastalar�n dahil edildi�i �al��malarda, invazif Candida enfeksiyonlar� olan hastalar�n b�y�k k�sm�nda, e� zamanl� �ok say�da ila� kullan�m�n� gerektiren altta yatan cidd i t�bbi durumlar mevcuttu (�rne�in: hematolojik veya di�er maligniteler, yak�n zamanda �nemli cerrahi operasyon, HIV). Kar��la�t�rmal� olmayan Aspergillus �al��mas�ndaki hastalarda genellikle e� zamanl� �ok say�da ila� kullan�m�n� gerektiren ciddi predispozan t�bbi durumlar mevcuttu (�rne�in kemik ili�i veya periferik k�k h�cre transplantasyonlar�, hematolojik malignitele r, solid t�m�r veya organ transplantlar�).
Flebit, b�t�n hasta pop�lasyonlar�nda yayg�n olarak rapor edilen lokal bir enjeksiyon b�lgesi advers reaksiyonudur. Di�er lokal reaksiyonlar ise eritem, a�r�/hassasiyet, ka��nt�, ak�nt� ve yanma hissidir.
Kaspofungin ile tedavi edilen t�m yeti�kinlerde rapor edilen klinik ve laboratuvar anormallikleri (toplam 1780) tipik olarak hafifti ve nadiren ilac�n kesilmesini gerektirmi�tir.
Klinik �al��malarda ve/veya pazarlama sonras� kullan�mda a�a��daki advers reaksiyonlar rapor edilmi�tir:
�ok yayg�n (≥1/10), yayg�n (≥1/100, <1/10), yayg�n olmayan (>1/1.000, <1/100), Seyrek (≥ 1/10.000 ila <1/1.000), �ok seyrek (<1/10.000), bilinmiyor (eldeki verilerden hareketle tahmin edilemiyor).
Kan ve lenf sistemi hastal�klar�:
Yayg�n: Hemoglobinde azalma, hematokritte azalma, akyuvar say�s�nda azalma.
Yayg�n olmayan: Anemi, trombositopeni, koag�lopati, l�kopeni, eozinofil say�s�nda art��, trombosit say�s�nda azalma, trombosit say�s�nda art��, lenfosit say�s�nda azalma, akyuvar say�s�nda art��, n�trofil say�s�nda azalma.
Metabolizma ve beslenme hastal�klar�:
Yayg�n: Hipokalemi
Yayg�n olmayan: A��r� s�v� y�klenmesi, hipomagnezemi, anoreksi, elektrolit dengesizli�i, hiperglisemi, hipokalsemi, metabolik asidoz.
Psikiyatrik hastal�klar:
Yayg�n olmayan: Anksiyete, oryantasyon bozuklu�u, uykusuzluk.
Sinir sistemi hastal�klar�:
Yayg�n: Ba� a�r�s�
Yayg�n olmayan: Ba� d�nmesi, tat duyumunda bozukluk, parestezi, somnolans, tremor, hipoestezi.
G�z hastal�klar�:
Yayg�n olmayan: G�zde sar�l�k, bulan�k g�rme, g�z kapa�� �demi, g�zya�� art���.
Kardiyak hastal�klar:
Yayg�n olmayan: �arp�nt�, ta�ikardi, aritmi, atriyal fibrilasyon, konjestif kalp yetmezli�i
Vask�ler hastal�klar:
Yayg�n: Flebit
Yayg�n olmayan: Tromboflebit, flushing (ciltte k�zar�kl�k), s�cak basmas�, hipertansiyon, hipotansiyon.
Solunum, g���s ve mediastinal hastal�klar:
Yayg�n: Dispne
Yayg�n olmayan: Nazal konjesyon, faringolaringeal a�r�, takipne, bronkospazm, �ks�r�k, paroksismal nokt�rnal dispne, hipoksi, raller, h�r�lt�l� solunum.
Gastrointestinal hastal�klar:
Yayg�n: Bulant�, ishal, kusma
Yayg�n olmayan: Abdominal a�r�, �st abdominal a�r�, a��z kurulu�u, dispepsi, mide rahats�zl���, abdominal distansiyon, assit, kab�zl�k, disfaji, flatulans.
Hepato-bilier hastal�klar:
Yayg�n: Karaci�er de�erlerinde y�kselme (alanin aminotransferaz, aspartat aminotransferaz, kan alkali fosfataz, konjuge bilir�bin, kan bilir�bini).
Yayg�n olmayan: Kolestaz, hepatomegali, hiperbilir�binemi, sar�l�k, karaci�er fonksiyon anormalli�i, hepatotoksisite, karaci�er bozuklu�u, gama-glutamil transferaz art���.
Deri ve deri alt� doku hastal�klar�:
Yayg�n: D�k�nt�, ka��nt�, eritem, a��r� terleme.
Yayg�n olmayan: Eritema multiforme, mak�ler d�k�nt�, mak�lo-pap�ler d�k�nt�, pruritik d�k�nt�, �rtiker, alerjik dermatit, jeneralize prurit, eritamat�z d�k�nt�, jeneralize d�k�nt�, morbiliform d�k�nt�, deri lezyonlar�.
Bilinmiyor: Toksik epidermal nekroliz ve Stevens-Johnson sendromu (bkz. B�l�m 4.4)
Kas-iskelet bozukluklar�, ba� doku ve kemik hastal�klar�:
Yayg�n: Artralji
Yayg�n olmayan: S�rt a�r�s�, ekstremitelerde a�r�, kemik a�r�s�, kas g��s�zl���, miyalji.
B�brek ve idrar hastal�klar�:
Yayg�n olmayan: B�brek yetmezli�i, akut b�brek yetmezli�i
Genel bozukluklar ve uygulama b�lgesine ili�kin hastal�klar:
Yayg�n: Ate�, ���me, inf�zyon b�lgesinde ka��nt�
Yayg�n olmayan: A�r�, kateter giri� yerinde a�r�, yorgunluk, ���me, s�cakbasmas�, inf�zyon yerinde eritem, inf�zyon yerinde sertlik, inf�zyon yerinde a�r�, inf�zyon yerinde �i�lik, enjeksiyon yerinde flebit, periferik �dem, hassasiyet, g���s rahats�zl���, g���s a�r�s�, y�zde �dem, v�cut �s�s�nda de�i�iklik hissi, sertle�me, inf�zyon yerinde ekstravazasyon, inf�zyon yerinde iritasyon, inf�zyon yerinde flebit, inf�zyon yerinde d�k�nt�, inf�zyon yerinde �rtiker, enjeksiyon yerinde eritem, enjeksiyon yerinde �dem, enjeksiyon yerinde a�r�, enjeksiyon yerinde �i�lik, malaise (k�r�kl�k), �dem.
Ara�t�rmalar:
Yayg�n: Kan potasyumunda azalma, kan alb�mininde azalma.
Yayg�n olmayan: Kan kreatininde art��, idrarda alyuvar h�creleri pozitif, total proteinde azalma, idrarda protein varl���, protrombin zaman�nda uzama, protrombin zaman�nda k�salma, kan sodyumunda azalma, kan sodyumunda art��, kan kalsiyumunda art��, kan kalsiyumunda azalma, kan klor�r�nde azalma, kan glukoz art���, kanda magnezyum azalmas�, kanda fosforun azalmas�, kanda fosfor art���, kan �re art���, aktif parsiyel tromboplastin zaman�n�n uzamas�, kanda bikarbonat azalmas�, kanda klor�r art���, kanda potasyum art���, kan bas�nc� art���, kanda �rike asit azalmas�, idrarda kan varl���, anormal solunum sesleri, karbondioksit azalmas�, ba����kl�k sistemini bask�lay�c� ila�lar�n seviyelerinde art��, uluslararas� normalize oranda art��, �riner silindirler, idrarda akyuvar h�crelerinin pozitif olmas�, idrar pH'�nda art��.
Kaspofungin ayn� zamanda 100 eri�kin hastada g�nde 150 mg (51 g�ne kadar) verilerek de�erlendirilmi�tir (bkz. B�l�m 5.1). �al��ma invazif kandidiyazis tedavisinde g�nde 50 mg kaspofungini (1. g�nde 70 mg y�kleme dozunu takiben) g�nde 150 mg dozu ile kar��la �t�rm��t�r. Bu hasta grubunda daha y�ksek olan bu kaspofungin dozunun g�venlili�i genel ola rak g�nde 50 mg kaspofungin alan hastalarla benzer bulunmu�tur. �la�la ili�kili ciddi bir advers reaksiyon veya kaspofunginin kesilmesine neden olan, ila�la ili�kili bir advers reaksiyon ya�ayan hastalar�n oran� iki tedavi grubunda da benzer bulunmu�tur.
Pediyatrik hastalar
171 pediyatrik hastada tamamlanan 5 klinik �al��man�n verileri klinik istenmeyen olaylar�n toplam insidans�n�n (%26.3; %95 g�ven aral���: -19.9, 33.6) kaspofungin ile tedavi edilen yeti�kinlerde bildirilen insidanstan (%43.1; %95 g�ven aral���: -40.0, 46.2) daha k�t� olmad���n� ortaya koymaktad�r. Ancak, pediyatrik hastalar�n istenmeyen olay profili yeti�kin hastalara k�yasla muhtemelen farkl�d�r. Kaspofungin ile tedavi edilen pediyatrik hastalarda en yayg�n, ila�la ili�k ili klinik istenmeyen olaylar pireksi (%11.7), d�k�nt� (%4.7) ve ba� a�r�s�yd� (%2.9).
A�a��daki advers reaksiyonlar rapor edilmi�tir:
(�ok yayg�n (≥1/10), yayg�n (≥1/100, <1/10), yayg�n olmayan (>1/1.000, <1/100), Seyrek (≥ 1/10.000 ila <1/1.000), �ok seyrek (<1/10.000), bilinmiyor (eldeki verilerden hareketle tahmin edilemiyor).
Kan ve lenf sistemi hastal�klar�: Yayg�n: Eozinofil say�s�nda art��
Sinir sistemi hastal�klar�:
Yayg�n: Ba� a�r�s�
Kardiyak hastal�klar:
Yayg�n: Ta�ikardi
Vask�ler hastal�klar:
Yayg�n: Flushing (ciltte k�zar�kl�k), hipotansiyon
Hepato-bilier hastal�klar:
Yayg�n: Karaci�er enzimlerinde y�kselme (AST, ALT)
Deri ve deri alt� doku hastal�klar�:
Yayg�n: D�k�nt�, ka��nt�
Genel bozukluklar ve uygulama b�lgesine ili�kin hastal�klar�:
�ok yayg�n: Ate�
Yayg�n: ���me, kateter b�lgesinde a�r�
Ara�t�rmalar:
Yayg�n: Potasyumda azalma, hipomagnezemi, glukoz art���, fosforda azalma, fosfor art���.
��pheli advers reaksiyonlar�n raporlanmas�
Ruhsatland�rma sonras� ��pheli ila� advers reaksiyonlar�n�n raporlanmas� b�y�k �nem ta��maktad�r. Raporlama yap�lmas�, ilac�n yarar/risk dengesinin s�rekli olarak izlenmesine olanak sa�lar. Sa�l�k mesle�i mensuplar�n�n herhangi bir ��pheli advers reaksiyonu T�rkiye Farmakovijilans Merkezi (T�FAM)'ne bildirmeleri gerekmektedir (www.titck.gov.tr; e- posta:tufam@titck.gov.tr; tel: 0 800 314 00 08; faks: 0 312 218 35 99)
4.9. Doz a��m� ve tedavisi
Bir g�nde 400 mg'a kadar kaspofunginin yanl��l�kla al�nd��� rapor edilmi�tir. Bu olaylar klinik y�nden �nemli advers reaksiyonlara yol a�mam��t�r. Kaspofungin diyalizle at�lmaz.
 En Yayg�n Alerji T�rleri
Ba����kl�k sistemi, polen, ar� zehiri veya evcil hayvan gibi yabanc� bir maddeye veya �o�u insanda reaksiyona neden olmayan bir yiyece�e tepki g�sterdi�inde alerjiler meydana gelir.
En Yayg�n Alerji T�rleri
Ba����kl�k sistemi, polen, ar� zehiri veya evcil hayvan gibi yabanc� bir maddeye veya �o�u insanda reaksiyona neden olmayan bir yiyece�e tepki g�sterdi�inde alerjiler meydana gelir. |
 Depresyonu Anlamak
Depresyon farkl� ki�ileri farkl� bi�imlerde etkiler. Duygusal veya fiziksel
olmak �zere geni� alanda belirtilere sebep olabilir.Depresyona neler sebep olur?
Depresyonu Anlamak
Depresyon farkl� ki�ileri farkl� bi�imlerde etkiler. Duygusal veya fiziksel
olmak �zere geni� alanda belirtilere sebep olabilir.Depresyona neler sebep olur? |
�LA� GENEL B�LG�LER�
Merck �la� Ecza ve Kimya Ticaret A�
| Geri �deme Kodu | A01580 |
| Sat�� Fiyat� | 4823.48 TL [ 13 Sep 2024 ] |
| �nceki Sat�� Fiyat� | 4823.48 TL [ 6 Sep 2024 ] |
| Original / Jenerik | Original �la� |
| Re�ete Durumu | Normal Re�eteli bir ila�d�r. |
| Barkodu | 8699636260227 |
| Etkin Madde | Kaspofungin Asetat |
| ATC Kodu | J02AX04 |
| Birim Miktar | 50 |
| Birim Cinsi | MG |
| Ambalaj Miktar� | 1 |
| Enfeksiyona Kar�� Kullan�lan (Antienfektif) �la�lar > Sistemik Antimikotikler > Kaspofungin Asetat |
| �thal ( ref. �lke : Yunanistan ) ve Be�eri bir ila�d�r. |
�LA� E�DE�ERLER�
| E�de�er �la� Ad� | Barkodu | �la� Fiyat� |
|---|---|---|
| E�de�er bir ila� bulunamad� |
 |
Diyabet Hastal��� Diyabet, ins�lin hormonu ile ilgili problemlerden kaynaklanan bir hastal�kt�r. |
 |
Artrit Artrit, olduk�a yayg�n bir hastal�kt�r ancak iyi anla��lamam��t�r. Asl�nda �artrit� tek bir hastal���n ad� de�ildir; eklem a�r�s� veya eklem hastal�klar�n� adland�rman�n gayri resmi yoludur. |
 |
Tiroid Kanseri En s�k g�r�len tiroid kanseri t�r� olan papiller tiroid kanseri, t�m tiroid kanserlerinin yakla��k %70'ini olu�turur. |