ANORO ELLIPTA 62.5/25 mcg kullan�ma haz�r inhilasyon tozu. 30 doz K�sa �r�n Bilgisi
{ Umeklidinyum Bromur + Vilanteral }
1. BE�ER� TIBB� �R�N�N ADI
ANORO ELLIPTA 62,5 mcg + 25 mcg kullan�ma haz�r inhalasyon tozu
2. KAL�TAT�F VE KANT�TAT�F B�LE��M
Etkin madde
Uygulanan her bir doz (Ellipta �nhaler'in a��zl���ndan ��kan doz) 55 mikrogram umeklidinyuma e�de�er 65 mikrogram umeklidinyum brom�r ve 22 mikrogram vilanterol (trifenatat olarak) i�ermektedir. Bu, kullan�ma haz�r 62,5 mikrogram umeklidinyuma e�de�er 74,2 mikrogram umeklidinyum brom�r ve 25 mikrogram vilanterole e�de�er 40 mikrogram vilanterol trifenatat dozuna kar��l�k gelmektedir.
Yard�mc� maddeler
Her bir doz yakla��k olarak 25 mg laktoz (monohidrat olarak) i�erir (inek s�t�nden elde edilir). Yard�mc� maddeler i�in 6.1'e bak�n�z.
3. FARMAS�T�K FORMU
Kullan�ma haz�r inhalasyon tozu.
K�rm�z� inhaler kapa�� ve dahili bir doz sayac� olan a��k gri inhaler. ANORO ELLIPTA, her biri beyaz bir toz i�eren 30 dozluk iki adet blister �erit i�ermektedir. Blister �eritlerden biri her dozda 62,5 mikrogram umeklidinyum, di�eri her dozda 25 mikrogram vilanterol i�erir.
1-24. haftada g�nde ortalama p�sk�rtme say�s�ndaki fark
4. KL�N�K �ZELL�KLER
4.1. Terap�tik endikasyonlar
ANORO ELLIPTA, eri�kin kronik obstr�ktif akci�er hastalar�nda (KOAH) g�r�len semptomlar�n giderilmesine y�nelik kontrol edici bir bronkodilat�r tedavidir.
4.2. Pozoloji ve uygulama �ekli
Yeti�kinler:
�nerilen doz g�nde bir defa ANORO ELLIPTA 62,5/25 mikrogram inhalasyondur.
ANORO ELLIPTA, bronkodilatasyonu muhafaza etmek i�in her g�n, g�nde bir kez, g�n�n ayn� saatinde uygulanmal�d�r. Maksimum doz, g�nde bir defa ANORO ELLIPTA 62,5/25 mikrogram inhalasyondur.
Uygulama �ekli:
ANORO ELLIPTA sadece inhalasyon yoluyla kullan�l�r.
ANORO ELLIPTA her g�n, g�nde bir kez, g�n�n ayn� saatinde uygulanmal�d�r. ANORO ELLIPTA tek dozluk kullan�ma haz�r inhalasyondur.
1
Kullanma Talimat�
ANORO ELLIPTA ilk kez kullan�lmaya ba�lan�ld���nda d�zg�n �al��t���n�n kontrol edilmesi ve �zel bir y�ntemle kullan�ma haz�rlanmas� gerekmemektedir. Sadece a�a��daki talimatlara uyulmal�d�r.
ANORO ELLIPTA ambalaj� a�a��daki i�eriklerden olu�ur:
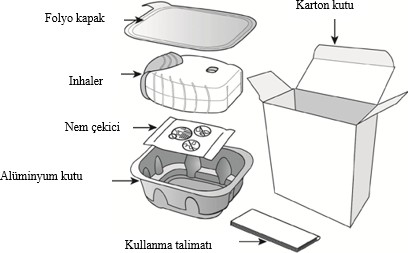
�nhaler, nemi azaltmak i�in nem �ekici bir paket i�eren al�minyum kutuda paketlenmi�tir. Al�minyum kutunun kapa�� a��ld�ktan sonra nem �ekici paket at�lmal�d�r. Nem �ekici paket a��lmamal�, yutulmamal� veya teneff�s edilmemelidir. Dozu almaya haz�r olana kadar al�minyum kutunun kapa�� a��lmamal�d�r.
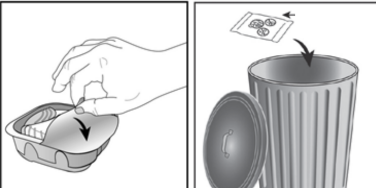
�nhaler al�minyum kutudan ��kar�ld���nda, “kapal�” pozisyonda olacakt�r. �nhalerin son kullanma tarihi etiketindeki bo�lu�a yaz�lmal�d�r. �nhalerin son kullanma tarihi al�minyum kutunun a��lmas�ndan sonra 6 haftad�r. Son kullanma tarihinden sonra inhaler kullan�lmamal�d�r. Folyo kapak a��ld�ktan sonra at�labilir.
�nhaler kullan�lmaya ba�lamadan �nce a�a��daki talimatlar okunmal�d�r.
E�er ila� inhale edilmeden, inhaler kapa�� a��l�p kapat�l�rsa, bir doz harcanm�� olur.
Harcanan doz inhalerin i�erisinde g�venle tutulur fakat art�k kullan�lamaz. Bir inhalasyonda
yanl��l�kla ilave ila� veya �ift doz almak m�mk�n de�ildir.
Doz sayac�
Bu saya�, inhaler i�inde ka� doz ila� kald���n� g�sterir.
4.3. Kontrendikasyonlar
ANORO ELLIPTA,
�iddetli s�t proteini alerjisi bulunan hastalarda,
4.4. �zel kullan�m uyar�lar� ve �nlemleri
Ast�m
Umeklidinyum/vilanterol�n ast�ml� hastalarda kullan�m�na ait �al��ma bulunmad���ndan bu
hasta pop�lasyonunda kullan�lmamal�d�r.
Paradoksal bronkospazm
Umeklidinyum/vilanterol�n uygulanmas�, ya�am� tehdit edebilecek paradoksal bronkospazma yol a�abilir. Paradoksal bronkospazm olu�mas� halinde umeklidinyum/vilanterol ile tedavi derhal kesilmelidir ve gerekirse alternatif tedavi ba�lat�lmal�d�r.
Akut kullan�m i�in de�ildir.
Umeklidinyum/vilanterol bronkospazm�n akut ataklar�n�n tedavisi i�in endike de�ildir.
Hastal���n k�t�le�mesi
Semptomlar� rahatlatmak i�in artan k�sa etkili bronkodilat�r kullan�m�, kontrol�n bozuldu�unu g�stermektedir. Umeklidinyum/vilanterol ile tedavi s�ras�nda KOAH'�n k�t�le�mesi durumunda, hastan�n ve KOAH tedavi rejiminin yeniden de�erlendirmesi yap�lmal�d�r.
Kardiyovask�ler etkiler
Umeklidinyum/vilanterol dahil muskarinik resept�r antagonistleri ve sempatomimetik ajanlar�n uygulanmas�ndan sonra kardiyak aritmiler (�r. atriyal fibrilasyon ve ta�ikardi) gibi kardiyovask�ler etkiler g�r�lebilir. Klinik olarak anlaml� kontrols�z kardiyovask�ler hastal��� olan hastalar klinik �al��malardan ��kar�lm��t�r. Dolay�s�yla, umeklidinyum/vilanterol �iddetli kardiyovask�ler hastal��� olan hastalarda dikkatle kullan�lmal�d�r.
Antimuskarinik aktivite
Antimuskarinik aktivitesine ba�l� olarak umeklidinyum/vilanterol, �riner retansiyonu veya dar a��l� glokomu olan hastalarda dikkatli kullan�lmal�d�r.
Hipokalemi
Betaadrenerjik agonistler, baz� hastalarda istenmeyen kardiyovask�ler etkiler olu�turma potansiyeli olan anlaml� hipokalemi olu�turabilir. Serum potasyumundaki azalma genellikle ge�icidir, takviye gerektirmez.
Umeklidinyum/vilanterol ile �nerilen terap�tik dozlarda yap�lan klinik �al��malarda hipokaleminin klinik olarak anlaml� etkisi g�r�lmemi�tir. Umeklidinyum/vilanterol, hipokalemiye neden olma potansiyeli olan di�er ila�larla birlikte kullan�ld���nda dikkatli olunmal�d�r (bkz. B�l�m 4.5).
Hiperglisemi
Betaadrenerjik agonistler baz� hastalarda ge�ici hiperglisemiye neden olabilir.
Umeklidinyum/vilanterol ile �nerilen terap�tik dozlarda yap�lan klinik �al��malarda plazma glukozu �zerinde klinik olarak anlaml� etki g�r�lmemi�tir. Umeklidinyum/vilanterol ile tedaviye ba�land���nda plazma glukozu diyabetik hastalarda daha yak�ndan takip edilmelidir.
E�lik eden ko�ullar
Umeklidinyum/vilanterol, konv�lsif bozukluklar� veya tirotoksikozu olan hastalarda ve beta
adrenerjik agonistlere kar�� al���lmad�k duyarl�l��� olan hastalarda dikkatli kullan�lmal�d�r.
Yard�mc� maddeler
Bu t�bbi �r�n laktoz i�ermektedir. Galaktoz intolerans�, Lapp laktaz eksikli�i ve glukoz- galaktoz malabsorpsiyonu gibi nadir kal�t�msal sorunlar� olan hastalar bu ilac� kullanmamal�d�r.
4.5. Di�er t�bbi �r�nler ile etkile�imler ve di�er etkile�im �ekilleri
Beta blok�rler ile etkile�im:
Beta adrenerjik blok�rler, vilanterol gibi betaadrenerjik agonistlerin etkisini zay�flatabilir veya antagonize edebilirler. Kullan�lmas�n� zorunlu k�lan sebepler olmad�k�a selektif veya selektif olmayan beta adrenerjik blok�rlerin e�zamanl� kullan�m�ndan ka��n�lmal�d�r.
Metabolik ve ta��y�c� bazl� etkile�imler
Vilanterol, sitokrom P450 3A4'�n (CYP3A4) bir substrat�d�r. G��l� CYP3A4 inhibit�rlerinin (�r. ketokonazol, klaritromisin, itrakonazol, ritonavir, telitromisin) e� zamanl� uygulamas�, vilanterol�n metabolizmas�n� inhibe edebilir ve vilanterole sistemik maruziyeti artt�rabilir. Ketokonazol (400 mg) ile birlikte uygulanmas�, ortalama vilanterol EAAve C'� s�ras�yla
%65 ve %22 oran�nda artt�rm��t�r. Vilanterol maruziyetindeki art��; kalp h�z�, kan potasyumu veya QT aral��� (Fridericia y�ntemi kullan�larak d�zeltilmi� olan) �zerindeki beta adrenerjik agonist ile ilgili sistemik etkiler ile ili�kilendirilmemi�tir. Umeklidinyum/vilanterol�, ketokonazol ve bilinen di�er g��l� CYP3A4 inhibit�rleri ile birlikte uygularken dikkatli olunmas� tavsiye edilmektedir, ��nk� vilanterole sistemik maruziyetin artma potansiyeli bulunmaktad�r, bu da istenmeyen etkilerin art���na sebep olabilir. Orta g��te bir CYP3A4 inhibit�r� olan verapamil, vilanterol�n farmakokineti�ini anlaml� bir �ekilde etkilememi�tir.
Umeklidinyum, sitokrom P450 2D6'n�n (CYP2D6) bir substrat�d�r. Umeklidinyumun kararl� durum farmakokineti�i, CYP2D6 eksikli�i olan (zay�f metabolize edenler) sa�l�kl� g�n�ll�lerde de�erlendirilmi�tir. 8 kat y�ksek dozda, umeklidinyum EAA veya C�zerinde herhangi bir etki g�zlenmemi�tir. 16 kat y�ksek dozda, umeklidinyum EAA'da 1,3 kat art�� g�zlenmi�tir ve umeklidinyum C'� �zerinde herhangi bir etki g�zlenmemi�tir. Bu de�i�ikliklerin b�y�kl���ne ba�l� olarak, umeklidinyum/vilanterol CYP2D6 inhibit�rleri ile birlikte veya CYP2D6 eksikli�i bulunan hastalara (zay�f metabolize edenler) uyguland���nda klinik olarak anlaml� bir ila� etkile�imi beklenmemektedir.
Hem umeklidinyum hem de vilanterol, P-glikoprotein ta��y�c�s�n�n (P-gp) substratlar�d�r. Orta g��te P-gp inhibit�r� verapamilin (g�nde bir kez 240 mg), umeklidinyum ve vilanterol�n kararl� durum farmakokineti�i �zerindeki etkisi sa�l�kl� g�n�ll�lerde de�erlendirilmi�tir. Verapamilin, umeklidinyum veya vilanterol C'lar� �zerinde herhangi bir etkisi g�zlenmemi�tir. Umeklidinyum EAA'da yakla��k 1,4 kat art�� g�zlenmi� olup vilanterol EAA de�eri �zerinde herhangi bir etki g�zlenmemi�tir. Bu de�i�ikliklerin b�y�kl���ne ba�l� olarak, umeklidinyum/vilanterol, P-gp inhibit�rleri ile birlikte uyguland���nda klinik olarak anlaml� bir ila� etkile�imi beklenmemektedir.
Di�er antimuskarinikler ve sempatomimetikler
agonistlerin istenmeyen etkilerini art�rabilece�inden tavsiye edilmemektedir (bkz. B�l�m 4.4 ve 4.9).
Hipokalemi
Metilksantin t�revleri, steroidler veya potasyum tutucu olmayan di�retikler ile e� zamanl� hipokalemik tedavi betaadrenerjik agonistlerin olas� hipokalemik etkilerini art�rabilece�inden dikkatle kullan�lmal�d�r (bkz. B�l�m 4.4).
KOAH i�in kullan�lan di�er t�bbi �r�nler
Resmi in vivo ila� etkile�im �al��malar� yap�lmam�� olmas�na kar��n, inhale umeklidinyum/vilanterol, k�sa etkili sempatomimetik bronkodilat�rler ve inhale kortikosteroidler de dahil olmak �zere di�er KOAH t�bbi ila�lar� ile e� zamanl� olarak kullan�lm�� olup klinik ila� etkile�imi g�zlenmemi�tir.
�zel pop�lasyonlara ili�kin ek bilgiler:
�zel pop�lasyonlarda herhangi bir etkile�im �al��mas� y�r�t�lmemi�tir.
Pediyatrik pop�lasyon:
Pediyatrik pop�lasyonda herhangi bir etkile�im �al��mas� y�r�t�lmemi�tir.
4.6. Gebelik ve laktasyon
Genel tavsiyeGebelik kategorisi: C
�ocuk do�urma potansiyeli bulunan kad�nlar/Do�um kontrol� (Kontrasepsiyon)
�ocuk do�urma potansiyeli bulunan kad�nlarda ve do�um kontrol� (kontrasepsiyon)
uygulayanlarda kullan�m�na ili�kin herhangi bir veri yoktur.
Gebelik d�nemi
Umeklidinyum/vilanterol�n gebe kad�nlarda kullan�m�na ili�kin veri bulunmamaktad�r. Hayvanlarda yap�lan �al��malar, vilanterol�n uygulanmas�ndan sonra �reme toksisitesi g�stermi�tir (bkz. B�l�m 5.3). Umeklidinyum/vilanterol gebelik d�neminde, sadece anne i�in beklenen yararlar� fet�s i�in olas� risklerden fazla oldu�unda kullan�lmal�d�r.
Laktasyon d�nemi
Umeklidinyum veya vilanterol�n anne s�t�ne ge�ip ge�medi�i bilinmemektedir. Ancak, anne s�t�nde di�er betaadrenerjik agonistler tespit edilmi�tir. Yeni do�ana/bebeklere y�nelik risk d��lanamaz. Emzirmenin bebe�e ve tedavinin anneye yarar� dikkate al�narak, emzirmenin kesilmesi veya ANORO ELLIPTA tedavisinin kesilmesinden hangisinin yap�lmas� gerekti�i konusunda bir karara var�lmal�d�r.
�reme yetene�i/Fertilite
Umeklidinyum/vilanterol�n insanlarda fertilite �zerindeki etkilerine ili�kin herhangi bir veri yoktur. Hayvan �al��malar� umeklidinyum veya vilanterol�n fertilite �zerinde hi�bir etkisi olmad���n� g�stermektedir (bkz. B�l�m 5.3).
4.7. Ara� ve makine kullan�m� �zerindeki etkiler
Umeklidinyum/vilanterol'�n ara� ve makine kullan�m� �zerine herhangi bir etkisi yoktur veya
ihmal edilebilir d�zeydedir.
4.8. �stenmeyen etkiler
G�venlilik profilinin �zeti
Umeklidinyum/vilanterol ile en s�k rapor edilen istenmeyen etki nazofarenjit olmu�tur (%9).
4.8. �stenmeyen etkiler
ANORO ELLIPTA'n�n g�venlilik profili, KOAH'l� 6855 hastan�n dahil oldu�u klinik geli�tirme program�nda, umeklidinyum/vilanterol ve bile�enlerin her biriyle elde edilmi� g�venlilik deneyimine ve spontan raporlamaya dayanmaktad�r.
Klinik geli�tirme program� 24 hafta veya daha uzun s�ren Faz III klinik �al��mada g�nde bir kez umeklidinyum/vilanterol alm�� olan 2354 hasta; 24 haftal�k �al��mada 55/22 mcg'l�k �nerilen dozu alm�� olan 1296 hasta, 24 haftal�k bir �al��mada 113/22 mcg'l�k y�ksek dozu alm�� olan 832 hasta ve 12 ayl�k bir �al��mada 113/22 mcg dozunu alm�� 226 hastay� i�ermektedir.
A�a��da verilen yan etkilere atanan frekanslar 24-haftal�k be� �al��man�n entegrasyonundan ve 12 ayl�k g�venlilik �al��mas�ndan g�zlemlenen ham s�kl�k oranlar�n� i�ermektedir.
A�a��da istenmeyen etkiler MedDRA v�cut organ sistem s�n�fland�rmas� ve s�kl��a g�re liste halinde sunulmaktad�r. �stenmeyen etkilerin s�n�fland�r�lmas� i�in a�a��daki s�n�fland�rma �l�e�i kullan�lm��t�r:
�ok yayg�n (≥1/10); yayg�n (≥1/100 ila <1/10); yayg�n olmayan (≥1/1.000 ila <1/100); seyrek (≥1/10.000 ila <1/1.000); �ok seyrek (<1/10.000), bilinmiyor (eldeki verilerden hareketle tahmin edilemiyor).
Enfeksiyonlar ve enfestasyonlar
Yayg�n: �drar yolu enfeksiyonu, sin�zit, nazofarenjit, farenjit, �st solunum yolu enfeksiyonu
Ba����kl�k sistemi hastal�klar�
Yayg�n olmayan: D�k�nt�y� i�eren hipersensitivite reaksiyonlar�
Seyrek: Anaflaksi, anjiyo�dem ve �rtikeri i�eren hipersensitivite reaksiyonlar�
Sinir sistemi hastal�klar�
Yayg�n: Ba� a�r�s� Yayg�n olmayan: Tremor, disguzi Bilinmiyor: Ba� d�nmesi
G�z hastal�klar�
Seyrek: Glokom, bulan�k g�rme, intraok�ler bas�n� art���, g�z a�r�s�
Kardiyak hastal�klar
Yayg�n olmayan: Atriyal fibrilasyon, supraventrik�ler ta�ikardi, idioventrik�ler ritim, ta�ikardi, supraventrik�ler ekstrasistoller, �arp�nt�
Solunum, g���s bozukluklar� ve mediastinal hastal�klar
Yayg�n: �ks�r�k, orofarenjiyal a�r� Yayg�n olmayan: Disfoni
Seyrek: Paradoksalbronkospazm
Gastrointestinal hastal�klar
Yayg�n: Kab�zl�k, a��z kurulu�u
Deri ve deri alt� doku hastal�klar�
Yayg�n olmayan: D�k�nt�
Kas-iskelet bozukluklar, ba� doku ve kemik hastal�klar�
Yayg�n olmayan: Kas spazmlar�
B�brek ve idrar yolu hastal�klar�
Seyrek: �riner retansiyon, dis�ri, mesane ��k��� obstr�ksiyonu
��pheli advers reaksiyonlar�n raporlanmas�:
Ruhsatland�rma sonras� ��pheli ila� advers reaksiyonlar�n�n raporlanmas� b�y�k �nem ta��maktad�r. Raporlama yap�lmas�, ilac�n yarar/risk dengesinin s�rekli olarak izlenmesine olanak sa�lar. Sa�l�k mesle�i mensuplar�n�n herhangi bir ��pheli advers reaksiyonu T�rkiye Farmakovijilans Merkezi (T�FAM)'ne bildirmeleri gerekmektedir (www.titck.gov.tr; e- posta: tufam@titck.gov.tr; tel: 0 800 314 00 08; faks: 0 312 218 35 99).
4.9. Doz a��m� ve tedavisi
Umeklidinyum/vilanterol�n doz a��m�nda muhtemelen bireysel bile�enlerin etkilerinden kaynaklanan, bilinen inhale muskarinik antagonist istenmeyen etkiler (�r: a��z kurulu�u, g�rme bozukluklar� ve ta�ikardi) ve di�er betaadrenerjik agonistlerde doz a��m�nda g�r�len istenmeyen etkiler (�r. aritmiler, tremor, ba� a�r�s�, palpitasyonlar, bulant�, hiperglisemi ve hipokalemi) ile tutarl� belirti ve semptomlar g�r�lecektir.
Tedavi
E�er doz a��m� meydana gelirse, hastaya gerekti�i �ekilde uygun takip ile destekleyici tedavi uygulanmal�d�r.
5. FARMAKOLOJ�K �ZELL�KLER
5.1. Farmakodinamik �zellikler
Farmakoterap�tik grup: Obstr�ktif hava yolu hastal�klar� i�in ila�lar, kortikosteroidlerle birlikte ��l� kombinasyon dahil antikolinerjikler ile kombinasyon halinde adrenerjikler
ATC kodu: R03AL03
Etki mekanizmas�:
Umeklidinyum/vilanterol uzun etkili bir muskarinik resept�r antagonisti/uzun etkili betaadrenerjik agonistinin (LAMA/LABA) inhalasyona y�nelik bir kombinasyonudur. �nhalasyonu takiben, her iki bile�en, solunum yollar�na lokal olarak etki eder ve farkl� mekanizmalarla bronkodilatasyon yarat�r.
Umeklidinyum
do�rudan uyguland���nda, in vitro insan M3 muskarinik resept�r altt�r�nde yava� reversibilite
ve in vivo uzun etki s�resi g�sterir.
Vilanterol
Vilanterol, selektif, uzun etkili bir betaadrenerjik resept�r agonistidir (betaadrenerjik agonisti). Vilanterol de dahil olmak �zere betaadrenerjik agonist ila�lar�n farmakolojik etkileri, en az�ndan k�smen de olsa adenozin trifosfat�n (ATP) siklik 3′,5′-adonezin monofosfata (siklik AMP) d�n��mesinde kataliz�r g�revi g�ren enzim olan intrasell�ler adenilat siklaz�n stim�lasyonu ile ili�kilendirilebilir. Artan siklik AMP d�zeyleri bron�iyal d�z kas�n gev�emesine ve �zellikle mast h�creler olmak �zere h�crelerden ani a��r� duyarl�l�k arac�lar�n�n sal�nmas�n�n inhibe edilmesine neden olmaktad�r.
Farmakodinamik etkiler
Faz III, 6 ayl�k �al��malarda plaseboya k�yasla umeklidinyum/vilanterol, g�nde bir kez uygulamay� takiben 24 saatte akci�er fonksiyonunda (1 saniyedeki zorlu ekspiratuar hacim [FEV] ile �l��ld��� �zere), ilk dozun uygulanmas�ndan sonra 15. dakikada belirginle�en (plaseboya k�yasla 112 ml iyile�me (p<0,001*)) klinik anlaml� iyile�meler sa�lam��t�r. Plaseboya k�yasla doz uygulamas�n� takip eden ilk 6 saat i�inde FEV'deki ortalama pik iyile�meleri 24. haftada 224 ml'dir (p<0,001*). ANORO ELLIPTA etkisinde zaman i�erisinde ta�ifilaksi kan�t�na rastlanmam��t�r.
Kardiyak elektrofizyoloji
Umeklidinyum/vilanterol�n QT aral��� �zerindeki etkisi 103 sa�l�kl� g�n�ll�de 10 g�n boyunca g�nde bir kez 113/22 mikrogram veya 500/100 mikrogram (�nerilen dozun sekiz kat� umeklidinyum ve �nerilen dozun d�rt kat� vilanterol ile tek doz) umeklidinyum/vilanterol uygulamas�n� i�eren plasebo ve aktif (moksifloksasin) kontroll� QT �al��mas�nda de�erlendirilmi�tir. QT aral��� uzamalar�nda ba�lang�ca g�re d�zeltme sonras�nda plaseboya g�re maksimum ortalama fark (Fridericia y�ntemi kullan�larak d�zeltilmi�, QTF) umeklidinyum/vilanterol 113/22 mikrogram ile uygulamadan 10 dakika sonra 4,3 (%90 GA=2,2 ila 6,4) milisaniye ve umeklidinyum/vilanterol 500/100 mikrogram ile uygulamadan 30 dakika sonra 8,2 (%90 GA=6,2 ila 10,2) milisaniyedir. Bu nedenle umeklidinyum/vilanterol 113/22 mikrogram ile QT aral��� uzamalar� ile ili�kili klinik ilgiye sahip pro-aritmik potansiyel g�zlenmemi�tir.
Kalp h�z�nda doza ba��ml� bir art�� da g�zlenmi�tir. Kalp h�z�nda ba�lang�ca g�re d�zeltme sonras�nda plaseboya k�yasla maksimum ortalama fark umeklidinyum/vilanterol 113/22 mikrogram ve 500/1000 mikrogram uygulamas�ndan 10 dakika sonra s�ras�yla 8,4 (%90 GA = 7 ila 9,8) at�m/dakika ve 20,3 (%90 GA = 18,9 ila 21,7) at�m/dakikad�r.
Ayr�ca, 6 ayl�k bir �al��mada g�nde bir kez umeklidinyum/vilanterol 55/22 mikrogram ile tedavi edilen KOAH'l� 53 hastada veya 6 ayl�k bir ba�ka �al��mada g�nde bir kez umeklidinyum/vilanterol 113/22 mikrogram alan ilave 55 hastada ve 12 ayl�k bir �al��mada g�nde bir kez 113/22 mikrogram alan 226 hastada 24 saatlik Holter takibinde kardiyak ritim �zerinde klinik olarak anlaml� etkiler g�zlenmemi�tir.
*Bu �al��mada geriye do�ru ad�mlamatestikullan�lm��t�rvebukar��la�t�rma, istatistiksel anlaml�l��a ula�mayan
Klinik etkililik ve g�venlilik
G�nde bir kez uygulanan umeklidinyum/vilanterol�n klinik etkilili�i klinik KOAH tan�s� alm�� 6.835 yeti�kin hastada y�r�t�len sekiz Faz III klinik �al��mada de�erlendirilmi�tir; 6 ayl�k �al��malardan 5.618 hasta (iki plasebo kontroll� ve �� aktif [tiotropium]-komparat�r kontroll�), iki 3 ayl�k egzersiz dayan�m�/akci�er fonksiyonu �al��malar�ndan 655 hasta ve 12 ayl�k destekleyici bir �al��madan 562 hasta.
Akci�er fonksiyonu �zerindeki etkiler
ANORO ELLIPTA �e�itli �al��malarda akci�er fonksiyonunda iyile�meler (dip FEV'de ba�lang�ca g�re de�i�iklik olarak tan�mlanan) g�stermi�tir. 6 ayl�k bir Faz III �al��mas�nda, ANORO ELLIPTA 24. haftada plaseboya ve her bir monoterapi bile�eni tedavi koluna k�yasla dip FEV'de istatistiksel olarak anlaml� iyile�meler g�stermi�tir.
Ayr�ca, ANORO ELLIPTA �� adet 6 ayl�k aktif kontroll� �al��man�n ikisinde dip FEV'de tiotropiyuma k�yasla klinik olarak �nemli ve istatistiksel olarak anlaml� iyile�meler ve ���nc� aktif komparat�rl� �al��mada tiotropiuma k�yasla say�sal olarak daha fazla iyile�meler g�stermi�tir (bkz. Tablo 1). Bronkodilat�r etkisinde zaman i�erisinde bir azalma g�r�lmemi�tir.
Semptomatik sonu�lar
Nefes darl���:
ANORO ELLIPTA plaseboya k�yasla 24. haftada TDI fokal skorunda (kritik ikincil sonlan�m noktas�) art�� ile de�erlendirilen nefes darl���nda istatistiksel olarak ve klinik olarak anlaml� azalma g�stermi�tir (bkz. Tablo 1). Her bir monoterapi bile�eni ve tiotropiuma k�yasla TDI fokal skorundaki iyile�meler istatistiksel olarak anlaml� de�ildir (bkz. Tablo 1).
24. haftada TDI fokal skorunda en az 1 �nitelik minimum klinik �nemli fark (MCID) ile yan�t veren hasta oran� plaseboya (%41) ve her bir monoterapi bile�enine (umeklidinyum i�in %53 ve vilanterol i�in %51) k�yasla ANORO ELLIPTA i�in daha y�ksektir (%58).
Sa�l�kla ba�lant�l� ya�am kalitesi:
ANORO ELLIPTA ayn� zamanda St. George Solunum Anketi (SGRQ) kullan�larak �l��len sa�l�kla ba�lant�l� ya�am kalitesinde plasebo ve her bir monoterapi bile�enine k�yasla 24. haftada SGRQ toplam skorundaki azalma ile kan�tlanan bir iyile�me g�stermi�tir (bkz., Tablo 1). ANORO ELLIPTA �� aktif kontroll� �al��man�n birinde tiotropiuma k�yasla SGRQ toplam skorunda istatistiksel olarak anlaml� bir azalma g�stermi�tir (bkz. Tablo 1).
24. haftada SGRQ skorunda en az MCID (ba�lang�ca g�re 4 birimlik bir azalma olarak tan�mlanan) ile yan�t veren hasta oran� plasebo (%34) ve her bir monoterapi bile�enine (umeklidinyum i�in %44 ve vilanterol i�in %48) k�yasla ANORO ELLIPTA i�in daha y�ksektir (%49). Bir aktif komparat�r �al��mas�nda, ANORO ELLIPTA kullanan daha y�ksek bir hasta y�zdesi tiotropiuma (%46) k�yasla 24. haftada SGRQ skorunda klinik olarak anlaml� bir iyile�me (%53) ile yan�t vermi�tir. Di�er iki aktif komparat�rl� �al��mada, benzer bir hasta oran� ANORO ELLIPTA ve tiotropium ile en az MCID elde edilmi�tir; ANORO ELLIPTA 62,5/25 mikrogram i�in %49 ve %54 ve tiotropium i�in %52 ve %55.
Kurtar�c� ila� kullan�m�
ANORO ELLIPTA, plasebo ve umeklidinyuma k�yasla salbutamol ile kurtar�c� ila� kullan�m�n� 1-24 hafta boyunca azaltm��t�r (bkz. Tablo 1) ve ba�lang�ca g�re kurtar�c� ila� kullan�m�n�n gerekmedi�i g�n oran�nda art�� sa�lam��t�r (ortalama %11,1); plaseboda ise bu oranda ba�lang�ca g�re azalma g�zlenmi�tir(ortalama%0,9).
�� adet 6 ayl�k aktif komparat�r kontroll� �al��mada, ANORO ELLIPTA tiotropiuma k�yasla salbutamol ile kurtar�c� ila� kullan�m�n� azaltm��t�r ve �al��malar�n ikisinde bu azalmalar istatistiksel olarak anlaml�d�r (bkz. Tablo 1). ANORO ELLIPTA ayn� zamanda �� �al��man�n t�m�nde kurtar�c� ila� kullan�m�n�n gerekmedi�i g�n oran�nda tiotropiuma k�yasla (ortalama
%11,7 ila %13,4 aral��� i�inde) ba�lang�ca g�re y�ksek bir art�� g�stermi�tir (ortalama %17,6 ila %21,5 aral��� i�inde).
Tablo 1. 24. haftada akci�er fonksiyonu, semptomatik ve sa�l�kla ba�lant�l� ya�am kalitesi bulgular�
ANORO ELLIPTA 62,5/25 mcg ile tedavi k�yaslamalar� | Tedavi fark�(%95 g�ven aral�klar�, p-de�eri) | |||
Dip FEV(ml) | TDI Fokal Skoru | SGRQ Toplam Skoru | Kurtar�c� ila� kullan�m� | |
ANORO ELLIPTA (N = | 167 | 1,2 | -5,51 | -0,8 |
413) | (128, 207) | (0,7,1,7) | (-7,88, -3,13) | (-1,3,-0,3) |
kar��s�nda plasebo (N = 280) | <0,001 | <0,001 | <0,001 | 0,001 |
ANORO ELLIPTA (N = 413) kar�����nda umeklidinyum 62,5 mcg (N = 418) | 52 (17, 87) 0,004 | 0,3 (-0,2, 0,7) 0,244 | -0,82 (-2,9, 1,27) 0,441 | -0,6 (-1, -0,1) 0,014 |
ANORO ELLIPTA (N = | 95 (60, 130) <0,001 | 0,4 (-0,1, 0,8) 0,117 | -0,32 (-2,41, 1,78) 0,767 | 0,1 (-0,3, 0,5) 0,675 |
413) | ||||
kar��s�nda vilanterol 25 mcg | ||||
(N = 421) | ||||
ANORO ELLIPTA (N = 454) kar��s�nda tiotropium 18 mcg (N = 451) (�al��ma ZEP117115) |
112 (81, 144) <0,001 |
n/e |
-2,10 (-3,61, -0,59) 0,006 |
-0,5 (-0,7, -0,2) <0,001 |
ANORO ELLIPTA |
90 (39, 141) <0,001 |
|
0,75 (-2,12, 3,63) 0,607 |
-0,7 (-1,2, -0,1) 0,022 |
(N = 207) |
| |||
kar��s�nda |
| |||
tiotropium 18 mcg |
| |||
(N = 203) (�al��ma DB2113360) | 0,1 (-0,4, 0,5) 0,817 | |||
ANORO ELLIPTA (N = 217) kar��s�nda tiotropium 18 mcg (N = 215) |
60 (10, 109) 0,018 |
-0,17 (-2,85, 2,52) 0,904 |
-0,6 (-1,2, 0,0) 0,069 | |
(�al��ma DB2113374) |
|
|
|
|
*Bu �al��mada geriye do�ru ad�mlama testi kullan�lm��t�r ve bu kar��la�t�rma, istatistiksel anlaml�l��a ula�mayan bir kar��la�t�rman�n alt�ndad�r. Bu nedenle, bu kar��la�t�rmadan istatistiksel bir anlama varmak olas� de�ildir.
N = Tedavi ama�l� pop�lasyon cinsinden say�
mcg = mikrogram
n/e = de�erlendirilmemi�tir
En k���k kareler ortalamas�
5.2. Farmakokinetik �zellikler
Genel �zelliklerUmeklidinyum ve vilanterol inhalasyon yoluyla birlikte uyguland���nda, her bir bile�enin farmakokineti�i her bir etkin madde ayr� ayr� uyguland���nda g�zlenene benzerdi. Dolay�s�yla, farmakokinetik ama�lar i�in her bir bile�en ba��ms�z olarak d���n�lebilir.
Emilim
Umeklidinyum
Umeklidinyumun sa�l�kl� g�n�ll�lere inhale edilerek uygulanmas�n� takiben, C5-15 dakikada olu�mu�tur. �nhale umeklidinyumun mutlak biyoyararlan�m�, oral emilimden gelen �nemsiz d�zeyde katk� ile dozun ortalama %13'�d�r. �nhale umeklidinyumun yinelenen dozlam�n� takiben, kararl� durum, 1,5-1,8 kat� birikim ile 7-10 g�n aras�nda elde edilmi�tir.
Vilanterol
Vilanterol�n sa�l�kl� g�n�ll�lere inhale edilerek uygulanmas�n� takiben, C5-15 dakikada olu�mu�tur. �nhale vilanterol�n mutlak biyoyararlan�m� oral emilimden gelen �nemsiz d�zeyde katk� ile %27'dir. �nhale vilanterol�n yinelenen dozlar�n� takiben, kararl� durum, 2,4 kat� birikim ile 6 g�n i�inde elde edilmi�tir.
Da��l�m
Umeklidinyum
Sa�l�kl� g�n�ll�lere intraven�z uygulamay� takiben, ortalama da��l�m hacmi 86 litredir. �nsan plazmas�ndaki in vitro plazma proteinine ba�lanma oran� ortalama %89'dur.
Vilanterol
Sa�l�kl� g�n�ll�lere yap�lan intraven�z uygulamay� takiben, kararl� durumda ortalama da��l�m hacmi 165 litredir. �nsan plazmas�ndaki in vitro plazma proteinine ba�lanma oran� ortalama
%94't�r.
Biyotranformasyon
Umeklidinyum
�n vitro �al��malar, umeklidinyumun daha �ok sitokrom P450 2D6 (CYP2D6) taraf�ndan metabolize edildi�ini ve P-glikoprotein (P-gp) transporteri i�in bir substrat oldu�unu g�stermi�tir. Umeklidinyum i�in primer metabolik yollar, oksidatif (hidroksilasyon, O- dealkilasyon) ve bunu takiben konjugasyonu (glukuronidasyon vb.) olup, d���k farmakolojik aktivite i�eren ya da farmakolojik aktivitesi olmayan bir dizi metabolitle sonu�lanm��t�r. Sistemik metabolit maruziyeti d���kt�r.
Vilanterol
In vitro �al��malar, vilanterol�n daha �ok sitokrom P450 3A4 (CYP3A4) taraf�ndan metabolize edildi�ini ve P-gp transporteri i�in bir substrat oldu�unu g�stermi�tir. Primer metabolik yollar, anlaml� olarak d���k betave betaadrenerjik agonist aktivitesi olan bir dizi metabolite O- dealkilasyondur. �nsanlarda radyoaktif i�aretli madde ile yap�lan oral vilanterol uygulamas�n� takiben plazma metabolik profilleri, y�ksek ilk ge�i� metabolizmas� ile tutarl�d�r. Sistemik metabolit maruziyeti d���kt�r.
Eliminasyon
Umeklidinyum
�ntraven�z uygulamay� takiben plazma klirensi 151 litre/saattir. �ntraven�z uygulamay� takiben, uygulanan radyoaktif i�aretli dozun yakla��k %58'i (ya da geri kazan�lan radyoaktivitenin
%73'�) doz sonras� 192 saatte d��k� ile at�lm��t�r. �riner eliminasyon, 168. saatte uygulanan radyoaktif i�aretli dozun %22'sine (geri kazan�lan radyoaktivitenin %27'si) kar��l�k gelmektedir. �ntraven�z dozlam� takiben ila�la ilgili maddelerin d��k� ile at�lmas�, safraya sal�m� g�stermi�tir. Sa�l�kl� erkek g�n�ll�lerde oral uygulamay� takiben, toplam radyoaktivite, doz sonras� 168 saatte daha �ok d��k� ile at�lm��t�r (uygulanan radyoaktif i�aretli dozun yakla��k
%92'si ya da geri kazan�lan radyoaktivitenin %99'u). Oral olarak uygulanan dozun %1'inden az� (geri kazan�lan radyoaktivitenin %1'i) idrarla at�lm��t�r ve bu da oral uygulamay� takiben �nemsiz d�zeyde emilim oldu�unu g�stermi�tir. 10 g�n boyunca uygulanan inhale dozlam� takiben umeklidinyum plazma eliminasyon yar� �mr� ortalama 19 saat olup ilac�n %3'� ila
%4'� kararl� durumda idrarda de�i�meden at�lm��t�r.
Vilanterol
�ntraven�z uygulamay� takiben vilanterol�n plazma klirensi 108 litre/saattir. Radyoaktif i�aretli
vilanterol�n oral uygulamas�n� takiben, k�tle dengesi, radyoaktif i�aretin %70'inin idrarda ve
%30'unun d��k�da oldu�unu g�stermi�tir. Vilanterol�n primer eliminasyonu, metabolizmay� takiben idrar ve d��k�da metabolitelerin at�l�m� ile ger�ekle�tirilmi�tir. 10 g�n boyunca inhale dozlam� takiben vilanterol plazma eliminasyon yar� �mr� ortalama 11 saattir.
Do�rusall�k/Do�rusal olmayan durum:
Veri bulunmamaktad�r.
Hastalardaki karakteristik �zellikler
Geriyatrik pop�lasyon:
Yap�lan bir pop�lasyon farmakokinetik analizi, umeklidinyum ve vilanterol farmakokineti�inin 65 ya� ve �zeri ve 65 ya��n alt�ndaki KOAH hastalar� aras�nda benzer oldu�unu g�stermi�tir.
B�brek yetmezli�i:
�iddetli b�brek yetmezli�i bulunan hastalarda, �nerilen dozun iki kat� umeklidinyum ve �nerilen dozda vilanterol i�eren umeklidinyum/vilanterol uygulamas�ndan sonra sistemik umeklidinyum ya da vilanterol maruziyetinde herhangi bir art�� oldu�una (Cve EAA) ve �iddetli b�brek yetmezli�i bulunan hastalar ve sa�l�kl� g�n�ll�ler aras�nda de�i�en protein ba�lanma profili g�r�ld���ne dair herhangi bir kan�t mevcut de�ildir.
Karaci�er yetmezli�i:
Orta d�zeyde karaci�er yetmezli�i (Child-Pugh Class B) bulunan hastalarda, �nerilen dozun iki kat� umeklidinyum ve �nerilen dozda vilanterol i�eren umeklidinyum/vilanterol uygulamas�ndan sonra sistemik umeklidinyum ya da vilanterol maruziyetinde herhangi bir art�� oldu�una (Cve EAA) ve orta d�zeyde karaci�er yetmezli�i bulunan hastalar ve sa�l�kl� g�n�ll�ler aras�nda de�i�en protein ba�lanma profili g�r�ld���ne dair herhangi bir kan�t mevcut de�ildir. Umeklidinyum/vilanterol, �iddetli karaci�er yetmezli�i bulunan hastalarda de�erlendirilmemi�tir.
Di�er �zel pop�lasyonlar:
Yap�lan bir pop�lasyon farmakokinetik analizi, ya�, �rk, cinsiyet, inhale kortikosteroid kullan�m� ya da v�cut a��rl���n�n etkisi dikkate al�narak umeklidinyum ya da vilanterol i�in herhangi bir doz ayarlamas� gerekmedi�ini g�stermi�tir. Zay�f CYP2D6 metabolize edicilere ili�kin bir �al��ma, sistemik umeklidinyum maruziyeti �zerinde CYP2D6 genetik polimorfizminin klinik olarak anlaml� herhangi bir etki olu�turmad���n� g�stermi�tir.
5.3. Klinik �ncesi g�venlilik verileri
Tek ba�lar�na ve kombinasyon halinde umeklidinyum ve vilanterol ile yap�lan klinik d��� �al��malarda, bulgular tipik olarak, s�ras�yla muskarinik resept�r antagonisti ya da betaadrenerjik agonistlerin primer farmakolojisi ve/veya lokal tahri� ile ili�kilendirilmi�tir. A�a��daki ifadeler her bir bile�ene ili�kin ger�ekle�tirilmi� olan �al��malar� yans�tmaktad�r.
Genotoksisite ve karsinojenisite:
Umeklidinyum standart �al��malarda genotoksik de�ilken EAA'ya g�re, umeklidinyum 55 mikrogram�n insan klinik maruziyetinin s�ras�yla 26 ya da 22 kat� maruziyet d�zeylerinde farelerde ya da s��anlarda ger�ekle�tirilen ya�am boyu inhalasyon �al��malar�nda da karsinojenik olmad��� g�r�lm��t�r.
Genetik toksisite �al��malar�nda vilanterol (alfa-fenilsinnamat olarak) ve trifenilasetik asit genotoksik de�ildi ve bu da vilanterol�n insanlar i�in genotoksik bir risk olu�turmad���n� g�stermektedir. Di�er betaadrenerjik agonistlere y�nelik bulgularla tutarl� olarak, ya�am boyu inhalasyon �al��malar�nda vilanterol, di�i s��an ve fare �reme yolunda ve s��an hipofiz bezinde proliferatif etkilere yol a�m��t�r. EAA'ya dayanarak, vilanterol 22 mikrogram�n insan klinik maruziyetinin s�ras�yla 0,5 ya da 13 kat� maruziyet d�zeylerinde s��anlarda ya da farelerde g�r�len t�m�r insidans�nda herhangi bir art�� olmam��t�r.
�reme toksisitesi:
Umeklidinyum s��anlar veya tav�anlarda teratojenik olmam��t�r. 180 mikrogram/kg/g�n (EAA'ya g�re insan�n 55 mikrogram umeklidinyuma klinik maruziyetinin yakla��k 80 kat�) dozu verilen annelerde yap�lan bir pre ve post natal �al��mada, s��anlara yap�lan subk�tan umeklidinyum uygulamas�, annede daha d���k v�cut a��rl��� art��� ve besin t�ketimi ile sonu�lanm��t�r ve yavrunun v�cut a��rl���n� s�tten kesmeden �nce hafif�e azaltm��t�r.
Vilanterol, s��anlarda teratojenik �zellik g�stermemi�tir. Tav�anlarda yap�lan inhalasyon �al��malar�nda, vilanterol, EAA'ya g�re klinik insan maruziyetinin 6 kat�nda di�er betaadrenerjik agonistler ile g�r�lenlere benzer etkiler yaratm��t�r (yar�k damak, g�z kapa��nda a��lma, sternebral f�zyon ve ekstremite fleks�r�/malrotasyon). Vilanterol 22 mikrogram subk�tan olarak verildi�inde, EAA'ya dayal� klinik insan maruziyetinin 36 kat�nda hi�bir etki g�r�lmemi�tir.
6. FARMAS�T�K �ZELL�KLER
6.1. Yard�mc� maddelerin listesi
Laktoz monohidrat (inek s�t�nden elde edilir.) Magnezyum stearat
6.2. Ge�imsizlikler
Bilinen bir ge�imsizli�i bulunmamaktad�r.
6.3. Raf �mr�
24 ay
Al�minyum kutu a��ld�ktan sonraki raf �mr�: ��inde bulundu�u al�minyum kutudan
��kar�ld�ktan sonra 30ºC'nin alt�ndaki oda s�cakl���nda 6 hafta.
�nhaler al�minyum kutudan ��kar�l�r ��kar�lmaz etiketi �zerinde bulunan bo�lu�a inhalerin son kullanma tarihi yaz�l�r.
6.4. Saklamaya y�nelik �zel tedbirler
30ºC alt�ndaki oda s�cakl���nda ve kuru bir yerde muhafaza ediniz.
�nhaleri nemden korumak i�in kapal� al�minyum kutu i�inde muhafaza ediniz ve ancak ilk kez kullanmaya ba�layaca��n�z zaman al�minyum kutuyu a��p inhalerinizi i�inden ��kar�n�z.
Al�minyum kutu a��ld�ktan sonra inhaler en fazla 6 hafta kullan�labilir. �nhaler al�minyum kutudan ��kar�l�r ��kar�lmaz etiketi �zerinde bulunan bo�lu�a inhalerin son kullanma tarihi yaz�l�r. �nhalerin son kullanma tarihi al�minyum kutunun a��lmas�ndan sonra 6 haftad�r. Etiket �zerine yaz�lan son kullanma tarihinden sonra inhaler kullan�lmamal�d�r. Folyo, al�minyum kutu a��ld�ktan sonra at�labilir.
6.5. Ambalaj�n niteli�i ve i�eri�i
Plastik inhaler, nem �ekici paket i�eren bir al�minyum kutu i�erisinde paketlenmi� olan a��k gri renkli bir g�vde, k�rm�z� renkli inhaler kapa�� ve bir doz sayac�ndan olu�maktad�r. Al�minyum kutu, s�yr�labilen bir folyo kapak ile kapat�lm��t�r. �nhalerde 30 dozluk kullan�ma haz�r blisterden olu�an, her biri beyaz bir toz i�eren iki al�minyum folyo �erit bulunmaktad�r.
6.6. Be�eri t�bbi �r�nden arta kalan maddelerin imhas� ve di�er �zel �nlemler
Kullan�lmam�� olan �r�nler ya da at�k materyaller “T�bbi At�klar�n Kontrol� Y�netmeli�i” ve “Ambalaj At�klar�n�n Kontrol� Y�netme�i”ne uygun olarak imha edilmelidir.
 Belso�uklu�u, Chlamydia ve Frengi
Belso�uklu�u, bakterilerin sebep oldu�u bir enfeksiyondur. Cinsel ili�ki
yoluyla bula��r ve d�lyata�� boynunda, idrar yollar�nda, an�ste, makatta ve
bo�azda enfeksyona sebep olabilir.
Belso�uklu�u, Chlamydia ve Frengi
Belso�uklu�u, bakterilerin sebep oldu�u bir enfeksiyondur. Cinsel ili�ki
yoluyla bula��r ve d�lyata�� boynunda, idrar yollar�nda, an�ste, makatta ve
bo�azda enfeksyona sebep olabilir. |
 G�da Alerjisi
Her y�l milyonlarca insan yiyeceklere alerji g�steriyor.
G�da Alerjisi
Her y�l milyonlarca insan yiyeceklere alerji g�steriyor. |
�LA� E�DE�ERLER�
| E�de�er �la� Ad� | Barkodu | �la� Fiyat� |
|---|---|---|
| LAVENTAIR | 8699240550745 | |
| Di�er E�de�er �la�lar |
 |
Parkinson Hastal��� Hastal�k ilk kez 1817 de �ngiliz doktor James Parkinson taraf�ndan tan�mlanm�� ve Dr. Parkinson hastal��� “sallay�c� fel�” olarak kaleme alm��. |
 |
A��z Kanseri A��z kanserinin en yayg�n t�rleri, dudak, dil, di�etidir. Nadiren yanak i�i veya damak b�lgelerini de i�ine al�r. |
 |
Do�um Sonras� Depresyonu Do�um sonras� depresyonu, do�umdan sonra her on kad�ndan biri taraf�ndan tecr�be edilen stresli bir durumdur. |
�LA� GENEL B�LG�LER�
Glaxo Smith Kline �la�lar� San.Ve Tic.A.�
| Geri �deme Kodu | A16378 |
| Sat�� Fiyat� | 1285.46 TL [ 4 May 2026 ] |
| �nceki Sat�� Fiyat� | 1285.46 TL [ 27 Apr 2026 ] |
| Original / Jenerik | Original �la� |
| Re�ete Durumu | Normal Re�eteli bir ila�d�r. |
| Barkodu | 8699522557660 |
| Etkin Madde | Umeklidinyum Bromur + Vilanteral |
| ATC Kodu | R03AL03 |
| Birim Miktar | 62,5+25 |
| Birim Cinsi | MCG |
| Ambalaj Miktar� | 30 |
| Solunum Sistemi > Adrenerjikler (�nhalan) |
| �thal ( ref. �lke : Ingiltere ) ve Be�eri bir ila�d�r. |