TAFINLAR 50 mg 120 kapsül { Novartis } Farmakolojik Özellikler
{ Dabrafenib }
5. FARMAKOLOJİK ÖZELLİKLER
5.1. Farmakodinamik özellikler
Farmakoterapötik grup: Antineoplastik ajanlar, protein kinaz inhibitörleri, B-Raf serin-treonin kinaz (BRAF) inhibitörleri.
ATC kodu: L01EC02
Etki mekanizması
TAFİNLAR, RAF kinazlarının inhibitörüdür. BRAF'deki onkojenik mutasyonlar RAS/RAF/MEK/ERK yolağının yapısal aktivasyonuna yol açar. BRAF mutasyonları, melanomda yaklaşık %50 olmak üzere spesifik kanserlerde de yüksek frekansta tespit edilmiştir. En sık gözlenen BRAF mutasyonu, melanomda görülen BRAF mutasyonlarının yaklaşık %90'ını oluşturan V600E'dir.
Biyokimyasal testlerden elde edilen preklinik veriler, TAFİNLAR'ın kodon 600 mutasyonlarını aktive ederek BRAF kinazları inhibe ettiğini göstermiştir (Tablo 3).
Tablo 3 TAFİNLAR'ın RAF kinazlara karşı kinaz inhibe edici etkinliği
Kinaz | İnhibe edici konsantrasyon 50 (IC50 nM) |
BRAF V600E | 0,65 |
BRAF V600K | 0,50 |
BRAF V600D | 1,8 |
BRAF WT | 3,2 |
CRAF WT | 5,0 |
İn vitro ve hayvan modellerinde, TAFİNLAR BRAF V600 mutant melanom hücre dizilerinde hücre büyümesini engellemiş ve farmakodinamik bir biyolojik aşağı akım belirtecinin (fosforile ERK) baskılanmasını göstermiştir. BRAF V600 mutasyon pozitif melanomu olan hastalarda TAFİNLAR verilmesi başlangıca göre tümör fosforile ERK'nin inhibisyonuna yol açmıştır.
Trametinib ile kombinasyon
Trametinib mitojen-tarafından aktive edilen ekstrasellüler sinyalle regüle edilen kinaz 1 (MEK1) ve MEK2 aktivasyonunun ve kinaz aktivitesinin geri dönüşlü, yüksek düzeyde seçici, allosterik bir inhibitörüdür. MEK proteinleri, ekstrasellüler sinyalle-ilişkili kinaz (ERK) yolağının bileşenleridir. Bu şekilde trametinib ve TAFİNLAR bu yolakta iki kinazı (MEK ve RAF) inhibe eder ve dolayısıyla kombinasyon, yolakta eşzamanlı inhibisyon sağlar. TAFİNLAR+trametinib kombinasyonunun in vitro ortamda BRAF V600 mutasyonu pozitif melanom hücre dizilerinde anti-tümör aktiviteye sahip olduğu ve in vivo ortamda BRAF V600 mutasyonu pozitif melanom ksenograftlarında direnç gelişimini geciktirdiği gösterilmiştir.
BRAF mutasyon durumunun tespiti
TAFİNLAR veya trametinib ile kombinasyon olarak alınmasından önce geçerliliği kanıtlanmış bir test ile hastaların BRAF V600 mutasyon pozitif tümör durumu doğrulanmalıdır. Faz II ve III klinik çalışmalarda uygunluk taraması için, en son tümör örneğinde BRAF mutasyon değerlendirme testi kullanılarak merkezi BRAF V600
mutasyonunun değerlendirmesi gereklidir. Primer tümör veya metastatik bir alandan tümör sadece araştırma amaçlı geliştirilmiş (IUO) bir test ile değerlendirilmiştir. IUO, formalin ile fikse edilmiş parafine batırılmış (FFPE) tümör dokudan elde edilmiş DNA'ya uygulanmış allele özgü polimeraz zincir reaksiyonu (PCR) testidir. Test özellikle V600E ve V600K mutasyonları arasında ayırım yapmak üzere özel olarak geliştirilmiştir. Sadece BRAF V600E veya V600K mutasyonu pozitif tümörleri olan hastalar bu çalışmaya katılmak üzere uygun bulunmuştur.
Sonrasında tüm hasta örnekleri CE işareti taşıyan geçerliliği oluşturulmuş bioMerieux (bMx) THxID BRAF testi kullanılarak yeniden test edilmiştir. bMx THxID BRAF testi, FFPE tümör dokusundan alınan DNA üzerinde uygulanan alele özgün bir PCR'dır. Test BRAF V600E ve V600K mutasyonlarını yüksek bir duyarlılıkla tespit edecek şekilde tasarlanmıştır (FFPE dokusundan alınan DNA kullanılarak yabanıl tip sıralamasından oluşan bir tabanda %5 V600E ve V600K sekansına inerek). Geriye dönük iki-yönlü Sanger sıralama analizleriyle yapılan klinik-dışı ve klinik çalışmalar testin daha az yaygın BRAF V600D mutasyonunu ve V600E/K601E mutasyonunu da daha düşük bir duyarlılıkla tespit ettiğini göstermiştir. Klinik- dışı ve klinik çalışmalarda THxID BRAF testiyle mutasyon pozitif çıkan, ardından referans yöntem kullanılarak sıralaması yapılan örneklerde (n=876) testin özgünlüğünün %94 olduğu saptanmıştır.
Klinik etkililik ve güvenlilik
Rezeke edilemeyen veya metastatik melanom Trametinib ile kombinasyon halinde TAFİNLAR Önceden tedavi görmemiş hastalar
BRAF V600 mutasyonlu rezeke edilemeyen veya metastatik melanomlu yetişkin hastaların tedavisinde TAFİNLAR (günde iki kez 150 mg) ile kombinasyon halinde trametinib (günde bir kez 2 mg) için önerilen dozun etkililiği ve güvenliliği iki Faz III çalışmada ve bir destekleyici Faz I/II çalışmada çalışılmıştır.
MEK115306 (COMBI-d)
MEK115306 rezeke edilemeyen (Evre IIIC) veya metastatik (Evre IV) BRAF V600E/K mutasyonu pozitif kutanöz melanomu olan gönüllüler için birinci basamak tedavi olarak TAFİNLAR ve trametinib kombinasyonunun TAFİNLAR ve plasebo ile karşılaştırıldığı bir Faz III, randomize, çift kör çalışmadır. Çalışmanın birincil sonlanım noktası progresyonsuz sağkalım (PFS) ve kritik ikincil sonlanım noktası Genel Sağkalım (OS) olmuştur. Gönüllüler laktat dehidrogenaz (LDH) düzeyi (≤ normalin üst sınırına (ULN) karşı > ULN) ve BRAF mutasyonuna (V600K'ya karşı V600E) göre sınıflandırılmıştır.
Toplam 423 gönüllü kombinasyon tedavisi (N=211) ya da TAFİNLAR (N=212) almak üzere 1:1 oranında randomize edilmiştir. Hastaların çoğu Beyaz (>%99) ve erkek (%53) olup medyan yaş 56'dır (%28'i ≥65 yaşındadır). Hastaların büyük çoğunluğu Evre IV M1c hastalığa (%67) sahiptir. Çoğu hastada başlangıçta LDH ≤ ULN (%65), ECOG performans durumu 0'dır (%72) ve bir viseral hastalık vardır (%73). Hastaların büyük çoğunlunda BRAF V600E mutasyonu söz konusudur (%85). Beyin metastazları olan gönüllüler çalışmaya dahil edilmemiştir.
Medyan OS ve tahmini 1 yıllık, 2 yıllık, 3 yıllık, 4 yıllık ve 5 yıllık sağkalım oranları Tablo 4'te sunulmaktadır. 5 yılda gerçekleştirilen bir OS analizinde, kombinasyon kolu için medyan
OS, TAFİNLAR monoterapisine kıyasla yaklaşık 7 ay daha uzun olmuş (18,7 aya karşı 25,8 ay), 5 yıllık sağkalım oranları TAFİNLAR monoterapisi için %27'ye karşılık kombinasyon için %32 bulunmuştur (Tablo 4, Şekil 1). Kaplan-Meier OS eğrisinin 3 ila 5 yıl arasında stabilize olduğu görülmektedir (bkz. Şekil 1). Beş yıllık genel sağkalım oranı, tedavi başlangıcında laktat dehidrojenaz düzeyleri normal olan hastalar için kombinasyon kolunda
%40 (%95 GA: 31,2; 48,4) iken, TAFİNLAR monoterapi kolunda %33 (%95 GA: 25,0; 41,0) olmuştur; başlangıç laktat dehidrojenaz düzeyleri yüksek olan hastalar için ise TAFİNLAR monoterapi kolunda %14'e (%95 GA: 6,8; 23,1) karşı kombinasyon kolunda %16 (%95 GA:
8,4; 26,0) bulunmuştur.
Tablo 4 Çalışma MEK115306 (COMBI-d) için Genel Sağkalım sonuçları
OS analizi (veri kesme tarihi: 12 Ocak 2015) | 5 yıllık OS analizi (veri kesme tarihi: 10 Aralık 2018) | |||
| TAFİNLAR + trametinib (n=211) | TAFİNLAR + Plasebo (n=212) | TAFİNLAR + trametinib (n=211) | TAFİNLAR + Plasebo (n=212) |
Hasta sayısı |
|
|
|
|
Ölen (olay), n (%) | 99 (47) | 123 (58) | 135 (64) | 151 (71) |
OS tahminleri (ay) | ||||
Medyan (%95 GA) | 25,1 (19,2; NR) | 18,7 (15,2; 23,7) | 25,8 (19,2; 38,2) | 18,7 (15,2; 23,1) |
Tehlike oranı (%95 GA) | 0,71 (0,55; 0,92) | 0,80 (0,63; 1,01) | ||
p değeri | 0,011 | NA |
| |
Genel sağkalım tahmini, % (%95 GA) | TAFİNLAR + trametinib (n=211) | TAFİNLAR + Plasebo (n=212) | ||
1 yılda | 74 (66,8; 79,0) | 68 (60,8; 73,5) | ||
2 yılda | 52 (44,7; 58,6) | 42 (35,4; 48,9) | ||
3 yılda | 43 (36,2; 50,1) | 31 (25,1; 37,9) | ||
4 yılda | 35 (28,2; 41,8) | 29 (22,7; 35,2) | ||
5 yılda | 32 (25,1; 38,3) | 27 (20,7; 33,0) | ||
NR = Ulaşılmadı, NA = Geçerli değil |
| |||
Tahmini Sağkalım Fonksiyonu
Şekil 1 Çalışma MEK115306 için Kaplan-Meier genel sağkalım eğrileri (ITT Popülasyonu)
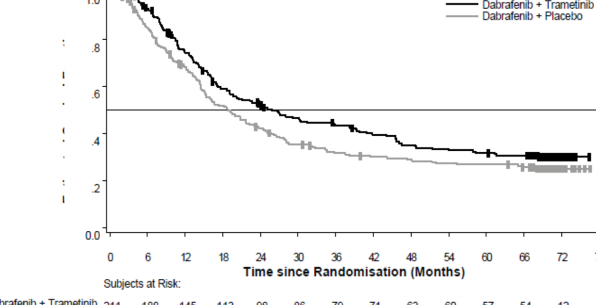
Randomizasyondan İtibaren Geçen Süre (Ay)
Riskteki gönüllüler:
Birincil sonlanım noktası PFS'de sağlanan iyileşmeler, TAFİNLAR monoterapisine kıyasla, kombinasyon kolunda 5 yıllık bir zaman dilimi içinde sürdürülmüştür. Genel yanıt oranı (ORR) için de iyileşmeler gözlenmiştir ve kombinasyon kolunda TAFİNLAR monoterapisine kıyasla daha uzun bir yanıt süresi (DoR) izlenmiştir (Tablo 5).
Tablo 5 MEK115306 (COMBI-d) çalışmasının etkililik sonuçları
| Birincil analiz (veri kesme tarihi: 26 Ağustos 2013) | Güncellenmiş analiz (veri kesme tarihi: 12 Ocak 2015) | 5 yıllık analiz (veri kesme tarihi: 10 Aralık 2018) | |||
Sonlanım noktası | TAFİNLAR + Trametinib (n=211) | TAFİNLAR + Plasebo (n=212) | TAFİNLAR + Trametinib (n=211) | TAFİNLAR + Plasebo (n=212) | TAFİNLAR + Trametinib (n=211) | TAFİNLAR + Plasebo (n=212) |
PFS |
|
| ||||
Progresif hastalık veya ölüm, n (%) | 102 (48) | 109 (51) | 139 (66) | 162 (76) | 160 (76) | 166 (78) |
Medyan PFS (ay) (%95 GA) | 9,3 (7,7; 11,1) | 8,8 (5,9; 10,9) | 11,0 (8,0; 13,9) | 8,8 (5,9; 9,3) | 10,2 (8,1; 12,8) | 8,8 (5,9; 9,3) |
Tehlike oranı (%95 GA) | 0,75 (0,57; 0,99) | 0,67 (0,53; 0,84) | 0,73 (0,59; 0,91) | |||
P değeri | 0,035 | <0,001 | NA | |||
ORR % (%95 GA) | 67 (59,9; 73,0) | 51 (44,5; 58,4) | 69 (61,8; 74,8) | 53 (46,3; 60,2) | 69 (62,5; 75,4) | 54 (46,8; 60,6) |
ORR farkı (%95 GA) | 15 (5,9; 24,5) | 15 (6,0; 24,5) | NA | |||
P değeri | 0,0015 | 0,0014 | NA | |||
DoR (ay) Medyan (%95 GA) |
9,2 (7,4; NR) |
10,2 (7,5; NR) |
12,9 (9,4; 19,5) |
10,6 (9,1; 13,8) |
12,9 (9,3; 18,4) |
10,2 (8,3; 13,8) |
a - Progresyonsuz Sağkalım (araştırıcı tarafından değerlendirilen)
b - Genel Yanıt Oranı = Tam Yanıt + Kısmi Yanıt
c - Yanıt Süresi
d - Bildirim zamanında araştırıcı tarafından değerlendirilen yanıtların çoğu (≥ %59) halen devam etmektedir
e - Yuvarlanmamış ORR bulgusu temelinde hesaplanmış ORR farkı
f - Güncellenmiş analiz önceden planlı değildir ve p değeri çoklu test için düzeltilmemiştir NR = Ulaşılmamıştır
NA = Geçerli değildir
MEK116513 (COMBI-v)
MEK116513 çalışması, BRAF V600 mutasyonu pozitif rezeke edilemeyen veya metastatik melanomda TAFİNLAR ve trametinib kombinasyon tedavisini vemurafenib monoterapisi ile karşılaştıran 2 kollu, randomize, açık etiketli bir Faz III çalışmadır. Çalışmanın birincil sonlanım noktası genel sağkalım olup kritik ikincil sonlanım noktası PFS'dir. Gönüllüler laktat dehidrogenaz (LDH) düzeyi (≤ normalin üst sınırına (ULN) karşı >ULN) ve BRAF mutasyonuna (V600K'ya karşı V600E) göre sınıflandırılmıştır.
Toplam 704 gönüllü kombinasyon ya da vemurafenib almak üzere 1:1 oranında randomize edilmiştir. Hastaların çoğu Beyaz (>%96) ve erkek (%55) olup medyan yaş 55'tir (%24'ü ≥ 65 yaşındadır). Hastaların büyük çoğunluğu Evre IV M1c hastalığa (%61 genel) sahiptir. Çoğu hastada başlangıçta LDH ≤ ULN (%67), ECOG performans durumu 0'dır (%70) ve bir viseral hastalık vardır (%78). Genel olarak gönüllülerin %54'ünde çalışma başlangıcında < 3 hastalık bölgesi vardır. Hastaların büyük çoğunlunda BRAF V600E mutasyonu pozitif melanom söz konusudur (%89). Beyin metastazları olan gönüllüler çalışmaya dahil edilmemiştir.
Medyan OS ve tahmini 1 yıllık, 2 yıllık, 3 yıllık, 4 yıllık ve 5 yıllık sağkalım oranları Tablo 6'da sunulmaktadır. 5 yılda gerçekleştirilen bir OS analizinde, kombinasyon kolu için ortalama OS, vemurafenib monoterapisine göre yaklaşık 8 ay daha uzun olmuş (17,8 aya karşı 26,0 ay), 5 yıllık sağkalım oranları vemurafenib monoterapisi için %23'e karşılık kombinasyon için %36 bulunmuştur (Tablo 6, Şekil 2). Kaplan-Meier OS eğrisinin 3 ila 5 yıl arasında stabilize olduğu görülmektedir (bkz. Şekil 2). Beş yıllık genel sağkalım oranı, tedavi başlangıcında laktat dehidrojenaz düzeyleri normal olan hastalar için kombinasyon kolunda
%46 (%95 GA: 38,8; 52,0) iken, vemurafenib monoterapi kolunda %28 (%95 GA: 22,5; 34,6) olmuştur; başlangıç laktat dehidrojenaz düzeyleri yüksek olan hastalar için ise vemurafenib monoterapi kolunda %10'a (%95 GA: 5,1; 17,4) karşı kombinasyon kolunda %16 (%95 GA:
9,3; 23,3) bulunmuştur.
Tablo 6 Çalışma MEK116513 (COMBI-v) için Genel Sağkalım sonuçları
OS analizi (veri kesme tarihi: 13 Mart 2015) | 5 yıllık OS analizi (veri kesme tarihi: 08 Ekim 2018) | |||
| TAFİNLAR + Trametinib (n=352) | Vemurafenib (n=352) | TAFİNLAR + Trametinib (n=352) | Vemurafenib (n=352) |
Hasta sayısı |
|
|
|
|
Ölen (olay), n (%) | 155 (44) | 194 (55) | 216 (61) | 246 (70) |
OS tahminleri (ay | ) |
|
|
|
Medyan (%95 GA) | 25,6 (22,6; NR) | 18,0 (15,6; 20,7) | 26,0 (22,1; 33,8) | 17,8 (15,6; 20,7) |
Düzeltilmiş tehlike oranı (%95 GA) | 0,66 (0,53; 0,81) | 0,70 (0,58; 0,84) | ||
p değeri | <0,001 |
| NA |
|
Genel sağkalım tahmini, % (%95 GA) | TAFİNLAR + Trametinib (n=352) | Vemurafenib (n=352) | ||
1 yılda | 72 (67; 77) | 65 (59; 70) | ||
2 yılda | 53 (47,1; 57,8) | 39 (33,8; 44,5) | ||
3 yılda | 44 (38,8; 49,4) | 31 (25,9; 36,2) | ||
4 yılda | 39 (33,4; 44,0) | 26 (21,3; 31,0) | ||
5 yılda | 36 (30,5; 40,9) | 23 (18,1; 27,4) | ||
NR = Ulaşılmamıştır, NA = Geçerli değildir |
| |||
Şekil 2 MEK116513 çalışması için güncel OS analizinin Kaplan-Meier eğrileri
Estimated Survival Function
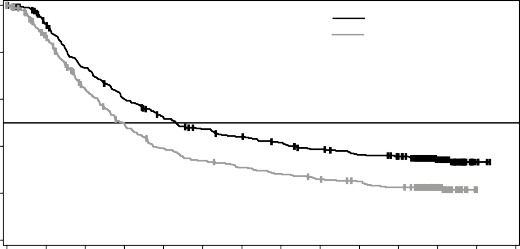
![]()
Tahmini Sağkalım Fonksiyonu
Time since Randomisation (Months)
![]()
Randomizasyondan İtibaren Geçen Süre (Ay)
İkincil sonlanım noktası PFS'de sağlanan iyileşmeler, vemurafenib monoterapisine kıyasla, kombinasyon kolunda 5 yıllık bir zaman dilimi içinde sürdürülmüştür. Genel yanıt oranı (ORR) için de iyileşmeler gözlenmiştir ve kombinasyon kolunda vemurafenib monoterapisine kıyasla daha uzun bir DoR izlenmiştir (Tablo 7).
Tablo 7 MEK116513 (COMBI-v) çalışması için etkililik sonuçları
| Birincil analiz (Veri kesme tarihi: 17 Nisan 2014) | 5 yıllık analiz (Veri kesme tarihi: 08 Ekim 2018) | ||
Sonlanım noktası | TAFİNLAR + Trametinib (n=352) | Vemurafenib (n=352) | TAFİNLAR + Trametinib (n=352) | Vemurafenib (n=352) |
PFS |
|
| ||
Progresif hastalık veya ölüm, n (%) | 166 (47) | 217 (62) | 257 (73) | 259 (74) |
Medyan PFS (ay) (%95 GA) | 11,4 (9,9; 14,9) | 7,3 (5,8; 7,8) | 12,1 (9,7; 14,7) | 7,3 (6,0; 8,1) |
Tehlike oranı (%95 GA) | 0,56 (0,46; 0,69) | 0,62 (0,52; 0,74) | ||
P değeri | <0,001 | NA | ||
| Birincil analiz (Veri kesme tarihi: 17 Nisan 2014) | 5 yıllık analiz (Veri kesme tarihi: 08 Ekim 2018) | ||
Sonlanım noktası | TAFİNLAR + Trametinib (n=352) | Vemurafenib (n=352) | TAFİNLAR + Trametinib (n=352) | Vemurafenib (n=352) |
ORR % (%95 GA) | 64 (59,1; 69,4) | 51 (46,1; 56,8) | 67 (62,2; 72,2) | 53 (47,2; 57,9) |
ORR farkı (%95 GA) | 13 (5,7; 20,2) | NA | ||
p değeri | 0,0005 | NA | ||
DoR (ay) Medyan (%95 GA) |
13,8 (11,0; NR) |
7,5 (7,3; 9,3) |
13,8 (11,3; 18,6) |
8,5 (7,4; 9,3) |
a – Progresyonsuz sağkalım (araştırmacı tarafından değerlendirilen) b – Genel Yanıt Oranı = Tam Yanıt + Kısmi Yanıt c – Yanıt süresi d – Raporlama sırasında, araştırmacı tarafından değerlendirilen yanıtların çoğunluğu (TAFİNLAR+trametinib %59 ve vemurafenib %42) halen devam etmektedir NR = Ulaşılmamıştır NA = Geçerli değildir | ||||
Önceki BRAF inhibitör tedavisi
Önceki BRAF inhibitör tedavisinde progrese olmuş hastalarda TAFİNLAR+trametinib kombinasyonu ile sınırlı veri mevcuttur.
BRF113220 çalışması Bölüm B, bir BRAF inhibitör tedavisinde progrese olmuş 26 hastadan oluşan bir grubu içermiştir. Trametinib 2 mg QD ve TAFİNLAR 150 mg BID kombinasyonu, bir BRAF inhibitörü tedavisinde progrese olan hastalarda sınırlı klinik aktivite göstermiştir. Araştırmacı tarafından değerlendirilen doğrulanmış yanıt oranı %15 (%95 GA: 4,4, 34,9) ve
medyan PFS 3,6 ay (%95 GA: 1,9, 5,2) bulunmuştur. Bu çalışmanın C Bölümünde TAFİNLAR monoterapisinden trametinib 2 mg QD+TAFİNLAR 150 mg BID kombinasyonuna geçiş yapan 45 hastada da benzer sonuçlar görülmüştür. Bu hastalarda 3,6 ay (%95 GA: 2, 4) medyan PFS ile %13'lük (%95 GA: 5,0, 27,0) bir doğrulanmış yanıt oranı gözlenmiştir.
Beyin metastazları olan hastalar:
Beyne metastaz yapmış BRAF V600 mutant-pozitif melanomu olan hastalarda trametinib ile kombinasyon halinde TAFİNLAR'ın etkililik ve güvenliliği, randomize olmayan, açık etiketli, çok merkezli bir Faz II çalışmada (COMBI-MB çalışması) incelenmiştir. Toplam 125 hasta dört kohorta kaydedilmiştir:
Kohort A: Daha önce beyin hedefli lokal tedavinin yapılmadığı, asemptomatik beyin metastazları ile birlikte BRAFV600E mutant melanomun olduğu, ECOG performans durumu 0 ya da 1 olan hastalar.
5.2. Farmakokinetik özellikler
Genel ÖzelliklerEmilim:
TAFİNLAR oral olarak emilir. Dozdan 2 saat sonra pik plazma konsantrasyonuna ulaşır. Oral TAFİNLAR'ın ortalama mutlak biyoyararlanımı %95'dir (%90 GA: %81, %110). TAFİNLAR maruziyeti (Cve EAA) doz ile orantılı olarak 12 ve 300 mg tek doz olarak verilmesinden sonra artmıştır, fakat bu artış günde 2 kez tekrarlanan doz alımından sonraki artıştan daha azdır. Tekrarlanan dozlar ile maruziyette bir azalma gözlemlenmiştir; bu da kendi metabolizmasının indüklenmesine bağlı olabilir. Ortalama birikim EAA Gün 18/Gün 1 oranları 0,73'dür. Günde 2 kez 150 mg verilmesinden sonra, geometrik ortalama C, EAA(0-Ï„) ve predoz konsantrasyonu (CÏ„) sırasıyla 1478 ng/ml, 4341 ng*sa/ml ve 26 ng/ml'dir.
TAFİNLAR'ın yiyecekler ile birlikte verilmesi biyoyararlanımı (Cve EAA sırasıyla %51 ve %31 düşer) azaltmıştır ve açlık durumu ile karşılaştırıldığında TAFİNLAR kapsüllerinin absorpsiyonunu geciktirmiştir.
Dağılım:
TAFİNLAR birincil olarak insan plazma proteinine bağlanır (%99,7 bağlı). İntravenöz mikrodoz verilmesinden sonra dağılımın sabit durum hacmi 46 L'dir.
Biyotransformasyon:
TAFİNLAR metabolizması birincil olarak CYP2C8 ve CYP3A4 aracılığıyla hidroksi- dabrafenib oluşturmaktadır; bu ise daha sonra CYP3A4 aracılığıyla karboksi dabrafenib oluşturmak üzere oksitlenir. Karboksi-dabrafenib enzimatik olmayan bir işlem ile desmetil dabrafenib oluşturmak üzere dekarboksillenir. Karboksi-dabrafenib safra ve idrarda atılır. Desmetil-dabrafenib bağırsaklarda oluşur ve tekrar emilir.
Desmetil-dabrafenib CYP3A4 aracılığıyla oksidatif metabolitlerine metabolize olur. Hidroksi- dabrafenib terminal yarılanma ömrü ana ürünün yarılanma ömrü olan 10 saate paralel iken karboksi- ve desmetil- metabolitleri daha uzun yarılanma ömrüne sahiptir (21-22 saat). Tekrarlanan doz alımlarından sonra hidroksi, karboksi ve desmetil defabrenibin ortalama metabolit/ ana ürün EAA oranları sırasıyla 0,9; 11 ve 0,7'dir. Maruziyet, rölatif güç ve farmakokinetik özelliklere göre hidroksi- ve desmetil-dabrafenibin her ikisi de TAFİNLAR'ın klinik aktivitesine katkıda bulunmakta iken karboksi-dabrafenibin aktivitesi anlamlı değildir.
İlaç-ilaç etkileşim potansiyelinin in vitro değerlendirmesi:
TAFİNLAR in vitro ortamda insan P-glikoproteini (Pgp) ve insan BCRP substratıdır. Ancak bu taşıyıcıların TAFİNLAR'ın oral biyoyararlanımı ve atılımı üzerindeki etkileri minimaldir ve Pgp ya da BCRP inhibitörleri ile klinik olarak anlamlı ilaç etkileşimi gösterme riski düşüktür. TAFİNLAR ya da 3 ana metabolitinin Pgp inhibitörü oldukları in vitro koşullarda gösterilmemiştir.
TAFİNLAR ve metabolitleri hidroksi-dabrafenib, karboksi-dabrafenib ve desmetil-dabrafenib in vitro ortamda insan organik anyon taşıyıcısı (OAT) 1 ve OAT3'ün inhibitörleri ve de, TAFİNLAR ve desmetil metabolit in vitro ortamda organik katyon taşıyıcıları 2'nin (OCT2) inhibitörü olsa dahi, bu taşıyıcılarda ilaç-ilaç etkileşimi riski TAFİNLAR ve metabolitlerinin klinik maruziyeti baz alındığında minimaldir.
Eliminasyon:
Tek intravenöz mikro-dozdan sonra TAFİNLAR'ın terminal yarılanma ömrü 2,6 saattir. TAFİNLAR terminal yarılanma ömrü, tek oral dozdan sonra, oral uygulama sonrasındaki emilim-kısıtlı eliminasyon nedeniyle 8 saattir (iki durumlu farmakokinetik). IV plazma klirensi 12 l/saattir.
Oral dozdan sonra TAFİNLAR‘ın başlıca eliminasyon yolu CYP3A4 ve CYP2C8 aracılı metabolizmadır. TAFİNLAR ile ilgili bileşikler temelde feçes ile atılır; oral dozun %71'i feçeste ve %23'i idrarda sadece metabolitler olarak tespit edilir.
Hastalardaki karakteristik özellikler
Karaciğer yetmezliği:
Bir popülasyon farmakokinetik analizi, hafif düzeyde yüksek bilirubin ve/veya AST düzeylerinin (Ulusal Kanser Enstitüsü [NCI] sınıflandırmasına göre) TAFİNLAR oral klirensini anlamlı ölçüde etkilemediğini göstermektedir. Ayrıca, bilirubin ve AST ile tanımlanan hafif karaciğer bozukluğunun, TAFİNLAR'ın metabolit plazma konsantrasyonları üzerinde anlamlı etkisi olmamıştır. Orta şiddette veya şiddetli karaciğer yetmezliği olan hastalar ile ilgili herhangi bir veri mevcut değildir. Hepatik metabolizma ve safra yoluyla atılım, TAFİNLAR'ın ve metabolitlerinin primer eliminasyon yolları olduğundan, TAFİNLAR, orta ila şiddetli düzeyde karaciğer yetmezliği bulunan hastalarda dikkatli şekilde uygulanmalıdır (bkz. Bölüm 4.2).
Böbrek yetmezliği:
Bir popülasyon farmakokinetik analizi, hafif böbrek bozukluğunun TAFİNLAR'ın oral klirensini etkilemediğini göstermektedir. Orta dereceli böbrek bozukluğu olan hastalarda klinik veriler sınırlı olmakla birlikte bu veriler klinik açıdan anlamlı bir etkiye işaret etmemektedir. Şiddetli böbrek bozukluğu olan hastalarda klinik veri yoktur (bkz. Bölüm 4.2).
Geriyatrik popülasyon:
Popülasyon farmakokinetik analizine göre, yaşın TAFİNLAR farmakokinetiği üzerinde önemli bir etkisi yoktur. Karboksi- ve desmetil-dabrafenib plazma konsantrasyonları için yaşın 75'ten büyük olması önemli bir belirteç olmuştur; ≥75 yaş hastalarda < 75 yaş hastalara kıyasla %40 daha fazla maruziyet saptanmıştır.
Vücut ağırlığı ve cinsiyet:
Popülasyon farmakokinetik analizine göre, cinsiyet ve ağırlık TAFİNLAR'ın oral klerensini etkilemiştir, ayrıca ağırlık oral hacmin dağılımı ve dağılma klerensini de etkilemiştir. Bu farmakokinetik farklılıklar klinik olarak anlamlı kabul edilmemiştir.
Irk:
Popülasyon farmakokinetiği analizi Asyalı ve Beyaz hastalar arasında TAFİNLAR farmakokinetiği bakımından anlamlı farklılıklar göstermemiştir. Diğer ırkların TAFİNLAR farmakokinetiği üzerindeki potansiyel etkisinin değerlendirebilmek için yetersiz veri mevcuttur.
Pediyatrik popülasyon:
Pediyatrik hastalarda TAFİNLAR farmakokinetiğini araştıran çalışmalar yapılmamıştır.
5.3. Klinik öncesi güvenlilik verileri
TAFİNLAR ile karsinojenite çalışmaları yapılmamıştır. TAFİNLAR, bakteri ve kültüre edilmiş memeli hücrelerindeki in vitro testlerde ve in vivo kemirgen mikronükleus değerlendirme testinde mutajenik veya klastojenik değildir.
Birleşik dişi fertilitesinde, sıçanlarda erken embriyonik ve embriyofetal gelişim çalışmalarında overiyen korpora lutea sayıları hamile dişilerde 300 mg/kg/gün seviyesine düşmüştür (EAA bazında insan klinik maruziyetinin yaklaşık 3 katı), fakat östrojen döngüsü, çiftleşme veya fertilitede etkileri yoktur. 300 mg/kg/gün dozunda embriyo-letalite ve ventriküler septal kusurlar ve timüs şeklinde varyasyon ve ≥20 mg/kg/gün dozlarında (EAA bazında insan klinik maruziyetinin ≥ 0,5 katı) iskelet gelişiminde gecikme ve fetüs ağırlığında azalma dahil gelişimsel toksisite görülmüştür.
TAFİNLAR ile erkek fertilite çalışmaları yapılmamıştır. Fakat tekrarlanan doz çalışmalarında sıçanlarda ve köpeklerde (EAA bazında insan klinik maruziyetinin ≥ 0,2 katı) testiküler dejenerasyon/deplesyon görülmüştür. Sıçan ve köpeklerdeki testiküler değişiklikler 4 haftalık iyileşme döneminden sonra da devam etmiştir (bkz. Bölüm 4.6).
Köpeklerde (EAA bazında klinik maruziyetin ≥ 2 katı) koroner arter dejenerasyon/nekroz ve/veya hemoraji, kardiyak atriyoventriküler kapak hipertrofisi/hemoraji ve atriyal fibrovasküler proliferasyon dahil olmak üzere kardiyovasküler etkiler görülmüştür. Farelerde çeşitli dokularda fokal arteriyel/perivasküler enflamasyon gözlenmiş olup, sıçanlarda enflamasyon eşliğinde spontan kardiyomiyosit dejenerasyonu (spontan kardiyomiyopati) ve hepatik arteriyel dejerasyon insidansında bir artış gözlenmiştir (sıçanlar ve fareler için klinik maruziyetin sırasıyla ≥0,5 ve 0,6 katı). Farelerde hepatoselüler nekroz ve enflamasyonu da içeren hepatik etkiler gözlenmiştir (klinik maruziyetin ≥0,6 katı).
Akciğerlerin bronkoalveolar inflamasyonu birçok köpekte ≥ 20 mg/kg/gün (EAA değerine göre insan klinik maruziyetinin ≥ 9 katı) dozunda görülmüştür ve yüzeysel ve/veya zorlu solunum ile birliktedir.
TAFİNLAR verilen köpek ve sıçanlarda geri dönüşümlü hematolojik etkiler gözlemlenmiştir. Köpek ve sıçanlarda, 13 haftaya kadar olan çalışmalarda retikülosit sayısı ve/veya kırmızı hücre kütlesi gözlenmiştir (sırasıyla klinik maruziyetin ≥ 10 ve 1,4 katı).
Farelerde jüvenil toksisite çalışmaları, büyüme üzerinde etki (uzun kemik boyunun daha kısa olması), renal toksisite (tübüler çökeltiler, artmış kortikal kist ve tübüler bazofili sıklığı, üre ve/veya kreatinin konsantrasyonlarında geri dönüşümlü artışlar) ve testiküler toksisite
(dejenerasyon ve tübüler genişleme) gözlenmiştir (EAA bazında yetişkin insan klinik maruziyetinin ≥0,2 katı).
TAFİNLAR, bir fare fibroblast 3T3 Nötr Kırmızı Tutulumu (NRU) tayininde in vitro şartlarda ve tüysüz farelerdeki bir oral fototoksisite çalışmasında ≥ 100 mg/kg dozlarda (Cbazında klinik maruziyetin >44 katı) in vivo koşullarda fototoksik etki göstermiştir.
Trametinib ile kombinasyon
Köpeklerle yürütülen trametinib ve TAFİNLAR'ın 4 hafta süreyle kombinasyon halinde verildiği bir çalışmada, tek başına trametinib verilen köpeklere kıyasla gastrointestinal toksisite ve azalan timus lenfoit selülaritesinde daha düşük maruziyetlerde gözlenmiştir. Bunun dışında, benzer monoterapi çalışmalarındakiler ile benzer toksisiteler gözlenmiştir.
 Grip, Soğuk Algınlığı ve Öksürük
Grip ve soğuk algınlığı (nezle) semptomları arasındaki farkı bilmek önemlidir. Soğuk algınlığı gripten daha hafif belirtiler gösteren bir solunum yolu hastalığıdır.
Grip, Soğuk Algınlığı ve Öksürük
Grip ve soğuk algınlığı (nezle) semptomları arasındaki farkı bilmek önemlidir. Soğuk algınlığı gripten daha hafif belirtiler gösteren bir solunum yolu hastalığıdır. |
 İnme
İnme, beynin hasar görmesinin sonucudur. Bu hasar, beynin bir kısmındaki ya bir kanama
ya da akut kan eksikliği nedeniyle o kısmın geçici ya da kalıcı olarak işlevini yapamamasına
yol açar.
İnme
İnme, beynin hasar görmesinin sonucudur. Bu hasar, beynin bir kısmındaki ya bir kanama
ya da akut kan eksikliği nedeniyle o kısmın geçici ya da kalıcı olarak işlevini yapamamasına
yol açar. |
İLAÇ GENEL BİLGİLERİ
Novartis Sağlık,Gıda ve Tarım Ürünleri San. Tic. A.Ş.
| Geri Ödeme Kodu | A14982 |
| Satış Fiyatı | 63425.88 TL [ 10 May 2024 ] |
| Önceki Satış Fiyatı | 63425.88 TL [ 3 May 2024 ] |
| Original / Jenerik | Original İlaç |
| Reçete Durumu | Normal Reçeteli bir ilaçdır. |
| Barkodu | 8699504151015 |
| Etkin Madde | Dabrafenib |
| ATC Kodu | L01EC02 |
| Birim Miktar | 50 |
| Birim Cinsi | MG |
| Ambalaj Miktarı | 120 |
| Antineoplastik ve İmmünomodülatör Ajanlar |
| İthal ve Beşeri bir ilaçdır. |
İLAÇ EŞDEĞERLERİ
| Eşdeğer İlaç Adı | Barkodu | İlaç Fiyatı |
|---|---|---|
| Eşdeğer bir ilaç bulunamadı |
 |
Gıda Alerjisi Her yıl milyonlarca insan yiyeceklere alerji gösteriyor. |
 |
Artrit Artrit, oldukça yaygın bir hastalıktır ancak iyi anlaşılamamıştır. Aslında “artrit” tek bir hastalığın adı değildir; eklem ağrısı veya eklem hastalıklarını adlandırmanın gayri resmi yoludur. |
 |
Lösemi Kan Kanseri Lösemi, kan kanseridir ve vücudunun kan oluşturan dokularının hastalanması anlamına gelir. Birçok lösemi türü vardır; bazı lösemi türleri çocuklarda bazıları da yetişkinlerde sık görülür. |