NEXPLANON 68 mg implant Klinik �zellikler
{ Etonogestrel }
4. KL�N�K �ZELL�KLER
4.1. Terap�tik endikasyonlar
Kontrasepsiyon
G�venlili�i ve etkilili�i 18-40 ya� aras� kad�nlarda belirlenmi�tir.
4.2. Pozoloji ve uygulama �ekli
Pozoloji/uygulama s�kl��� ve s�resiNEXPLANON yerle�tirilmeden �nce gebelik olas�l��� d��lanmal�d�r.
Uygulama yerinde 3 y�l kalabilen 1 implant.
NEXPLANON'un sadece aplikat�r kullan�m� ve implant�n yerle�tirme-��karma e�itimini tamamlam�� olan doktorlar taraf�ndan yerle�tirilmesi ve ��kar�lmas� �nemle tavsiye edilir. Uygun oldu�u durumlarda, implant�n yerle�tirme ve ��karma teknikleri i�in e�itim alan doktorlar�n g�zetmenli�i talep edilebilir.
�mplant yerle�tirilmeden �nce, ‘NEXPLANON nas�l yerle�tirilir' ve ‘NEXPLANON nas�l ��kar�l�r' b�l�mlerindeki (bkz. B�l�m 4.2) yerle�tirme ve ��karma talimatlar�n� dikkatlice okuyunuz ve uygulay�n�z.
E�er NEXPLANON'un g�venli bir �ekilde yerle�tirilmesi ve/veya ��kar�lmas� i�in gerekli ad�mlardan emin de�ilseniz, l�tfen prosed�r� denemeyiniz.
NEXPLANON nas�l kullan�l�r:
NEXPLANON uzun etkili bir hormonal kontraseptiftir. Deri alt�na tek bir implant yerle�tirilir
ve �� y�l boyunca orada b�rak�labilir. Yerle�tirildi�i tarihten sonra, en fazla �� y�l i�inde
implant� ��kar�n�z. Kullan�c�, herhangi bir zamanda NEXPLANON ��karmak isteyebilece�i ve implant�n �� y�ldan daha uzun s�re kullan�lamayaca�� konusunda bilgilendirilmelidir. Sa�l�k �al��anlar� kilolu kad�nlarda implant� daha erken de�i�tirmeyi d���nebilir (bkz. B�l�m 4.4). �mplant ��kar�ld�ktan hemen sonra yeni bir implant�n yerle�tirilmesi kontrasepsiyonu s�rd�recektir. E�er kad�n NEXPLANON kullan�m�na devam etmek istemez fakat gebelikten korunmaya devam etmek isterse, ba�ka bir kontraseptif y�ntem �nerilmelidir.
NEXPLANON implant�n�n ba�ar�l� bir �ekilde kullan�labilmesi ve daha sonra da ��kar�labilmesi i�in, implant deri alt�na, talimatlara uygun �ekilde, dikkatlice ve do�ru olarak yerle�tirilmelidir.
E�er implant talimatlara uygun �ekilde ve do�ru zamanda yerle�tirilmezse, bu durum istenmeyen gebelikle sonu�lanabilir (bkz. B�l�m 4.2 NEXPLANON nas�l yerle�tirilir ve NEXPLANON ne zaman yerle�tirilir).
Deri alt�ndan daha derine yerle�tirilen (derin yerle�tirme) implant, elle hissedilemeyebilir ve yerinin tespit edilmesi ve/veya ��kar�lmas� zor olabilir (bkz. B�l�m 4.2 NEXPLANON nas�l ��kar�l�r ve bkz. B�l�m 4.4)
NEXPLANON implant�, genellikle kullan�lmayan kolun �st b�l�m�n�n i� taraf�na subdermal olarak DER�N�N HEMEN ALTINA yerle�tirilmelidir. Yerle�tirme yeri humerus medial epikondilinin yakla��k 8-10 cm (3-4 in�) yukar�s�nda triseps kas�n�n �zerine gelecek �ekilde ve biseps ve triseps kaslar�n�n aras�ndaki olu�un (sulkus) 3-5 cm (1,25-2 in�) posteriorundad�r (a�a��da). Bu b�lge, sulkus i�inde ve �evresinde yer alan b�y�k kan damarlar� ve sinirlerden ka��nmay� ama�lamaktad�r (bkz. �ekil 2a, 2b ve 2c) .
Yerle�tirilme tamamland�ktan hemen sonra, implant�n varl��� palpasyonla do�rulanmal�d�r. �mplant�n palpe edilemedi�i durumlarda ya da implant�n varl���ndan ku�ku duyuldu�u zaman, (bkz. b�l�m 4.2 NEXPLANON nas�l yerle�tirilir ba�l��� alt�nda yer alan “E�er implant yerle�tirmeden sonra palpasyonla hissedilmezse”).
NEXPLANON'un ambalaj�nda kad�n�n, implant�n seri numaras�n� yazaca�� bir Kullan�c� Kart� vard�r. Sa�l�k �al��anlar�ndan da Kullan�c� Kart�'na implant�n yerle�tirilme tarihini, hangi kola yerle�tirildi�ini ve ��kar�lmas� ama�lanan tarihi kaydetmeleri istenmektedir. Ambalajda ayr�ca sa�l�k �al��anlar�n�n seri numaras�n� kaydetmeleri i�in yap��kanl� etiketler de vard�r.
NEXPLANON ne zaman yerle�tirilir:
�NEML�: �mplant yerle�tirilmeden �nce gebelik olas�l���n� d��lay�n�z.
Yerle�tirilme i�leminin ne zaman yap�laca��, a�a��da belirtildi�i �zere kad�n�n yak�n zamandaki kontrasepsiyon hikayesine ba�l�d�r:
�ncesinde hormonal kontrasepsiyon kullan�lmam��sa
�mplant, kad�n�n kanamas� devam ediyor olsa bile menstr�al siklusun 1. g�n� (menstr�asyon kanamas�n�n ilk g�n�) ve 5. g�n� aras�nda yerle�tirilmelidir.
E�er yerle�tirme �nerildi�i �ekilde yap�l�rsa, ilave kontrasepsiyon gerekli de�ildir. E�er yerle�tirme i�in �nerilen zamandan sap�l�rsa, kad�na yerle�tirme sonras� 7 g�ne kadar bir bariyer y�ntem kullan�lmas� tavsiye edilmelidir. E�er halihaz�rda ili�kiye girilmi�se, gebelik olas�l��� d��lanmal�d�r.
Hormonal kontraseptif y�ntemden NEXPLANON'a ge�i�
Kombine hormonal kontraseptif y�nteminden ge�i� yap�l�rsa (kombine oral kontraseptif
(kombine OK), vajinal halka ya da transdermal flaster)
�mplant tercihen, �nceki kombine OK tedavisinin son etkin tablet (etkin madde i�eren son tablet) kullan�m g�n�nden sonraki g�n, fakat en ge� olarak tabletsiz d�nem veya �nceki kombine oral kontraseptifin en son plasebo tabletini takiben yerle�tirilmelidir. Vajinal halka ya da transdermal flaster kullan�ld��� durumlarda, tercihen flasterin ��kar�ld��� g�n i�inde olmak �zere, en ge� sonraki uygulama g�n�ne kadar istenilen zamanda implant yerle�tirilmelidir.
E�er yerle�tirme �nerildi�i �ekilde yap�l�rsa, ilave kontrasepsiyon gerekli de�ildir. E�er yerle�tirme i�in �nerilen zamandan sap�l�rsa, kad�na yerle�tirme sonras� 7 g�ne kadar bir bariyer y�ntem kullan�lmas� tavsiye edilmelidir. E�er halihaz�rda ili�kiye girilmi�se, gebelik olas�l��� d��lanmal�d�r.
Yaln�zca-progestagen y�nteminden ge�i� yap�l�rsa (�rn: yaln�zca-progestagen i�eren do�um kontrol hap�, enjekte edilebilen kontraseptif, implant ya da rahim i�i sistem (R�S)
Yaln�zca-progestagen y�ntemlerinin bir�ok �e�idi oldu�undan, implant a�a��daki �ekilde yerle�tirilmelidir.
Enjekte edilebilen kontraseptifler: Planlanm�� bulunan bir sonraki enjeksiyon g�n�nde,
enjeksiyon yerine implant yerle�tirilmelidir.
Yaln�zca-progestagen i�eren do�um kontrol hap�: Kad�n ay�n herhangi bir g�n�nde yaln�zca- progestagen i�eren do�um kontrol hap�ndan NEXPLANON kullan�m�na ge�i� yapabilir. �mplant, son tablet al�m�ndan sonraki 24 saat i�inde yerle�tirilmelidir.
�mplant/ Rahim i�i sistem (R�S): �nceki implant�n veya R�S'in ��kar�ld��� ayn� g�n implant yerle�tirilebilir.
E�er yerle�tirme �nerildi�i �ekilde yap�l�rsa, ilave kontrasepsiyon gerekli de�ildir. E�er yerle�tirme i�in �nerilen zamandan sap�l�rsa, kad�na yerle�tirme sonras� 7 g�ne kadar bir bariyer y�ntem kullan�lmas� tavsiye edilmelidir. E�er halihaz�rda ili�kiye girilmi�se, gebelik olas�l��� d��lanmal�d�r.
D���k veya k�rtaj sonras�nda
�lk trimester: �lk trimesterdeki d���k ve k�rtaj sonras� 5 g�n i�inde implant yerle�tirilmelidir.
�kinci trimester: �kinci trimesterdeki d���k ve k�rtaj sonras� implant 21 ila 28. g�nler aras�nda yerle�tirilmelidir.
E�er yerle�tirme �nerildi�i �ekilde yap�l�rsa, ilave kontrasepsiyon gerekli de�ildir. E�er yerle�tirme i�in �nerilen zamandan sap�l�rsa, kad�na yerle�tirme sonras� 7 g�ne kadar bir bariyer y�ntem kullan�lmas� tavsiye edilmelidir. E�er halihaz�rda ili�kiye girilmi�se, gebelik olas�l��� d��lanmal�d�r.
Do�um sonras�nda
Emzirme durumunda: �mplant do�um sonras� d�rd�nc� haftadan sonra yerle�tirilmelidir (bkz. B�l�m 4.6). Kad�nlara yerle�tirme sonras� 7 g�ne kadar bir bariyer y�ntem kullan�lmas� �nerilmelidir. E�er halihaz�rda ili�kiye girilmi�se, gebelik olas�l��� d��lanmal�d�r.
Emzirmeme durumunda: �mplant do�um sonras� 21 ila 28. g�nler aras�nda yerle�tirilmelidir. E�er yerle�tirme �nerildi�i �ekilde yap�l�rsa, ilave kontrasepsiyon gerekli de�ildir. E�er implant do�um sonras� 28 g�nden sonra yerle�tirilirse, kad�na yerle�tirme sonras� 7 g�ne
kadar bir bariyer y�ntem kullan�lmas� tavsiye edilmelidir. E�er halihaz�rda ili�kiye girilmi�se, gebelik olas�l��� d��lanmal�d�r.
Uygulama �ekli
NEXPLANON nas�l yerle�tirilir:
NEXPLANON implant�n�n ba�ar�l� bir �ekilde kullan�labilmesi ve daha sonra da ��kar�labilmesi i�in, talimatlara g�re dikkatlice ve do�ru olarak subdermal yerle�tirilmesi gerekir. Yerle�tirilme sonras� gerek sa�l�k �al��anlar� gerekse kad�n implant� palpasyonla, yerle�tirildi�i yerde hissedebilmelidir.
�mplant genellikle kullan�lmayan kolun �st b�l�m�n�n i� taraf�na derinin hemen alt�na subdermal olarak yerle�tirilmelidir.
Deri alt�ndan daha derine yerle�tirilen (derin yerle�tirme) implant, elle hissedilemeyebilir ve yerinin tespit edilmesi ve/veya ��kar�lmas� zor olabilir (bkz. b�l�m 4.2 ve b�l�m 4.4) �mplant �ok derine yerle�tirilirse, sinirler veya damarlar zarar g�rebilir. �mplant derine veya hatal� olarak yerle�tirilirse, parestezi (sinir hasar�na ba�l�) veya yerle�tirildi�i yerden uzakla�ma (kas i�erisine veya fasyaya yerle�tirilmesine ba�l�) ve seyrek olarak damar i�erisine yerle�tirilme g�r�lebilir. NEXPLANON'un yerle�tirilmesi, aseptik ko�ullar alt�nda ve yaln�zca, prosed�r� bilen bir doktor taraf�ndan ger�ekle�tirilmelidir. �mplant�n yerle�tirilmesi yaln�zca, implant�n �nceden y�klenmi� oldu�u aplikat�r ile ger�ekle�melidir.
Yerle�tirme Prosed�r�
�mplant�n derinin hemen alt�na yerle�tirildi�inden emin olmak i�in, sa�l�k �al��an� aplikat�r� kolun �zerinden de�il, yandan g�zlemleyerek i�nenin ilerlemesini g�recek �ekilde konumlanmal�d�r. Yandan bak�ld���nda, yerle�tirilme yeri ve i�nenin derinin hemen alt�ndaki hareketi a��k �ekilde g�r�lebilmelidir.
A��klama amac�yla, �ekiller sol i� kolu g�stermektedir.
Kad�n�n, genellikle kullanmad��� kolu dirsekten b�k�lm�� ve d��a do�ru d�nm�� durumda muayene masas�na yat�r�lmal� ve eli ba��n�n alt�nda (veya m�mk�n oldu�unca yak�n) durmal�d�r (�ekil 1).

�ekil 1
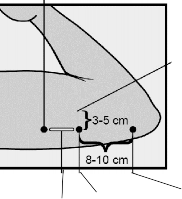
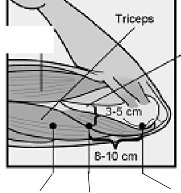
Yerle�tirme yeri, genellikle kullan�lmayan kolun �st b�l�m�n�n i� taraf� olarak belirlenir. Yerle�tirme yeri, humerus medial epikondilinden yakla��k 8-10 cm (3-4 in�) yukar�s�nda ve biseps ve triseps kaslar�n�n aras�ndaki olu�un (sulkus) 3-5 cm (1,25-2 in�) posteriorunda (a�a��da) olmal�d�r (bkz. �ekil 2a, 2b ve 2c). Bu b�lge, sulkusun i�inde ve �evresinde bulunan b�y�k kan damarlar� ve sinirlerden ka��nmay� ama�lamaktad�r. �mplant�n bu b�lgeye yerle�tirilmesi m�mk�n de�ilse (�rne�in ince kollu kad�nlar), sulkustan m�mk�n oldu�unca uza�a yerle�tirilmelidir.
Cerrahi bir i�aret kalemiyle birincisi implant�n yerle�tirilece�i yere, ikincisi bunun 5 santimetre (2 in�) proksimaline (omuza do�ru) olmak �zere iki i�aret koyulmal�d�r (�ekil 2a ve 2b). �kinci i�aret (k�lavuz i�aret) daha sonra, yerle�tirilme i�lemi s�ras�nda y�n g�steren bir k�lavuz olarak kullan�lacakt�r.
K�lavuz i�aret
Sulkus Sulkus
P D P D
Yerle�tirmeden sonra implant�n yeri
Yerle�tirme
yeri
Medial
epikondil
K�lavuz i�aret
Yerle�tirme
yeri
Medial
epikondil
�ekil 2a �ekil 2b
P: proksimal (omuza do�ru) D: distal (dirse�e do�ru)
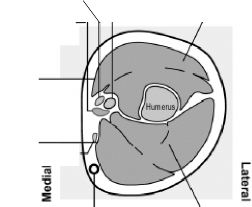
Median siniri
Basilik damar�
Kol
atardamar�
Biseps kas�
Sulkus
alan�
Yerle�tirmeden sonra implant
�ekil 2c
Triseps kas�
Dirsekten bak�ld��� �ekliyle, sol �st kolun kesiti Medial (kolun i� taraf�)
Lateral (kolun d�� taraf�)
Kol i�aretlendikten sonra, yerle�tirme yerinin kolun i� k�sm�nda do�ru b�lgede oldu�u teyit edilir.
Deri, yerle�tirme yerinden k�lavuz i�aretine kadar antiseptik bir sol�syon ile temizlenmelidir.
Yerle�tirme yerine anestezi uygulanmal�d�r. (�rne�in; hemen deri alt�na, planlanan yerle�tirme kanal� boyunca % 1'lik 2 mL lidokain enjekte edilerek veya anestezik spreyle).
Steril tek kullan�ml�k NEXPLANON aplikat�r i�eren implant blisterinden ��kar�lmal�d�r. E�er sterilitesinden ��phe edilirse, aplikat�r kullan�lmamal�d�r.

Mor renkli s�rg� (Hen�z dokunmay�n�z)
Aplikat�r�, i�nenin hemen yukar�s�nda olan, y�zey b�lgesinden tutunuz. Ok y�n�nde g�sterildi�i �zere horizontal olarak kayd�rarak i�nenin �zerindeki koruyucu saydam kapa�� ��kar�n�z (�ekil 3). E�er kapak aplikat�rden kolayca ayr�lm�yorsa, aplikat�r kullan�lmamal�d�r. ��nenin ucundan i�eriye bak�ld���nda, beyaz renkli implant� g�rmelisiniz. ��ne geri �ekilip implant�n aplikat�rden zaman�ndan �nce serbest kalmas�n� sa�layaca��ndan, i�neyi deri alt�na t�m�yle sokuncaya kadar mor renkli s�rg�ye dokunmay�n�z.
�ekil 3
Mor renkli s�rg� zaman�ndan �nce serbest b�rak�l�rsa, yeni bir aplikat�r ile prosed�r yeniden ba�lat�l�r.
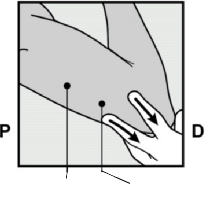
K�lavuz i�aret
Yerle�tirme yeri
Yerle�tirme yeri �evresindeki deri, bo�ta olan elle dirse�e do�ru gerilir (�ekil 4).
�ekil 4
�mplant subdermal olarak derinin hemen alt�na yerle�tirilmelidir (bkz B�l�m 4.4). �mplant�n derinin hemen alt�na yerle�tirildi�inden emin olmak i�in, kendinizi
aplikat�r� kolun �zerinden de�il, yandan g�zlemleyerek i�nenin ilerlemesini g�recek �ekilde konumland�rmal�s�n�z. Yandan bak�ld���nda, yerle�tirme yerini ve i�nenin derinin hemen alt�ndaki hareketini a��k �ekilde g�rebilirsiniz (bkz �ekil 6).
��ne, ucu deriyle 30°'den biraz az a�� yapacak �ekilde deriye bat�r�l�r. (�ekil 5a).
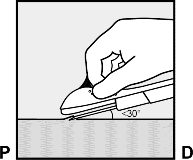
�ekil 5a
��neyi, konik u� (ucun e�imli a�z�) derinin hemen alt�nda olacak �ekilde (daha fazla de�il) yerle�tiriniz (�ekil 5b). E�er i�neyi, konik u�tan daha derine sokarsan�z, sadece konik u� deri alt�nda kalana kadar i�neyi geri �ekiniz.
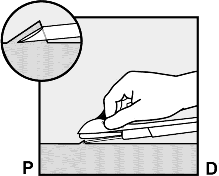
�ekil 5b
Aplikat�r a�a��ya do�ru indirilip neredeyse yatay konuma getirilir. Deri alt�na yerle�tirmeyi kolayla�t�rmak i�in, i�ne t�m uzunlu�u boyunca ileriye do�ru kayd�r�l�rken, deri i�ne ile kald�r�l�r (�ekil 6). Hafif bir diren� hissedilebilir ama a��r� g�� kullan�lmamal�d�r. ��ne deri alt�na tamamen girmezse, implant gereken �ekilde yerle�tirilemeyecektir.
��nenin yerle�imi tamamlanmadan �nce i�ne ucu deriden ��karsa, i�ne geri �ekilmeli ve yerle�tirme i�lemini tamamlamak i�in deri alt� pozisyonuna yeniden ayarlanmal�d�r.
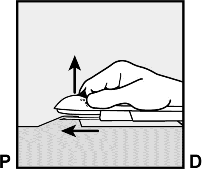
�ekil 6
Tam olarak yerle�en i�ne ile aplikat�r� ayn� pozisyonda tutunuz (�ekil 7). E�er gerekirse, aplikat�r� sabit tutmak i�in serbest olan elinizi kullanabilirsiniz.
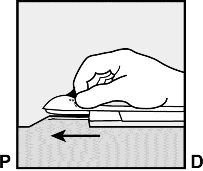
�ekil 7
Mor renkli s�rg�n�n kilidini, hafif�e a�a��ya do�ru bast�rarak a��n�z (�ekil 8a). Duruncaya kadar s�rg�n�n tamam�n� arkaya do�ru �ekiniz.
Mor renkli s�rg�y� hareket ettirirken, aplikat�r� hareket ettirmeyiniz ( ) (�ekil 8b). �mplant �imdi deri alt�ndaki en son pozisyonundad�r ve i�ne aplikat�r�n g�vdesi i�erisinde kilitlidir. Aplikat�r �imdi ��kar�labilir (�ekil 8c).
) (�ekil 8b). �mplant �imdi deri alt�ndaki en son pozisyonundad�r ve i�ne aplikat�r�n g�vdesi i�erisinde kilitlidir. Aplikat�r �imdi ��kar�labilir (�ekil 8c).
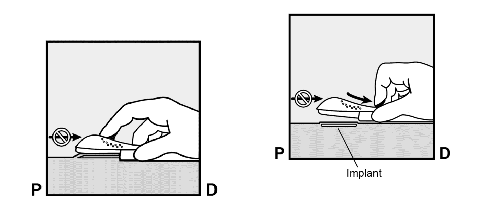
�ekil 8a �ekil 8b
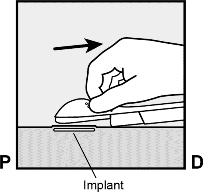
�ekil 8c
E�er aplikat�r bu i�lem boyunca ayn� pozisyonda kalmazsa veya mor renkli s�rg� arkaya do�ru tamamen �ekilmezse, implant gereken �ekilde yerle�meyecek ve yerle�im yerinden ��kacakt�r.
E�er implant, yerle�im yerinden ��k�yorsa, implant� ��kar�n�z ve yeni bir aplikat�r kullanarak ayn� yerle�im yerinde yeni bir i�lem ger�ekle�tiriniz. Yerle�im yerinden ��kan implant� kesite do�ru geri itmeyiniz.
4.3. Kontrendikasyonlar
Yaln�zca progestagen i�eren kontraseptifler a�a��daki ko�ullar�n herhangi birinin varl���nda kullan�lmamal�d�r. NEXPLANON kullan�m� s�ras�nda bu durumlardan herhangi biri ortaya ��karsa, �r�n�n kullan�m� hemen durdurulmal�d�r.
NEXPLANON i�indeki etkin maddeye ya da yard�mc� maddelerden herhangi birine kar�� a��r� duyarl�l�k.
Bilinen veya ��phelenilen gebelik.
Aktif ven�z tromboembolik bozukluk.
Bilinen veya ��phe edilen, cinsel steroidlere duyarl� k�t� huylu hastal�klar (maligniteler).
Karaci�er t�m�rlerinin varl��� veya �yk�s� (benign veya malign)
Uzun s�re karaci�er fonksiyon de�erlerinin normale d�nmedi�i ciddi karaci�er hastal��� ya
da �yk�s�.
Tan� konmam�� vajinal kanama.
4.4. �zel kullan�m uyar�lar� ve �nlemleri
A�a��daki durum / risklerden herhangi biri ortaya ��kt���nda, her kad�n i�in progestagen kullan�m�n�n yararlar� ile olas� riskleri de�erlendirilmeli ve NEXPLANON kullan�m�na ba�lamadan �nce kad�n ile konu�ulmal�d�r. Bu durumlardan herhangi birinin artmas�, �iddetlenmesi ya da ilk kez ortaya ��kmas� halinde kad�n, sa�l�k �al��an�na ba�vurmal�d�r. Daha sonra sa�l�k �al��an� NEXPLANON kullan�m�na devam edilip edilmeyece�ine karar vermelidir.
Meme karsinomu
Meme kanseri riski genel olarak ya� ile artmaktad�r. (Kombine) Oral kontraseptiflerin (OK) kullan�m� s�ras�nda meme kanseri tan�s� riski hafif d�zeyde artmaktad�r. Bu risk art��� OK kullan�m�n�n kesilmesinden sonraki 10 y�l i�inde yava��a ortadan kalkar ve kullan�m s�resi ile ili�kili de�ildir, fakat OK kullan�lan ya� ile ili�kilidir. Kombine OK kullanan 10.000 kad�nda tan� konulmas� beklenen olgu say�s� (kesildikten sonra 10 y�la dek), ayn� ya�larda hi� kullanmam�� ya� gruplar�na g�re hesaplanm��t�r: 4,5/4 (16-19 ya�), 17,5/16 (20-24 ya�), 48,7/44 (25-29 ya�), 110/100 (30-34 ya�), 180/160 (35-39 ya�) ve 260/230 (40-44 ya�).
Yaln�zca progestagen i�eren kontraseptif y�ntem kullan�c�lar�n�n riski, muhtemelen kombine OK kullananlar�n riski ile benzer b�y�kl�ktedir. Bununla birlikte, bu y�ntemler i�in elde edilen kan�tlar ile sa�l�kl� bir sonuca var�lmam��t�r. T�m ya�am boyu meme kanseri riski ile kar��la�t�r�ld���nda, OK ile ili�kili olan risk art��� d���kt�r. OK kullan�c�lar� aras�nda meme kanseri tan�s� konulmu� olgular�n, OK kullanmam�� olgulara k�yasla daha az ilerlemi� olgular olmas� e�ilimi s�z konusudur. OK kullan�c�lar�nda g�zlenen risk art���n�n daha erken tan� ve OK biyolojik etkilerinden ya da her ikisinden kaynaklanmas� olas�d�r.
Karaci�er bozuklu�u
Akut veya kronik karaci�er fonksiyonu bozukluklar� meydana geldi�inde, kad�n muayene olmak ve dan��mak i�in doktoruna ba�vurmal�d�r.
Trombotik ve di�er vask�ler olaylar
Epidemiyolojik ara�t�rmalar kombine OK (�strojen + progestagen) kullan�m� ile ven�z tromboembolizm (VTE, derin ven trombozu ve pulmoner emboli) ve arteriyel tromboembolizm (ATE, miyokard infarkt�s� ve iskemik inmeler) insidans� art���n� ili�kilendirmi�tir. �strojenik bile�en yoklu�unda sadece progestagen i�eren kontraseptif olarak kullan�lan etonogestrel (desogestrel'in biyolojik olarak aktif metaboliti) i�in bu bulgular�n klinik �nemi bilinmemektedir.
S�n�rl� epidemiyolojik veri, implant kullanan kad�nlarda artm�� VTE veya ATE riskini d���nd�rmemektedir, ancak etonogestrel implant� kullanan kad�nlarda pazarlamas� sonras� VTE ve ATE rapor edilmi�tir. VTE ve ATE riskini art�rd��� bilinen risk fakt�rlerinin de�erlendirilmesi �nerilir.
Tromboembolik bozukluk ge�mi�i olan kad�nlar�n n�ksetme olas�l��� konusunda uyar�lmalar� gereklidir. Tromboz durumunda implant ��kar�lmal�d�r. Ameliyat veya hastal�k nedeniyle uzun s�reli hareketsizlik durumunda implant�n ��kar�lmas� d���n�lmelidir.
Kan bas�nc�nda art��
NEXPLANON kullan�m� s�ras�nda s�rekli hipertansiyon ortaya ��kt���nda ya da kan bas�nc�nda anlaml� bir art�� antihipertansif tedaviye yeterli yan�t vermedi�inde, NEXPLANON ��kar�lmal�d�r.
Karbonhidrat metabolik etkisi
Sadece progestagen i�eren kontraseptiflerin kullan�m�n�n periferik ins�lin direnci ve glukoz tolerans� �zerinde etkisi olabilir. Bu nedenle, diyabet hastas� kad�nlar NEXPLANON kullan�m�n�n ilk aylar�nda yak�ndan izlenmelidirler.
Kloazma
�zellikle kloazma gravidarum �yk�s� olan kad�nlarda, seyrek olarak kloazma ortaya ��kabilir. Kloazmaya yatk�nl��� olan kad�nlar, NEXPLANON kullan�rken g�ne� ya da UV ���nlar�na maruz kalmaktan ka��nmal�d�r.
V�cut a��rl���
NEXPLANON'un kontraseptif etkisi, etonogestrelin plazma d�zeyleri ile ili�kilidir. Plazma d�zeyleri v�cut a��rl��� ile ters orant�l�d�r ve yerle�tirildikten sonra zaman ge�tik�e azal�r. Kilolu kad�nlarda klinik deneyim 3 y�l kullan�m ile s�n�rl�d�r. Bu nedenle bu kad�nlarda ���nc� y�ldaki kontraseptif etkinin normal a��rl�ktaki kad�nlardakinden daha d���k olabilece�i d���n�lmelidir. Doktorlar kilolu kad�nlarda implant�n daha erken de�i�tirilmesini d���nebilirler.
�mplant�n yerle�tirilmesiyle ilgili komplikasyonlar
Derin ilk yerle�tirmeye (ayn� zamanda bkz. 4.2. ‘NEXPLANON nas�l yerle�tirilir') ve/veya d�� etkilere (�rn: implant�n manipule edilmesi ya da temas i�eren sporlar) ba�l� olarak implant�n yerle�tirme alan�ndan ba�ka bir yere hareket etti�ine dair raporlar vard�r. Ayr�ca, nadir olarak pazarlama sonras� raporlarda implant�n derine yerle�tirilmesine veya intravask�ler yerle�tirilmesine ba�l� olarak implant koldaki kan damarlar�nda veya pulmoner arterde bulunmu�tur. �mplant�n orijinal yerle�tirme alan�ndan hareket etmi� oldu�u bu durumlarda implant�n lokalizasyonu �ok zor olabilir ve ��karma i�lemi i�in daha geni� bir insizyon ve cerrahi operasyon gerekebilir (ayn� zamanda bkz. 4.2. ‘NEXPLANON nas�l ��kar�l�r'). E�er implant palpe edilemezse, medikal a��dan uygun olur olmaz yerinin tespit edimesi ve ��kar�lmas� �nerilmektedir. E�er implant ��kar�lmazsa, kontrasepsiyon ve progestagenle ilgili istenmeyen etkilerin riski, kad�n�n istedi�i zaman aral���ndan daha uzun s�reli etkili olabilirler.
�zellikle ‘NEXPLANON nas�l yerle�tirilir' (bkz. 4.2) b�l�m�ndeki talimatlara g�re yerle�tirilmedi�inde ya da lokal inflamasyon durumlar�nda, implant yerinden ��kabilir.
Over kistleri
T�m d���k doz hormonal kontraseptiflerle, folik�ler geli�im g�r�lebilir ve seyrek olarak folik�l normal d�ng�deki boyuta kadar b�y�meye devam edebilir. Genel olarak b�y�yen folik�ller kendili�inden ortadan kalkar. S�kl�kla asemptomatiktirler; baz� olgularda hafif kar�n a�r�s�na neden olabilirler. Nadiren cerrahi giri�im gerektirirler.
Ektopik gebelik
Yaln�z progestagen i�eren geleneksel kontraseptiflerin ektopik gebeli�i �nlemedeki etkileri, bu y�ntemlerin kullan�m� s�resince ov�lasyonlar�n s�kl��� ile ili�kili oldu�undan, kombine OK tedavisi kadar iyi de�ildir. NEXPLANON'nun ovulasyonu bask�lamas�na ra�men, amenore ya da kar�n a�r�s� olan kad�nlarda ay�r�c� tan�da ektopik gebelik de dikkate al�nmal�d�r.
Psikiyatrik bozukluklar
Depresif duygudurum ve depresyon, hormonal kontraseptif kullan�m�n�n iyi bilinen istenmeyen etkileridir (bkz. B�l�m 4.8). Depresyon ciddi olabilir ve intihar e�ilimi ve intihar i�in bilinen bir risk fakt�r�d�r. Kad�nlar�n, tedaviye ba�lad�ktan k�sa bir s�re sonra da dahil olmak �zere, duygudurum de�i�iklikleri ve depresif belirtiler durumunda doktorlar�yla ileti�ime ge�meleri tavsiye edilmelidir.
Di�er durumlar
A�a��daki durumlar gebelik ve cinsiyet steroidleri kullan�m�nda bildirilmi�tir, fakat progestagen kullan�m�yla ili�kisi saptanamam��t�r; kolestaz ile ili�kili sar�l�k ve/veya ka��nt�, safra kesesi ta�� olu�umu; porfiri; sistemik lupus eritematozus, hemolitik �remik sendrom; Sydenham koresi, gestasyonal herpes , otoskleroza ba�l� duyma kayb� ve (kal�t�msal) anjiyo�dem.
T�bbi muayene/dan��manl�k
NEXPLANON ilk olarak yerle�tirilmeden ya da de�i�tirilmeden �nce tam bir t�bbi �yk� al�nmal�d�r (t�bbi soyge�mi�) ve gebelik olmad���ndan emin olunmal�d�r. Kontrendikasyonlar (bkz. B�l�m 4.3.) ve uyar�lar (bkz. B�l�m 4.4.) k�lavuzlu�unda, kan bas�nc� �l��lmeli ve fiziki muayene yap�lmal�d�r. NEXPLANON yerle�tirilmesinden �� ay sonra da bir muayene yap�lmas� �nerilir. Bu muayenede, kan bas�nc� �l��lmeli, sorular ve yak�nmalar dinlenmeli ve istenmeyen etkiler sorulmal�d�r. Daha sonraki periyodik muayenelerin s�kl��� ve tarz�, klinik karar k�lavuzlu�unda ki�iye g�re ayarlanmal�d�r. �mplant her genel sa�l�k kontrol� muayenesinde elle kontrol edilmelidir. Kad�n, genel sa�l�k kontrolleri aras�ndaki herhangi bir zamanda implant�n� eliyle hissedemedi�i zaman hemen doktoruna haber vermesi konusunda bilgilendirilmelidir.
Kad�nlara NEXPLANON kullan�m�n�n HIV enfeksiyonu (AIDS) ya da di�er cinsel yolla bula�an hastal�klara kar�� korumad��� a��klanmal�d�r.
Etkilili�in azalmas�
NEXPLANON'un etkilili�i, e�zamanl� kullan�lan t�bbi �r�nlerle azalabilir (bkz. 4.5.).
Menstr�el kanama d�zeninde de�i�iklikler
NEXPLANON kullan�m� s�ras�nda, muhtemelen kad�nlar�n menstr�el kanama d�zeninde �nceden tahmin edilemeyen de�i�iklikler olabilir. Bu de�i�iklikler �unlar� i�erebilir; kanama s�kl�klar�nda de�i�iklikler (kanama olmamas�, daha az s�kl�kta olmas�, �ok s�k veya devaml� olmas�) ve kanama yo�unlu�unda (azalmas� veya artmas�) veya s�resinde de�i�iklikler. 5 kad�ndan 1'inde amonere bildirilirken, yine 5 kad�ndan 1'inde s�k ve/veya uzun s�reli kanama bildirilmi�tir. �lk �� aydaki kanama profili bir�ok kad�nda, daha sonraki kanama profillerinin yakla��k olarak tahmin edilmesini sa�lar. Bilgi, dan��manl�k ve kanama g�nl��� kullan�m� gibi destekler, kad�n�n kanama d�zenini kabul etmesini kolayla�t�rabilir. Vajinal kanama de�erlendirmesi, ki�iye �zel olarak yap�lmal�d�r ve jinekolojik patoloji ya da gebeli�i d��lamak i�in muayeneyi i�erebilir.
�n situ k�r�lan veya b�k�len implantlar
D�� etkiler nedeniyle hastan�n kolundayken k�r�lan veya b�k�len implantlar rapor edilmi�tir. K�r�lan implant par�as�n�n kolun i�inde hareket etmesi ayr�ca rapor edilmi�tir. �n vitro verilere g�re, implant k�r�ld���nda ya da b�k�ld���nde, etonogestrelin sal�m h�z� �ok az artabilir. Bu de�i�ikli�in klinik olarak anlaml� etkileri olmas� beklenmez.
Ancak, implant k�r�ld���nda ��kar�lmal�d�r ve tamamen ��kar�lm�� olmas� �nemlidir. Bkz. implant ��karma prosed�rleri i�in B�l�m 4.2 (palpasyonla hissedilebilen veya hissedilemeyen).
4.5. Di�er t�bbi �r�nler ile etkile�imler ve di�er etkile�im �ekilleri
Not: Olas� etkile�imleri belirlemek i�in birlikte kullan�lan ila�lar�n �r�n bilgilerine ba�vurulmal�d�r.
Di�er t�bbi �r�nlerin NEXPLANON �zerine etkisi
Mikrozomal enzimleri ind�kleyen ila�larla etkile�im seks hormonlar�n�n y�k�m�nda art��a ve
menstr�el kanama ve/veya kontrasepsiyonda ba�ar�s�zl��a neden olabilir.
�dame edilmesi
Enzim ind�ksiyonu tedaviden sonraki birka� g�n i�erisinde g�zlemlenebilir. Maksimum enzim ind�ksiyonu genel olarak birka� hafta i�erisinde g�zlemlenir. �la� tedavisini b�rakt�ktan sonra, enzim ind�ksiyonu yakla��k 4 hafta boyunca devam edebilir.
Hepatik enzim ind�kleyici ila� ya da bitkisel �r�nleri alan kad�nlar NEXPLANON'un etkilili�inin azalabilece�i konusunda uyar�lmal�d�r. �mplant�n ��kar�lmas� gerekmemektedir; ancak kad�nlar�n birlikte ila� kulland�klar� d�nemde ve tedavinin b�rak�lmas�n� takiben 28 g�n boyunca maksimum korumay� elde etmek i�in ek hormonal olmayan kontraseptif y�ntemi kullanmalar� �nerilmektedir.
Literat�rde a�a��daki etkile�imler bildirilmi�tir (esas olarak kombine kontraseptiflerle ancak bazen NEXPLANON dahil sadece progestajen i�eren kontraseptiflerle):
Hormonal kontraseptiflerin y�k�m�n� art�ran maddeler (enzim ind�ksiyonu ile hormonal kontraseptiflerin etkilili�i azal�r), �rne�in:
Barbit�ratlar, bosentan, karbamazepin, fenitoin, primidon, rifampin ve HIV/HCV tedavisinde kullan�lan ritonavir, efavirenz, boseprevir, nevirapin ve muhtemelen felbamat, griseofulvin, okskarbazepin, topiramat ve St. John's Wort (Hypericum perforatum) gibi bitkisel �r�nler.
Hormonal kontraseptiflerin y�k�m�nda �e�itli etkileri olan maddeler
Hormonal kontraseptiflerle birlikte kullan�ld���nda HIV proteaz inhibit�rlerinin ve n�kleozid olmayan ters transkriptaz inhibit�rlerinin bir�ok kombinasyonu ve HCV inhibit�rleri ile de kombinasyonlar�, etonogestrel dahil progestinlerin plazma konsantrasyonlar�n� art�rabilir ya da azaltabilir. Bu de�i�ikliklerin net etkileri baz� vakalarda klinik olarak anlaml� olabilir.
Bundan dolay�, potansiyel etkile�imleri belirlemek ve ilgili tavsiyeler y�n�nden birlikte kullan�lan HIV/HCV ila�lar�n�n �r�n bilgilerine bak�lmal�d�r. Herhangi bir ��phe durumunda, proteaz inhibit�r� ya da n�kleozid olmayan ters transkriptaz inhibit�r tedavisi alan kad�nlar
ek bir bariyer kontraseptif y�ntemi kullan�lmal�d�r.
Hormonal kontraseptiflerin y�k�m�n� azaltan maddeler (enzim inhibit�rleri)
CYP3A4 mikrozomal enzimlerini kuvvetli inhibe eden ila�lar (�rn; ketokonazol, itrakonazol, klaritromisin) veya orta derecede inhibe eden ila�lar (flukonazol, diltiazem, eritromisin), etonogestrel dahil, progestinlerin serum konsantrasyonlar�n� art�rabilir.
NEXPLANON'un di�er t�bbi �r�nler �zerine etkisi
Hormonal kontraseptifler di�er ila�lar�n metabolizmalar� ile etkile�ebilir. Dolay�s�yla, plazma ve doku konsantrasyonlar�n� art�rabilir (�rn; siklosporin) veya azaltabilir (�rn; lamotrijin).
�zel pop�lasyonlara ili�kin ek bilgiler:
�zel pop�lasyonlar ile yap�lm�� herhangi bir etkile�im �al��mas� yoktur.
Pediyatrik pop�lasyon:
Pediyatrik pop�lasyon ile yap�lm�� herhangi bir etkile�im �al��mas� yoktur.
Laboratuvar testleri:
Kombine OK ile elde edilen veriler, kontraseptif steroidlerin, karaci�er, tiroid, adrenal bez ve renal i�levlerle ilgili biyokimyasal testler, ta��y�c� proteinlerin serum d�zeyleri �rn; kortikosteroid ba�layan protein ve lipid/ lipoprotein fraksiyonlar�, karbonhidrat metabolizmas� parametreleri ve p�ht�la�ma ve fibrinoliz parametreleri gibi belli laboratuvar testlerinin sonu�lar�n� etkileyebilece�ini g�stermi�tir. De�i�iklikler genellikle normal s�n�rlar i�inde kalmaktad�r. Yaln�zca progestagen i�eren kontraseptiflerin etki derecesi bilinmemektedir.
4.6. Gebelik ve laktasyon
Gebelik kategorisi: X
�ocuk do�urma potansiyeli bulunan kad�nlar/Do�um kontrol� (Kontrasepsiyon)
Bu t�bbi �r�n�n endikasyonu kontrasepsiyon oldu�u i�in bu ba�l�k ge�erli de�ildir.
Gebelik d�nemi
NEXPLANON gebelik d�neminde uyguland��� taktirde ciddi do�um kusurlar�na yol a�maktad�r/yol a�t���ndan ��phelenilmektedir.
NEXPLANON gebelik s�ras�nda kontrendikedir. NEXPLANON kullan�m� s�ras�nda gebelik ortaya ��karsa, NEXPLANON ��kar�lmal�d�r. Hayvan �al��malar� �ok y�ksek doz progestagenik maddelerin di�i f�tuslarda mask�linizasyona yol a�abildi�ini g�stermi�tir. Yayg�n epidemiyolojik �al��malarda, gebelik �ncesinde OK kullanan kad�nlar�n �ocuklar�nda do�um defekti art��� ya da gebelik s�ras�nda istenmeden kullan�ld���nda teratojenik etki saptanmam��t�r. Olas�l�kla b�t�n OK'ler ile ilgili olmas�na kar��n, bu durumun NEXPLANON i�in de ge�erli olup olmad��� belli de�ildir.
Etonogestrel- ve desogestrel- i�eren �e�itli �r�nler (etonogestrel, desogestrelin bir metabolitidir) ile ili�kili farmakovijilans verileri risk art��� g�stermemi�tir.
Laktasyon d�nemi
Klinik veriler, NEXPLANON anne s�t�n�n �retimini ve niteli�ini (protein, laktoz ya da ya� konsantrasyonu) etkilemedi�ini bildirir. Bununla birlikte, etonogestrel anne s�t�ne az miktarda ge�er. G�nl�k ortalama 150 mL/kg s�t t�ketimi temelinde, etonogestrel sal�m�ndan bir ay sonra bebekte saptanan etonogestrel dozu g�nl�k ortalama yakla��k 27 nanogram/kg/g�n olmu�tur. Yakla��k olarak bu, v�cut a��rl���na g�re d�zeltilmi� maternal g�nl�k dozun yakla��k %2,2'sine ve hesaplanan mutlak maternal g�nl�k dozun yakla��k %0,2'sine e�ittir. S�tteki etonogestrel konsantrasyonu laktasyon periyodu s�ras�nda zaman ge�tik�e azal�r.
Do�umdan sonraki 4-8 haftal�k d�nemde implant kullanmaya ba�lam�� annelerin 38 �ocu�una ili�kin uzun d�nemli veri mevcuttur. 38 �ocuk ortalama 14 ay boyunca anne s�t� alm��lar ve
36 ayl�k olana dek izlenmi�lerdir. B�y�me de�erlendirmeleri, fiziksel ve psikomotor geli�imleri, anneleri R�A kullanan bebeklere (n=33) k�yasla fark g�stermemi�tir. Bununla birlikte �ocu�un geli�imi ve b�y�mesi dikkatle izlenmelidir. Var olan veriler temelinde, NEXPLANON laktasyon s�ras�nda kullan�labilir ve do�umdan 4 hafta sonra yerle�tirilebilir.
�reme yetene�i/Fertilite
Etonogestrelin kontraseptif etkilili�i geri d�n��l�d�r, implant ��kar�ld�ktan sonra normal menstr�el d�ng� h�zla geri d�ner.
4.7. Ara� ve makine kullan�m� �zerindeki etkiler
Farmakodinamik profiline g�re, NEXPLANON'un ara� ve makine kullan�m� �zerine etkisi yoktur veya etkisi ihmal edilebilir.
4.8. �stenmeyen etkiler
NEXPLANON kullan�m� s�ras�nda, kad�nlar�n menstr�el kanama d�zeninde �nceden tahmin edilemeyen de�i�iklikler olmas� muhtemeldir. Bu de�i�iklikler �unlar� i�erebilir: kanama s�kl�klar�nda de�i�iklikler (kanama olmamas�, daha az s�kl�kta olmas�, �ok s�k veya devaml� olmas�), kanama yo�unlu�unda de�i�iklikler (azalmas� veya artmas�) veya s�resinde de�i�iklikler. 5 kad�ndan 1'inde amenore bildirilirken, yine 5 kad�ndan 1'inde s�k ve/veya uzun s�reli kanama bildirilmi�tir. Ara s�ra a��r kanama rapor edilmi�tir. Klinik �al��malarda kanama de�i�iklikleri tedavinin b�rak�lmas�nda en yayg�n gerek�e olmu�tur (yakla��k %11). �lk �� aydaki kanama profili bir�ok kad�nda, daha sonraki kanama profillerinin yakla��k olarak tahmin edilmesini sa�lar.
Klinik �al��malarda saptanan olas� ili�kili istenmeyen etkiler MedDRA sistemine g�re a�a��da belirtilmektedir.
�ok yayg�n (≥1/10); yayg�n (≥1/100 ila ≤1/10); yayg�n olmayan (≥1/1.000 ila ≤1/100); seyrek (≥1/10.000 ila ≤1/1.000); �ok seyrek (≤1/10.000), bilinmiyor (eldeki verilerden hareketle tahmin edilemiyor).
Enfeksiyonlar ve enfestasyonlar
�ok yayg�n: Vajinal enfeksiyon
Yayg�n olmayan: Farenjit, rinit, idrar yolu enfeksiyonu
Ba����kl�k sistemi hastal�klar�
Yayg�n olmayan: A��r� duyarl�l�k
Metobolizma ve beslenme hastal�klar�
Yayg�n: ��tah artmas�
Psikiyatrik hastal�klar
Yayg�n: Duygulan�mda de�i�kenlik, depresif duygudurum, sinirlilik, libido azalmas� Yayg�n olmayan: Anksiyete, insomnia
Sinir sistemi hastal�klar�
�ok yayg�n: Ba� a�r�s�
Yayg�n: Ba� d�nmesi (sersemlik hali)
Yayg�n olmayan: Migren, somnolans
Vask�ler hastal�klar
Yayg�n: S�cak basmas�
Gastrointestinal hastal�klar
Yayg�n: Kar�n a�r�s�, bulant�, flatulans Yayg�n olmayan: Kusma, kab�zl�k,ishal
Deri ve derialt� doku hastal�klar�
�ok yayg�n: Akne
Yayg�n: Sa� d�k�lmesi
Yayg�n olmayan: Hipertrikoz, ka��nt�, d�k�nt�
Kas-iskelet bozukluklar�, ba� doku ve kemik hastal�klar�
Yayg�n olmayan: S�rt a�r�s�, artralji, miyalji, iskelet kas a�r�s�
B�brek ve idrar yolu hastal�klar�
Yayg�n olmayan: Diz�ri
�reme sistemi ve meme hastal�klar�
�ok yayg�n: Memede hassasiyet; memede a�r�, d�zensiz menstur�asyon Yayg�n: Dismenore, over kisti
Yayg�n olmayan: Genital ak�nt�, vulvovajinal rahats�zl�k, galaktore, meme b�y�mesi, genital
ka��nt�
Genel bozukluklar ve uygulama b�lgesine ili�kin hastal�klar
Yayg�n: �mplant yerinde a�r�, implant yerinde reaksiyon, yorgunluk, grip benzeri hastal�k, a�r�
Yayg�n olmayan: Y�ksek ate�, �dem
Ara�t�rmalar
�ok yayg�n: V�cut a��rl���nda art�� Yayg�n: V�cut a��rl���nda azalma
Pazarlama sonras� g�zlemler s�ras�nda, seyrek durumlarda klinik olarak anlaml� kan bas�nc� y�kselmesi g�zlenmi�tir. Sebore de bildirilmi�tir. Anafilaktik reaksiyonlar, �rtiker, anjio�dem, anjio�dem agrevasyonu ve/veya herediter anjio�dem agrevasyonu ortaya ��kabilir.
�mplant�n yerle�tirilmesi veya ��kar�lmas� prosed�r� ile ba�lant�l� olarak a�a��daki istenmeyen etkiler bildirilmi�tir:
�mplant�n yerle�tirilmesi ya da ��kar�lmas� morarma, baz� durumlarda hematom dahil, hafif lokal iritasyon, a�r� ya da ka��nt�ya neden olabilir.
�mplant�n yerle�tirilmesi vazovagal reaksiyonlara (hipotansiyon, ba� d�nmesi veya senkop gibi) neden olabilir.
�mplant b�lgesinde fibroz meydana gelebilir, skar ya da apse olu�abilir. Parestezi ya da parestezi benzeri olaylar olu�abilir. G���s duvar� da dahil olmak �zere implant�n ��kmas� ya da yer de�i�tirmesi raporlanm��t�r. Nadir durumlarda, implant pulmoner arteri de i�erecek �ekilde damarda bulunmu�tur. �mplant�n pulmoner arterde bulundu�u baz� durumlarda g���ste ac� ve/veya solunum yolu hastal�klar� (�rne�in dispne, �ks�r�k, hemoptiz) raporlanm��t�r; di�erleri asemptomatik olarak raporlanm��t�r (ayn� zamanda bkz. B�l�m 4.4.). Talimatlara uyulmazsa (bkz. B�l�m 4.2) hatal� yerle�tirme, lokalizasyonda zorlanma ve implant�n ��kar�lmas�nda zorlanma ger�ekle�ebilir. �mplant ��kar�l�rken cerrahi giri�im gerekebilir.
Seyrek olarak ektopik gebelik bildirilmi�tir (bkz. b�l�m 4.4.).
Kombine oral (kontraseptif) kullanan kad�nlarda birka� (ciddi) istenmeyen etki bildirilmi�tir. Bunlar, ven�z tromboembolik hastal�klar, arteriyel tromboembolik hastal�klar, hormon-ba��ml� t�m�rler (�rn; karaci�er t�m�rleri, meme kanseri) ve kloasma, b�l�m 4.4'de daha detayl� olarak tart���lm��t�r.
��pheli advers reaksiyonlar�n raporlanmas�
Ruhsatland�rma sonras� ��pheli ila� advers reaksiyonlar�n�n raporlanmas� b�y�k �nem ta��maktad�r. Raporlama yap�lmas�, ilac�n yarar/risk dengesinin s�rekli olarak izlenmesine olanak sa�lar. Sa�l�k mesle�i mensuplar�n�n herhangi bir ��pheli advers reaksiyonu T�rkiye Farmakovijilans Merkezi (T�FAM)'ne bildirmeleri gerekmektedir (www.titck.gov.tr; eposta: tufam@titck.gov.tr; tel: 0 800 314 00 08; faks: 0 312 218 35 99).
4.9. Doz a��m� ve tedavisi
Bir implant her zaman yenisi yerle�tirilmeden �nce ��kar�lmal�d�r. Etonogestrel ile ili�kili doz a��m� verisi bulunmamaktad�r. Genel olarak kontraseptif doz a��m�n�n ciddi zararl� etkilerini bildiren rapor bulunmamaktad�r.
 Rahim Boyu ( Serviks ) Kanseri
Rahim boynu (serviks) kanseri 35 ya� alt� kad�nlarda g�r�len vakalarda meme kanserinden
sonra ikinci s�ray� al�r.Serviks kanserinin geli�mesi y�llarca s�rebilir.
Rahim Boyu ( Serviks ) Kanseri
Rahim boynu (serviks) kanseri 35 ya� alt� kad�nlarda g�r�len vakalarda meme kanserinden
sonra ikinci s�ray� al�r.Serviks kanserinin geli�mesi y�llarca s�rebilir. |
 Depresyonu Anlamak
Depresyon farkl� ki�ileri farkl� bi�imlerde etkiler. Duygusal veya fiziksel
olmak �zere geni� alanda belirtilere sebep olabilir.Depresyona neler sebep olur?
Depresyonu Anlamak
Depresyon farkl� ki�ileri farkl� bi�imlerde etkiler. Duygusal veya fiziksel
olmak �zere geni� alanda belirtilere sebep olabilir.Depresyona neler sebep olur? |
�LA� GENEL B�LG�LER�
Organon Turkey �la�lar� Ltd. �ti.
| Sat�� Fiyat� | 4064.7 TL [ 10 May 2024 ] |
| �nceki Sat�� Fiyat� | 4064.7 TL [ 3 May 2024 ] |
| Original / Jenerik | Original �la� |
| Re�ete Durumu | Normal Re�eteli bir ila�d�r. |
| Barkodu | 8683280337299 |
| Etkin Madde | Etonogestrel |
| ATC Kodu | G03AC08 |
| Birim Miktar | 68 |
| Birim Cinsi | MG |
| Ambalaj Miktar� | 1 |
| �rogenital Sistem ve Cinsiyet Hormonlar� > Sistemik Hormonal Gebeli�i �nleyici �la�lar > Etonogestrel |
| �thal ( ref. �lke : Italya ) ve Be�eri bir ila�d�r. |
�LA� E�DE�ERLER�
| E�de�er �la� Ad� | Barkodu | �la� Fiyat� |
|---|---|---|
| E�de�er bir ila� bulunamad� |
 |
Rahim Boyu ( Serviks ) Kanseri Rahim boynu (serviks) kanseri 35 ya� alt� kad�nlarda g�r�len vakalarda meme kanserinden sonra ikinci s�ray� al�r.Serviks kanserinin geli�mesi y�llarca s�rebilir. |
 |
Diyabet Hastal��� Diyabet, ins�lin hormonu ile ilgili problemlerden kaynaklanan bir hastal�kt�r. |
 |
HIV ve Aids HIV, Human Immunodeficiency Virus’d�r (�nsanlarda Ba����kl�k Sistemini Bozan Vir�sd�r). Bu vir�s AIDS hastal���na sebep olur. |