TEMOMID 5 mg 20 kaps�l K�sa �r�n Bilgisi
{ Temozolomid }
1. BE�ER� TIBB� �R�N�N ADI
TEMOM�D 5 mg Kaps�l Sitotoksik
2. KAL�TAT�F VE KANT�TAT�F B�LE��M
Etkin madde
Temozolomid 5 mg
Yard�mc� maddeler
Laktoz anhidr�z (s���r s�t� kaynakl�) 68,19 mg Yard�mc� maddeler i�in 6.1'e bak�n�z.
3. FARMAS�T�K FORMU
Sert kaps�l.
Sert kaps�ller opak beyaz g�vdeli ve opak f�st�k ye�ili kapakl� olup, a��k pembe renkli toz i�erir.
4. KL�N�K �ZELL�KLER
4.1. Terap�tik endikasyonlar
TEMOM�D, birinci basamakta yeni tan� konmu� glioblastoma multiforme tedavisinde radyoterapi ile birlikte ve sonras�nda endikedir.
TEMOM�D, standart tedaviden sonra n�kseden veya progresyon g�steren glioblastoma multiforme veya anaplastik astrositoma gibi malign glioma hastalar�nda endikedir.
TEMOM�D, metastatik malign melanomlu hastalar�n tedavisinde endikedir.
4.2. Pozoloji ve uygulama �ekli
TEMOM�D sadece beyin t�m�rleri konusunda uzman doktorlar taraf�ndan re�etelendirildi�i zaman kullan�lmal�d�r.
TEMOM�D yemekten en az bir saat �nce, a� karn�na verilmelidir. Uygulamadan �nce veya sonra antiemetik tedavisi uygulanabilir.
TEMOM�D tedavisi hastal���n ilerlemesine kadar maksimum 2 y�l s�rd�r�lebilir.
Yeni te�his edilen glioblastoma multiformeli eri�kin hastalar:
E�zamanl� faz:
TEMOM�D, radyoterapi (30 fraksiyonda verilen 60 Gy) ile e� zamanl� olarak, 42 g�n s�reyle g�nde 75 mg/m dozunda ve takibinde 6 k�r adjuvan tedavi olarak oral yoldan verilir. Doz azalt�lmas� �nerilmez; ama hastan�n tolerans�na g�re doza ara verilebilir. A�a��daki ko�ullar�n t�m� sa�lan�r ise, TEMOM�D ile e� zamanl� d�nem 42 g�nden 49 g�ne kadar s�rd�r�lebilir:
mutlak n�trofil say�s� ≥ 1,5 x 10 /l;
4.3. Kontrendikasyonlar
TEMOM�D,
- Etkin maddeye veya B�l�m 6.1'de listelenen yard�mc� maddelerden herhangi birine a��r� duyarl�l���,
Dakarbazine (DTIC) kar�� a��r� duyarl�l���,
4.4. �zel kullan�m uyar�lar� ve �nlemleri
F�rsat�� enfeksiyonlar ve enfeksiyonlar�n reaktivasyonu
TEMOM�D ile tedavi s�ras�nda f�rsat�� enfeksiyonlar (Pneumocystis jirovecii pn�monisi gibi) ve enfeksiyonlar�n reaktivasyonu (hepatit B vir�s� (HBV), sitomegalovir�s (CMV) gibi) g�zlenmi�tir
(bkz. B�l�m 4.8).
Pneumocystis jirovecii pn�monisi
Bir pilot �al��mada uzat�lm�� 42 g�nl�k �emayla e�zamanl� olarak temozolomid ve radyoterapi alan hastalar�n Pneumocystis jirovecii pn�monisi (PCP) geli�imi y�n�nden �zel bir riske sahip olduklar� g�sterilmi�tir. Bu nedenle, 42 g�nl�k (maksimum 49 g�nl�k) rejimde e� zamanl� temozolomid ve radyoterapi alan b�t�n hastalara lenfosit say�s� ne olursa olsun PCP i�in profilaksi uygulanmas� gerekir. Lenfopeni ortaya ��karsa, hastalar lenfopeni Evre ≤1'e gerileyinceye kadar profilaksiye devam etmelidir.
Temozolomidin, daha uzun s�reli bir dozaj rejiminde kullan�lmas� durumunda PCP g�r�lme s�kl��� artabilir. Ancak, temozolomid alan t�m hastalar, �zellikle de steroid kullanan hastalar, doz rejimine bak�lmaks�z�n PCP a��s�ndan yak�ndan izlenmelidir. �zellikle deksametazon veya di�er steroidlerle birlikte temozolomid kullanan hastalarda �l�mc�l solunum yetmezli�i vakalar� rapor edilmi�tir.
HBV
�l�mle sonu�lanan baz� vakalarda, hepatit B vir�s� (HBV) reaktivasyonuna ba�l� hepatit rapor edilmi�tir. Pozitif hepatit B serolojisi olan hastalarda (aktif hastal��� olanlar da dahil) tedaviye ba�lanmadan �nce karaci�er hastal���nda uzmanlara dan���lmal�d�r. Tedavi s�ras�nda hastalar izlenmeli ve uygun �ekilde tedavi edilmelidir.
Herpetik meningoensefalit
Pazarlama sonras� vakalarda, e� zamanl� steroid kullanan vakalar dahil, radyoterapi ile birlikte temozolomid alan hastalarda herpetik meningoensefalit (�l�mle sonu�lanan vakalar dahil) g�r�lm��t�r.
Hepatotoksisite
Temozolomid ile tedavi edilen hastalarda �l�mc�l karaci�er yetmezli�i dahil olmak �zere karaci�er hasar� bildirilmi�tir (bkz. B�l�m 4.8). Tedaviye ba�lamadan �nce karaci�er fonksiyon testleri yap�lmal�d�r. Bu testler anormal ise, hekimler temozolomide ba�lamadan �nce �l�mc�l karaci�er yetmezli�i potansiyeli dahil risk/yarar oran�n� de�erlendirmelidir. 42 g�nl�k tedavi k�r� alan hastalarda, karaci�er fonksiyon testleri bu k�r�n ortalar�nda tekrarlanmal�d�r. T�m hastalarda, her bir tedavi k�r�nden sonra karaci�er fonksiyon testleri yap�lmal�d�r. Anlaml� karaci�er fonksiyon anormallikleri saptanan hastalarda hekimler tedaviye devam edilmesinin risk/yarar oran�n� de�erlendirmelidir. En son temozolomid tedavisinden birka� hafta sonra veya daha sonra karaci�er toksisitesi meydana gelebilir.
Maligniteler
�ok nadir olarak miyeloid l�semi dahil olmak �zere miyelodisplastik sendrom ve sekonder malignite vakalar� bildirilmi�tir (bkz. B�l�m 4.8).
Antiemetik tedavi
Bulant� ve kusma temozolomid tedavisiyle �ok yayg�n �ekilde g�r�l�r. TEMOM�D uygulanmadan �nce veya uyguland�ktan sonra anti-emetik tedavi uygulanabilir.
Yeni te�his edilen glioblastoma multiformeli eri�kin hastalar i�in:
E� zamanl� faz�n ba�lang�� dozundan �nce anti-emetik profilaksisi �nerilir ve monoterapi faz�nda anti-emetik profilaksisi kuvvetle �nerilir.
Rek�rran veya progresif malign gliomas� olan hastalar:
�nceki tedavi k�rlerinde �iddetli (evre 3 veya 4) kusma ya�ayan hastalarda antiemetik tedavi gerekebilir.
Laboratuvar parametreleri
TEMOM�D ile tedavi edilen hastalar uzun s�ren pansitopeni dahil miyelosupresyon ya�ayabilir; bu durum baz� vakalarda �l�mle sonu�lanan aplastik anemiye neden olabilir. Baz� vakalarda karbamazepin, fenitoin ve s�lfametoksazol/trimetoprim gibi aplastik anemiyle ili�kili t�bbi �r�nlere e� zamanl� maruz kal�m de�erlendirmeyi karma��kla�t�r�r. Tedaviden �nce a�a��daki laboratuvar parametreleri kar��lanmal�d�r: MNS ≥ 1,5 x 10/l ve trombosit say�s� ≥ 100 x 10/l. �lk dozdan 21 g�n sonra (22. g�nde) veya o g�nden sonraki 48 saat i�indetam kan say�m� yap�lmal� ve MNS 1,5 x 10/l' nin �zerine ve trombosit say�s� 100 x 10/l'nin �zerine ��k�ncaya kadar haftada bir tam kan say�m� yap�lmal�d�r. Herhangi bir k�rde MNS 1,0 x 10/l'nin alt�na veya trombosit say�s� 50 x 10/l'nin alt�na d��erse bir sonraki k�rde 1 doz d�zeyi azalt�lmal�d�r (bkz. B�l�m 4.2). Doz d�zeyleri 100 mg/m, 150 mg/m ve 200 mg/m'dir. �nerilen en d���k doz 100 mg/m'dir.
Pediyatrik kullan�m:
�� ya��n alt�ndaki �ocuklarda temozolomid kullan�m�na ili�kin klinik deneyim yoktur. Daha b�y�k ya�taki �ocuklarda ve ergenlerde deneyim �ok s�n�rl�d�r (bkz. B�l�m 4.2 ve 5.1).
Ya�l� hastalarda kullan�m (70 ya� �zeri):
Ya�l� hastalarda gen� hastalara g�re n�tropeni ve trombositopeni riski daha fazlad�r. Bu nedenle, ya�l� hastalarda TEMOM�D kullan�m�nda dikkatli olunmal�d�r.
Erkek hastalar:
TEMOM�D ile tedavi edilen erkeklerin son dozu ald�ktan sonraki 6. aya kadar �ocuk sahibi olmamalar� ve tedaviden �nce spermlerin dondurularak korunmas� konusunda tavsiye almalar� �nerilir (bkz. B�l�m 4.6).
Di�er:
TEMOM�D 68,19 mg laktoz i�erir. Nadir kal�t�msal galaktoz intolerans�, Lapp laktaz yetmezli�i ya da glukoz-galaktoz malabsorpsiyon problemi olan hastalar�n bu ilac� kullanmamalar� gerekir.
4.5. Di�er t�bbi �r�nler ile etkile�imler ve di�er etkile�im �ekilleri
Ayr� bir faz I �al��mada, ranitidinle birlikte temozolomid uygulamas� temozolomidin emilim derecesinde ya da onun aktif metaboliti monometil triazenoimidazol karboksamide (MTIC) maruz kal�mda de�i�ikliklere yol a�mam��t�r.
Temozolomid yemekle birlikte uyguland���nda C'daki %33'l�k azalma ve EAA'da %9'luk azalma g�r�lm��t�r. C'daki de�i�imin klinik anlaml�l��� bertaraf edilemeyece�inden, temozolomid yemekle birlikte uygulanmamal�d�r.
Faz II �al��malardaki pop�lasyon farmakokineti�i �zerinde yap�lan bir analize dayanarak deksametazon, proklorperazin, fenitoin, karbamazepin, ondansetron, Hresept�r antagonistleri veya fenobarbital ile birlikte uygulanmas�, temozolomidin klerensini de�i�tirmemektedir. Valproik asit ile birlikte uygulanmas� durumunda temozolomid klerensinde k���k fakat istatistiksel olarak anlaml� bir azalma meydana gelmektedir.
Temozolomidin di�er t�bbi �r�nlerin metabolizmas� ya da eliminasyonu �zerindeki etkilerini belirlemek amac�yla hi�bir �al��ma yap�lmam��t�r. Bununla beraber temozolomid karaci�erde metabolize edilmedi�i ve proteinlere d���k oranda ba�land��� i�in, di�er t�bbi �r�nlerin farmakokineti�ini etkilemesi muhtemel de�ildir (bkz. B�l�m 5.2).
Temozolomid ile di�er miyelosupresif ajanlar�n kombine kullan�m�, miyelosupresyon olas�l���n� art�rabilir.
�zel pop�lasyonlara ili�kin ek bilgiler
Herhangi bir veri yoktur.
Pediyatrik pop�lasyon
Etkile�im �al��malar� yaln�zca eri�kinlerde yap�lm��t�r.
4.6. Gebelik ve laktasyon
Gebelik kategorisi: D
�ocuk do�urma potansiyeli bulunan kad�nlar/ Do�um kontrol� (Kontrasepsiyon)
�ocuk do�urma potansiyeli olan kad�nlara TEMOM�D kullan�m� s�ras�nda gebeli�i �nlemek i�in etkili kontrasepsiyon kullanmalar� tavsiye edilmelidir.
Gebelik d�nemi
Temozolomid'in gebe kad�nlarda kullan�m�na ili�kin veri mevcut de�ildir. 150 mg/m temozolomid alan fare ve tav�anlarda yap�lan klinik �ncesi �al��malarda teratojenite ve/veya fetal toksisite g�sterilmi�tir (bkz. B�l�m 5.3). TEMOM�D, gebe kad�nlara verilmemelidir. Gebelikte kullan�lmas� d���n�l�yorsa, hasta fetusa y�nelik potansiyel risk konusunda bilgilendirilmelidir.
Laktasyon d�nemi
Temozolomidin anne s�t�ne ge�ip ge�medi�i bilinmedi�inden TEMOM�D emziren kad�nlarda kullan�lmamal�d�r.
�reme yetene�i/ Fertilite
S��an ve k�peklerde erkek �reme sisteminde toksisite g�sterilmi�tir (bkz. B�l�m 5.3).
Erkek fertilitesi
Temozolomidin genotoksik etkileri olabilir. Bu nedenle temozolomid ile tedavi edilen erkeklere son dozu ald�ktan sonra 6 aya kadar �ocuk sahibi olmamalar� ve temozolomid tedavisine ba�l� geri
d�n��s�z infertilite olas�l��� nedeniyle tedaviden �nce spermlerini dondurarak saklamalar� (kriyokonservasyon) �nerilmelidir.
4.7. Ara� ve makine kullan�m� �zerindeki etkiler
TEMOM�D bitkinlik ve uyku hali nedeniyle ara� ve makine kullanma becerisi �zerinde hafif bir etki g�sterebilir (bkz. B�l�m 4.8).
4.8. �stenmeyen etkiler
G�venlilik profilinin �zeti
Klinik �al��ma deneyimi
Klinik �al��malarda temozolomid ile tedavi edilen hastalarda bildirilen en yayg�n advers reaksiyonlar bulant�, kusma, konstipasyon, anoreksi, ba� a�r�s�, yorgunluk, konv�lsiyonlar ve d�k�nt�d�r. Hematolojik advers reaksiyonlar�n �o�u yayg�n �ekilde raporlanm��t�r; derece 3-4 laboratuvar bulgular�n�n s�kl��� Tablo 4'den sonra sunulmaktad�r.
Rek�rren ve progresif gliomal� hastalarda bulant� (%43) ve kusma (%36) genellikle derece 1 veya 2'dir (24 saatte 0 – 5 kusma episodu) ve kendini s�n�rlayan tarzdad�r veya standart antiemetik tedaviyle kolayca kontrol alt�na al�nabilmi�tir. �iddetli bulant� ve kusma insidans� %4'd�r.
Advers reaksiyonlar�n tablola�t�r�lm�� listesi
Klinik �al��malarda g�zlenen ve temozolomid'in pazarlama sonras� kullan�m� s�ras�nda bildirilen advers reaksiyonlar Tablo 4'de listelenmektedir.
Bu reaksiyonlar Sistem Organ S�n�f� ve s�kl��a g�re s�n�flanmaktad�r. S�kl�k gruplamalar� a�a��daki standart oranlara g�re tan�mlanmaktad�r: �ok yayg�n (≥ 1/10); yayg�n (≥ 1/100 ila <1/10); yayg�n olmayan (≥ 1/1.000 ila < 1/100); seyrek (≥ 1/10.000 ila < 1/1.000); �ok seyrek (< 1/10.000); bilinmiyor: eldeki verilerden hareketle tahmin edilemiyor. Her bir s�kl�k gruplamas�nda istenmeyen etkiler azalan ciddiyet s�ras�yla sunulmaktad�r.
Tablo 4. Temozolomid ile tedavi edilen hastalarda bildirilen advers reaksiyonlar | |
Enfeksiyonlar ve enfestasyonlar | |
Yayg�n: | Enfeksiyonlar, herpes zoster, farenjit, oral kandidiyazis |
Yayg�n olmayan: | F�rsat�� enfeksiyon (PCP dahil), sepsis†, herpetik meningoensefalit†, CMV enfeksiyonu, CMV reaktivasyonu, hepatit B vir�s�†, herpes simpleks, enfeksiyon reaktivasyonu, yara enfeksiyonu, gastroenterit |
(Kist ve polipler de dahil olmak �zere) �yi huylu ve k�t� huylu neoplazmalar | |
Yayg�n olmayan: | Miyelodisplastik sendrom (MDS), sekonder maligniteler (miyeloid l�semi dahil) |
Kan ve lenf sistemi hastal�klar� | |
Yayg�n: | Febril n�tropeni, n�tropeni, trombositopeni, lenfopeni, l�kopeni, anemi |
Yayg�n olmayan: | Uzam�� pansitopeni, aplastik anemi†, pansitopeni, pete�i |
Ba����kl�k sistemi hastal�klar� | |
Yayg�n: | Alerjik reaksiyon |
Yayg�n olmayan: | Anaflaksi |
Endokrin hastal�klar | |
Yayg�n: | Cushingoid |
Yayg�n olmayan: | Diabetes insipidus |
Metabolizma ve beslenme hastal�klar� | |
�ok yayg�n: | Anoreksi |
Yayg�n: | Hiperglisemi |
Yayg�n olmayan: | Hipokalemi, alkalen fosfataz art��� |
Psikiyatrik hastal�klar | |
Yayg�n: | Ajitasyon, amnezi, depresyon, anksiyete, konf�zyon, insomni |
Yayg�n olmayan: | Davran�� bozuklu�u, emosyonel labilite, hal�sinasyonlar, apati |
Sinir sistemi hastal�klar� | |
�ok yayg�n: | Konv�lsiyonlar, hemiparezi, afazi/disfazi, ba� a�r�s� |
Yayg�n: | Ataksi, denge bozuklu�u, bili�sel bozukluk, konsantrasyon bozuklu�u, bilin� azalmas�, ba� d�nmesi, hipoestezi, haf�za bozuklu�u, n�rolojik bozukluk, n�ropati , parestezi, somnolans, konu�ma bozuklu�u, tat duyumunda de�i�iklik, tremor |
Yayg�n olmayan: | Status epileptikus, hemipleji, ekstrapiramidal bozukluk, parosmi, y�r�mede anormallik, hiperestezi, duyusal bozukluk, anormal koordinasyon |
G�z hastal�klar� | |
Yayg�n: | Hemianopi, bulan�k g�rme, g�rme bozuklu�u, g�rme alan� defekti, diplopi, g�z a�r�s� |
Yayg�n olmayan: | G�rme keskinli�inde azalma, g�zlerde kuruluk |
Kulak ve i� kulak hastal�klar� | |
Yayg�n: | Sa��rl�k, vertigo, tinnitus, kulak a�r�s� |
Yayg�n olmayan: | ��itme bozuklu�u, hiperakuzi, otitis media |
Kardiyak hastal�klar | |
Yayg�n olmayan: | Palpitasyon |
Vask�ler hastal�klar | |
Yayg�n: | Hemoraji, pulmoner emboli, derin ven trombozu, hipertansiyon |
Yayg�n olmayan: | Serebral hemoraji, y�zde ve boyunda k�zar�kl�k, s�cak basmas� |
Solunum, g���s bozukluklar� ve mediastinal hastal�klar | |
Yayg�n: | Pn�moni, dispne, sin�zit, bron�it, �ks�r�k, �st solunum yolu enfeksiyonu |
Yayg�n olmayan: | Solunum yetmezli�i†, interstisyel pn�monit/pn�monit, pulmoner fibroz, nazal konjesyon |
Gastrointestinal hastal�klar | |
�ok yayg�n: | Diyare, konstipasyon, bulant�, kusma |
Yayg�n: | Stomatit, abdominal a�r�, dispepsi, disfaji |
Yayg�n olmayan: | Abdominal distansiyon, fekal inkontinans, gastrointestinal bozukluk, hemoroidler, a��z kurulu�u |
Hepato-bilier hastal�klar | |
Yayg�n olmayan: | Karaci�er yetmezli�i†, karaci�er hasar�, hepatit, kolestaz, hiperbilir�binemi |
Deri ve deri alt� doku hastal�klar� | |
�ok yayg�n: | D�k�nt�, alopesi |
Yayg�n: | Eritem, cilt kurulu�u, prurit |
Yayg�n olmayan: | Toksik epidermal nekroliz, Stevens-Johnson sendromu, anjiyo�dem, eritema multiforme, eritroderma, deri soyulmas�, fotosensitivite reaksiyonu, �rtiker, ekzantem, dermatit, terleme art���, anormal pigmentasyon |
Bilinmiyor: | Eozinofili ve sistemik semptomlar�n e�lik etti�i ila� reaksiyonu (DRESS) |
Kas-iskelet bozukluklar�, ba� doku ve kemik hastal�klar� | |
Yayg�n: | Miyopati, kas g��s�zl���, artralji, s�rt a�r�s�, kas- iskelet a�r�s�, miyalji |
B�brek ve idrar yolu hastal�klar� | |
Yayg�n: | S�k idrara ��kma, �riner inkontinans |
Yayg�n olmayan: | Diz�ri |
�reme sistemi ve meme hastal�klar� | |
Yayg�n olmayan: | Vajinal hemoraji, menoraji, amenore, vajinit, meme a�r�s�, impotans |
Genel bozukluklar ve uygulama b�lgesine ili�kin hastal�klar | |
�ok yayg�n: | Yorgunluk |
Yayg�n: | Ate�, grip benzeri semptomlar, asteni, halsizlik, a�r�, �dem, periferik �dem |
Yayg�n olmayan: | Durumda a��rla�ma, rigor, y�zde �dem, dil renginde de�i�iklik, susama, di� hastal��� |
Ara�t�rmalar | |
Yayg�n: | Karaci�er enzimlerinde y�kselme, v�cut a��rl���nda azalma, v�cut a��rl���nda artma |
Yayg�n olmayan: | Gama-glutamiltransferaz art��� |
Yaralanma, zehirlenme ve prosed�re ba�l� komplikasyonlar | |
Yayg�n: | Radyasyona ba�l� hasar |
† �l�mle sonu�lanan vakalar� i�erir
Yeni te�his edilen glioblastoma multiformeli hastalar:
Laboratuvar sonu�lar�:
Temozolomid dahil �o�u sitotoksik ajan i�in doz k�s�tlay�c� oldu�u bilinen miyelosupresyon (n�tropeni ve trombositopeni) g�zlemlenmi�tir. E� zamanl� ve monoterapi tedavi fazlar� i�in laboratuvar anormallikleri ve advers olaylar kombine edildi�inde, n�tropenik olaylar dahil evre 3 veya evre 4 n�trofil anormallikleri hastalar�n %8'inde g�zlenmi�tir. Trombositopenik olaylar dahil evre 3 veya evre 4 trombosit anormallikleri temozolomid alan hastalar�n %14'�nde g�zlenmi�tir.
Rek�rran veya progresif malign gliomal� hastalar:
Laboratuvar sonu�lar�:
Evre 3 veya 4 trombositopeni ve n�tropeni malign glioma i�in tedavi edilen hastalar�n s�ras�yla
%19 ve %17'sinde g�r�lm��t�r. Bu durum hastalar�n s�ras�yla %8 ve %4'�nde temozolomid
tedavisinin kesilmesini ve/veya hospitalizasyonu gerektirmi�tir. Miyelosupresyon tahmin edilebilir olup (genellikle ilk birka� k�rde, en d���k noktas� 21 ve 28. g�nler aras�nda g�r�lm��), d�zelme h�zl� ve genellikle 1-2 hafta i�inde olmu�tur. K�m�latif miyelosupresyona ili�kin kan�tlar g�zlenmemi�tir. Trombositopeni varl��� kanama riskini artt�rabilir ve n�tropeni veya l�kopeni varl��� enfeksiyon riskini artt�rabilir.
Cinsiyet:
Klinik �al��ma deneyiminin pop�lasyon farmakokinetik analizinde 101 kad�n ve 169 erkek hastadaki en d���k mutlak n�trofil say�s� ve 110 kad�n ve 174 erkek hastadaki en d���k mutlak trombosit say�s� kaydedilmi�tir. Evre 4 n�tropeni, (MNS <500 h�cre/mikrolitre), tedavinin 1. k�r�nde kad�nlarda % 12, erkeklerde %5, trombositopeni (< 20,000 h�cre/mikrolitre) ise kad�nlarda
%9 erkeklerde %3 olarak saptanm��t�r. 400 rek�rran gliomal� hastay� i�eren veri setinde, tedavininilk k�r�nde Evre 4 n�tropeni kad�nlar�n % 8, erkeklerin % 4'�nde geli�irken, Evre 4 trombositopeni kad�nlar�n %8, erkeklerin ise % 3'�nde geli�mi�tir. Yeni glioblastoma multiforme tan�s� konmu� 288 hastay� i�eren bir �al��mada, tedavinin ilk k�r�nde Evre 4 n�tropeni kad�nlar�n % 3'�nde g�r�l�rken erkeklerde bu oran % 0'd�r. Evre 4 trombositopeni ise kad�nlar�n % 1'inde g�r�l�rken erkeklerde bu oran % 0'd�r.
Pediyatrik pop�lasyon
Oral temozolomid n�ks eden beyin sap� gliomas� veya n�ks eden y�ksek dereceli astrositomas� olan pediyatrik hastalarda (3-18 ya� aras�) 28 g�nde bir 5 g�n boyunca uygulanan bir rejimde �al���lm��t�r. Veriler s�n�rl� olmakla birlikte, �ocuklardaki tolerans�n eri�kinlerdekiler ile ayn� olmas� beklenir. �� ya��n alt�ndaki �ocuklarda temozolomidin g�venlili�i belirlenmemi�tir.
![]()
��pheli advers reaksiyonlar�n raporlanmas�
![]()
Ruhsatland�rma sonras� ��pheli ila� advers reaksiyonlar�n�n raporlanmas� b�y�k �nem ta��maktad�r. Raporlama yap�lmas�, ilac�n yarar/risk dengesinin s�rekli olarak izlenmesine olanak sa�lar. Sa�l�k mesle�i mensuplar�n�n herhangi bir ��pheli advers reaksiyonu T�rkiye Farmakovijilans Merkezi (T�FAM)'ne bildirmeleri gerekmektedir (www.titck.gov.tr; e-posta: tufam@titck.gov.tr; tel: 0 800 314 00 08; faks: 0 312 218 35 99).
4.9. Doz a��m� ve tedavisi
Hastalarda 500, 750, 1000 ve 1250 mg/m'lik (5 g�n boyunca k�r ba��na toplam doz) dozlar klinik olarak incelenmi�tir. Doz k�s�tlay�c� toksisite hematolojik toksisitedir ve bir�ok dozda bildirilmi�tir, fakat y�ksek dozlarda daha �iddetli olmas� beklenir. Bir hastada 10,000 mg'l�k (5 g�n boyunca tek bir k�rde toplam doz) doz a��m� ya�anm��t�r. Bildirilen yan etkiler; pansitopeni, pireksi, �oklu organ yetmezli�i ve �l�md�r. 5 g�nden uzun (64 g�ne kadar) tedavide �nerilen dozu alm�� hastalarda enfeksiyon ile birlikte ya da enfeksiyonsuz kemik ili�i supresyonu bildirilmi� ve baz� vakalarda �iddetli ve uzun s�reli olmu� ve �l�m ile sonu�lanm��t�r. Doz a��m� durumunda hematolojik inceleme gerekmektedir. Gerekti�i takdirde destekleyici tedavi uygulanmal�d�r.
5. FARMAKOLOJ�K �ZELL�KLER
5.1. Farmakodinamik �zellikler
Farmakoterap�tik grup: Antineoplastik ajanlar - Di�er alkilleyici ajanlar
ATC Kodu: L01AX03
Etki mekanizmas�
Temozolomid fizyolojik pH'da h�zl� bir kimyasal d�n���m g�stererek aktif bile�en olan monometil triazenoimidazol karboksamide (MT�K) d�n��en bir triazendir. MT�K'nin sitotoksisitesinin, primer olarak guaninin O pozisyonunun alkilasyonundan ve ilaveten N pozisyonunda alkilasyonundan ileri geldi�i d���n�lmektedir. Bunu takiben geli�en sitotoksik lezyonlar�n, metil kat�l�m�n�n anormal onar�m� ile ilgili oldu�u d���n�lmektedir.
Klinik etkililik ve g�venlilik
Yeni te�his edilen glioblastoma multiforme
Toplam 573 hasta temozolomid + RT (n=287) veya tek ba��na RT (n=286) almak �zere randomize edilmi�tir. Temozolomid + RT kolundaki hastalar RT'nin ilk g�n�nden itibaren RT'nin son g�n�ne kadar 42 g�n s�reyle (maksimum 49 g�n) g�nde bir kez e� zamanl� temozolomid (75 mg/m) alm��t�r. Bunu RT'nin bitiminden sonraki 4 haftadan ba�layarak 6 k�re kadar, 28 g�nl�k her bir k�r�n 1-5. g�nlerinde verilen temozolomid monoterapisi (150- 200 mg/m) izlemi�tir. Kontrol kolundaki hastalar yaln�zca RT alm��t�r. RT ve kombine temozolomid tedavisi s�resince Pnemocytis jirovecii pn�monisine (PCP) y�nelik profilaksi gerekmi�tir.
Tek ba��na RT kolundaki 282 hastadan 161'i (% 57) ve temozolomid + RT kolundaki 277 hastadan 62'sine (% 22) takip d�neminde kurtar�c� tedavi olarak temozolomid uygulanm��t�r.
Genel sa�kal�m i�in tehlike oran� (HR) 1,59'dur (HR i�in % 95 g�ven aral��� (GA) =1,33 - 1,91) ve log-rank p de�eri temozolomid kolunun lehine < 0,0001'dir. Hesaplanan 2 y�l veya daha uzun s�re hayatta kalma olas�l��� (% 26'ya kar�� % 10) RT + temozolomid kolunda daha y�ksektir. Yeni te�his edilmi� glioblastoma multiformeli hastalar�n tedavisinde RT'ye e� zamanl� temozolomid eklenmesi ve ard�ndan temozolomid monoterapisi tek ba��na RT'ye k�yasla genel sa�kal�mda (OS) istatistiksel olarak anlaml� iyile�me g�stermi�tir (�ekil 1).
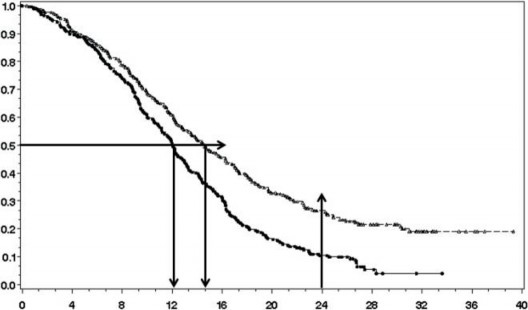
HR (95GA) = 1,59(1,33-1,91)
Log-rank p de�eri <0,0001
%26
RT + TMZ
%10
12,1
14,6
Tek ba��na RT
ITT Pop�lasyonu: Genel Sa�kal�m
Olas�l�k
Randomizasyondan sonra ge�en s�re (ay)
�ekil 1. Genel sa�kal�m i�in Kaplan-Meier e�rileri (ITT (tedavi ama�l�) pop�lasyon)
�al��man�n sonu�lar� performans durumu k�t� olan bir hasta alt grubunda (WHO PS=2, n=70) tutarl� de�ildir ve bu alt grupta genel sa�kal�m ve progresyona kadar ge�en s�re her iki kolda benzerdir. Ancak bu hasta grubunda kabul edilemez risklerin mevcut olmad��� anla��lmaktad�r.
N�ks eden veya ilerleyen malign glioma
Cerrahiden ve RT'den sonra ilerleyen veya n�ks eden glioblastoma multiformeli hastalarda (Karnofski performans durumu [KPS] ≥ 70) klinik etkinlik verileri oral temozolomid ile y�r�t�len iki klinik �al��maya dayanmaktad�r. Bunlardan biri 138 hastada (% 29'u daha �nce kemoterapi alm��t�) y�r�t�len kar��la�t�rmas�z bir �al��ma, di�eri ise toplam 225 hastada (% 67'si daha �nce nitrozo�reye dayal� kemoterapi alm��t�) y�r�t�len, temozolomidin prokarbazin ile kar��la�t�r�ld��� randomize, aktif-kontroll� bir �al��mad�r. Her iki �al��mada, birincil son nokta manyetik rezonans g�r�nt�lemesi veya n�rolojik k�t�le�me ile tan�mlanan progresyonsuz sa�kal�md�r (PFS). Kar��la�t�rmas�z �al��mada 6 ayda PFS % 19, progresyonsuz medyan sa�kal�m s�resi 2,1 ay ve medyan genel sa�kal�m 5,4 ayd�r. MR g�r�nt�lemelerine dayanan objektif yan�t oran� (ORR)
%8'dir.
Randomize, aktif-kontroll� �al��mada temozolomid ile 6 ayda PFS prokarbazine g�re anlaml� olarak daha fazlad�r (% 21'e kar�� % 8 – ki-kare p = 0,008) ve medyan PFS s�ras�yla 2,89 ay ve 1,88 ayd�r (log s�ra p = 0,0063). Temozolomid ve prokarbazin i�in medyan sa�kal�m s�resi s�ras�yla 7,34 ay ve 5,66 ayd�r (log s�ra p = 0,33). Alt� ayda, temozolomid kolunda hayatta kalan hastalar�n oran� (% 60) prokarbazin koluna k�yasla (% 44) anlaml� olarak daha y�ksektir (ki-kare p = 0,019). Daha �nce kemoterapi alm�� hastalarda yarar KPS ≥ 80 olan hastalarda g�sterilmi�tir.
N�rolojik durumda k�t�le�meye kadar ge�en s�reye ili�kin veriler ve performans durumunda k�t�le�meye kadar ge�en s�reye ili�kin veriler prokarbazine g�re temozolomid lehinedir (KPS'nin
<70'e gerilemesi veya en az 30 puan azalma). Bu son noktalarda progresyona kadar ge�en medyan s�reler prokarbazine k�yasla temozolomid ile 0,7 – 2,1 ay daha uzundur (log s�ra p = < 0,01 - 0,03).
N�ks eden anaplastik astrositoma
Anaplastik astrositomal� hastalar�n ilk relapstaki tedavisinde oral temozolomidin g�venlili�ini ve etkilili�ini de�erlendiren �ok-merkezli, ileriye d�n�k bir faz II �al��mada, 6 ayda PFS % 46 ve medyan PFS 5,4 ayd�r. Medyan genel sa�kal�m s�resi 14,6 ayd�r. Merkezi g�zden ge�irmeyi yapan ara�t�rmac�n�n de�erlendirmesine dayanan yan�t oran� tedavi ama�l� pop�lasyonda (ITT) (n=162)
%35'dir (13 tam yan�t ve 43 k�smi yan�t). 43 hastada stabil hastal�k bildirilmi�tir. ITT pop�lasyonunda 6 ayl�k olays�z sa�kal�m oran� %44 ve medyan olays�z sa�kal�m s�resi 4,6 ayd�r; bu rakamlar progresyonsuz sa�kal�m sonu�lar�yla benzerdir. Uygun nitelikteki histoloji pop�lasyonunda etkinlik sonu�lar� benzerdir. Radyolojik objektif yan�ta ula��lmas� veya progresyonsuz durumun korunmas� ya�am kalitesinin korunmas� veya iyile�mesiyle g��l� bi�imde ili�kili bulunmu�tur.
Pediyatrik hastalar:
Oral temozolomid, 28 g�nde bir 5 g�n boyunca g�nl�k olarak uygulanm�� bir rejimde n�ks eden beyin sap� gliomas� ya da n�ks eden y�ksek evreli astrositomu olan pediyatrik hastalarda (3-18 ya� aras�) incelenmi�tir. Temozolomide tolerans eri�kinlerdekine benzerdir.
5.2. Farmakokinetik �zellikler
Genel �zelliklerTemozolomid fizyolojik pH'de esas olarak aktif t�r olan 3-metil-(triazen-1-il)imidazol-4-
karboksamide (MT�K) kendili�inden hidrolize olur. MT�K, p�rin ve n�kleik asit biyosentezinde bilinen bir ara madde olan 5-amino-imidazol-4-karboksamide (A�K) ve aktif alkilleyici t�r oldu�una inan�lan metilhidrazine kendili�inden hidrolize olur. MT�K sitotoksisitesinin, esas olarak guaninin O ve N pozisyonlar�nda olmak �zere DNA alkillenmesinden kaynakland��� d���n�lmektedir. Temozolomid EAA's�na k�yasla MT�K ve A�K'ye maruz kal�m s�ras�yla ~%2,4 ve %23't�r. �n vivo ko�ullarda MT�K'in t'si temozolomidinkine (1,8 saat) benzerdir.
Emilim:
Eri�kin hastalarda oral yoldan uyguland�ktan sonra temozolomid h�zla emilmekte ve dozdan sonra 20 dakika gibi k�sa bir s�rede doruk konsantrasyona ula�maktad�r (ortalama s�re 0,5 ile 1,5 saat). C ile i�aretlenmi� temozolomid oral yolla uyguland�ktan sonra C'nin dozdan sonra 7 g�n boyunca fe�es ile ortalama at�l�m oran� % 0,8 bulunmu�tur; bu oran tam emilimi g�sterir.
Da��l�m:
Temozolomid proteinlere d���k oranda ba�lan�r (% 10-% 20) ve proteine y�ksek oranda ba�lanan maddelerle etkile�mesi beklenmez.
Klinik �ncesi veriler ve insanlarda yap�lan PET �al��malar�, temozolomidin kan beyin bariyerini h�zla ge�ti�ini ve beyin-omurilik s�v�s�nda (BOS) bulundu�unu d���nd�rmektedir. Beyin omurilik s�v�s�na penetrasyonu 1 hastada do�rulanm��t�r ve temozolomidin e�ri alt�nda kalan alan�na g�re BOS maruz kal�m� plazmadakinin yakla��k % 30'u kadard�r; bu bulgu hayvan verileriyle paraleldir.
Biyotransformasyon:
Oral uygulamay� takiben dozun ortalama % 5-% 10'u 24 saat i�inde idrarla de�i�meden ve geriye kalan� ise temozolomid asidi, 5-aminoimidazol-4-karboksamid (A�K) veya tan�mlanmam�� polar metabolitler �eklinde at�lmaktad�r. Plazma konsantrasyonlar� doza-ba��ml� bir tarzda artmaktad�r.
Eliminasyon:
Plazma yar�lanma �mr� (t) yakla��k 1,8 saattir. C'nin eliminasyonu esas olarak b�breklerde ger�ekle�ir.
Do�rusall�k/Do�rusal olmayan durum:
Plazma konsantrasyonlar� doza ba�l� olarak artar. Plazma klerensi, da��l�m hacmi ve yar�lanma �mr� dozdan ba��ms�zd�r.
�zel pop�lasyonlara ili�kin ek bilgiler
Temozolomidin pop�lasyon bazl� farmakokinetik analizi sonucunda plazma temozolomid klerensinin ya�, b�brek fonksiyonu veya t�t�n kullan�m�ndan ba��ms�z oldu�u bulunmu�tur. Di�er bir farmakokinetik �al��mada hafif ilâ orta dereceli hepatik disfonksiyonu bulunan hastalar�n, normal hepatik fonksiyonu olan hastalar ile benzer plazma farmakokinetik profilleri oldu�u g�zlenmi�tir.
Pediyatrik hastalarda e�ri alt�nda kalan alan (EAA) daha b�y�kt�r; ancak, maksimum tolere edilebilen doz (MTD) hem �ocuklar hem de eri�kinlerde k�r ba��na 1000 mg/m'dir.
5.3. Klinik �ncesi g�venlilik verileri
S��anlarda ve k�peklerde tek k�rl�k (5 g�n dozaj, 23 g�nl�k tedavisiz d�nem), �� ve alt� k�rl�k toksisite�al��malar� y�r�t�lm��t�r. Toksisitenin primer hedefleri kemik ili�i, lenforetik�ler sistem, testisler ve gastrointestinal kanald� ve daha y�ksek dozlarda (test edilen s��anlar�n ve k�peklerin % 60-100'�nde �l�mc�l olmu�tur) retina dejenerasyonu g�zlenmi�tir. Erkek �reme sistemi ve retina dejenerasyonunu i�eren istenmeyen olaylar hari�, toksisitenin b�y�k k�sm� geri d�n��l� olma bulgular� sergilemi�tir. Ancak retina dejenerasyonundan sorumlu tutulan dozlar �l�mc�l doz aral���nda oldu�undan ve klinik �al��malarda benzer bir etki g�zlenmedi�inden, bu bulgunun klinik y�nden �nemli oldu�u d���n�lmemi�tir.
Temozolomid embriyotoksik, teratojenik ve genotoksik alkilleyici ajand�r. Temozolomid s��an ve k�peklerde insanlara g�re daha toksiktir ve klinik doz s��an ve k�peklerde minimum �l�mc�l doza yak�nd�r. L�kositlerin ve trombositlerin doza ba�l� olarak azalmalar�, toksisitenin duyarl� birer g�stergesidir. Alt� k�rl�k s��an �al��mas�nda memekarsinomlar�, deride keratoakantoma v e bazal h�creli adenomu i�eren �e�itli neoplazmlar g�zlenmi� ancak k�pek �al��malar�nda t�m�rler veya preneoplastik de�i�iklikler g�zlenmemi�tir. S��anlar�n temozolomidin onkojenik etkilerine �zellikle duyarl� oldu�u anla��lmaktad�r ve ilk t�m�rler dozaja ba�land�ktan sonra 3 ay i�inde
g�r�lm��t�r. Bu latent d�nem bir alkilleyici ajan i�in bile �ok k�sad�r.
Ames/Salmonella ve �nsan Periferik Kan Lenfositi (HPBL) kromozom aberasyonu testlerinin sonu�lar�nda pozitif bir mutajenik yan�t g�r�lm��t�r
6. FARMAS�T�K �ZELL�KLER
6.1. Yard�mc� maddelerin listesi
Laktoz anhidr�z (s���r s�t� kaynakl�) Sodyum ni�asta glikolat
Kolloidal anhidr�z silika Kroskarmelloz sodyum Fumarik asit
Stearik asit
Jelatin (s���r kaynakl�) Titanyum dioksit G�nbat�m� sar�s� Kinolin sar�s�
Patent mavisi V
6.2. Ge�imsizlikler
Uygulanamaz.
6.3. Raf �mr�
24 ay
6.4. Saklamaya y�nelik �zel tedbirler
25°C'nin alt�ndaki oda s�cakl���nda saklay�n�z.
6.5. Ambalaj�n niteli�i ve i�eri�i
Kutuda, beyaz plastik kapakl� renkli cam �i�ede 5 ve 20 kaps�l.
6.6. Be�eri t�bbi �r�nden arta kalan maddelerin imhas� ve di�er �zel �nlemler
Kaps�ller a��lmamal�d�r. Kaps�l�n tahrip olmas� halinde, cilt ya da muk�z membranlar�n kaps�l�n toz i�eri�i ile temas�ndan ka��n�lmal�d�r. Temas oldu�u takdirde b�lge su ve sabunla hemen ve iyice y�kanmal�d�r.
Herhangi bir kullan�lmam�� �r�n ya da at�k materyal, yerel d�zenlemelere uygun olarak at�lmal�d�r.
Hastalara kaps�lleri �ocuklar�n g�remeyece�i ve eri�emeyece�i bir yerde, tercihen kilitli bir dolapta saklamalar� s�ylenmelidir. Kazara yutulmalar� �zellikle �ocuklarda �l�me sebebiyet verebilir.
Kullan�lmam�� olan �r�nler ya da at�k materyaller “T�bbi At�klar�n Kontrol� Y�netmeli�i” ve “Ambalaj At�klar�n�n Kontrol� Y�netmeli�i”ne uygun olarak imha edilmelidir.
Son kullanma tarihi ge�mi� veya kullan�lmayan ila�lar� ��pe atmay�n�z! �evre ve �ehircilik Bakanl���nca belirlenen toplama sistemine veriniz.
Sitotoksik ve sitostatik be�eri t�bbi �r�nlerin kullan�mlar� sonucu bo�alan i� ambalajlar�n�n at�klar� TEHL�KEL� ATIKTIR ve bu at�klar�n y�netimi 2/4/2015 tarihli ve 29314 say�l� Resmî Gazetede yay�mlanan At�k Y�netimi Y�netmeli�ine g�re yap�l�r.
 Mide Kanseri
Mide kanseri genellikle mideyi t�m�yle kaplayan ve mukus �retmekle g�revli h�crelerde ba�lar. Bu kanser tipine adenokarsinom denir.
Mide Kanseri
Mide kanseri genellikle mideyi t�m�yle kaplayan ve mukus �retmekle g�revli h�crelerde ba�lar. Bu kanser tipine adenokarsinom denir. |
 Depresyonu Anlamak
Depresyon farkl� ki�ileri farkl� bi�imlerde etkiler. Duygusal veya fiziksel
olmak �zere geni� alanda belirtilere sebep olabilir.Depresyona neler sebep olur?
Depresyonu Anlamak
Depresyon farkl� ki�ileri farkl� bi�imlerde etkiler. Duygusal veya fiziksel
olmak �zere geni� alanda belirtilere sebep olabilir.Depresyona neler sebep olur? |
�LA� E�DE�ERLER�
| E�de�er �la� Ad� | Barkodu | �la� Fiyat� |
|---|---|---|
| TEMODAL | 8699636150504 | 2,668.70TL |
| TEMOMID | 8699828150442 | |
| TEMOZOLID | 8699769150051 | 2,802.13TL |
| Di�er E�de�er �la�lar |
 |
Grip, So�uk Alg�nl��� ve �ks�r�k Grip ve so�uk alg�nl��� (nezle) semptomlar� aras�ndaki fark� bilmek �nemlidir. So�uk alg�nl��� gripten daha hafif belirtiler g�steren bir solunum yolu hastal���d�r. |
 |
Do�um Sonras� Depresyonu Do�um sonras� depresyonu, do�umdan sonra her on kad�ndan biri taraf�ndan tecr�be edilen stresli bir durumdur. |
 |
Parkinson Hastal��� Hastal�k ilk kez 1817 de �ngiliz doktor James Parkinson taraf�ndan tan�mlanm�� ve Dr. Parkinson hastal��� “sallay�c� fel�” olarak kaleme alm��. |
�LA� GENEL B�LG�LER�
Ko�ak Farma �la� ve Kimya Sanayi A.�.
| Sat�� Fiyat� | 375.12 TL [ 22 Sep 2023 ] |
| �nceki Sat�� Fiyat� | 375.12 TL [ 15 Sep 2023 ] |
| Original / Jenerik | Jenerik �la� |
| Re�ete Durumu | Normal Re�eteli bir ila�d�r. |
| Barkodu | 8699828150404 |
| Etkin Madde | Temozolomid |
| ATC Kodu | L01AX03 |
| Birim Miktar | 5 |
| Birim Cinsi | MG |
| Ambalaj Miktar� | 20 |
| Antineoplastik ve �mm�nomod�lat�r Ajanlar > Alkilleyici Ajanlar > Temozolomid |
| Yerli ve Be�eri bir ila�d�r. |