OPSUMIT 10 mg 28 film kapl� tablet K�sa �r�n Bilgisi
{ Masitentan }
1. BE�ER� TIBB� �R�N�N ADI
OPSUM�T 10 mg film kapl� tablet.
2. KAL�TAT�F VE KANT�TAT�F B�LE��M
Etkin madde
Her film kapl� tablet 10 mg masitentan i�erir.
Yard�mc� maddeler
Her film kapl� tablet,
Laktoz (monohidrat olarak) (s���r kaynakl�) … 37 mg
Lesitin (soya) (E322) 0,06 mg i�erir.
Yard�mc� maddelerin tam listesi i�in b�l�m 6.1'e bak�n�z.
3. FARMAS�T�K FORMU
Film kapl� tablet.
Her iki taraf� "10" oymal�, 5,5 mm, yuvarlak, bikonveks, beyaz ile soluk beyaz aras� tablet.
4. KL�N�K �ZELL�KLER
4.1. Terap�tik endikasyonlar
OPSUM�T, monoterapi veya kombinasyon halinde, WHO Fonksiyonel S�n�f� (FS) II veya
III olan pulmoner arteriyel hipertansiyonlu (PAH, WHO Grup 1) yeti�kin hastalar�n uzun s�reli tedavisinde endikedir.
Etkilili�in g�sterildi�i uzun s�reli PAH �al��mas�na, a��rl�kl� olarak idiyopatik ve kal�tsal PAH, ba� doku hastal�klar� ile ili�kili PAH ve d�zeltilmi� basit konjenital kalp hastal��� ile ili�kili PAH hastalar� dahil edilmi�tir (bkz. B�l�m 5.1).
4.2. Pozoloji ve uygulama �ekli
Tedavi yaln�zca PAH tedavisinde deneyimli bir doktor taraf�ndan ba�lat�lmal� ve izlenmelidir.
Pozoloji /uygulama s�kl��� ve s�resi:
OPSUM�T, yemekle birlikte veya yemekten ba��ms�z olarak g�nde bir kez 10 mg dozunda oral yolla al�n�r.
OPSUM�T her g�n yakla��k olarak ayn� zamanda al�nmal�d�r. Hastaya, bir OPSUM�T dozunu almay� unutursa, m�mk�n olan en k�sa s�rede almas� ve sonraki dozu normal zaman�nda
almas� s�ylenmelidir. Hastaya, bir doz unutulsa bile ayn� anda iki doz almamas� hat�rlat�lmal�d�r.
Uygulama �ekli:
Film kapl� tabletler k�r�lmamal� ve b�t�n halinde suyla birlikte yutulmal�d�r.
�zel pop�lasyonlara ili�kin ek bilgiler:
B�brek yetmezli�i:
Farmakokinetik verilere dayal� olarak, b�brek yetmezli�i olan hastalarda doz ayarlamas� gerekli de�ildir. Masitentan�n �iddetli b�brek yetmezli�i olan PAH hastalar�nda kullan�m�na ili�kin klinik deneyim yoktur. Diyalize giren hastalarda OPSUM�T kullan�m� �nerilmemektedir (bkz. B�l�m 4.4 ve 5.2).
Karaci�er yetmezli�i:
Farmakokinetik verilere dayal� olarak, hafif, orta derece veya �iddetli karaci�er yetmezli�i olan hastalarda doz ayarlamas� gerekli de�ildir (bkz. B�l�m 4.4 ve 5.2). Ancak, masitentan�n orta derece veya �iddetli karaci�er yetmezli�i olan PAH hastalar�nda kullan�m�na ili�kin klinik deneyim yoktur. OPSUM�T �iddetli karaci�er yetmezli�i veya klinik olarak anlaml� �l��de y�ksek hepatik aminotransferaz d�zeyleri (Normalin �st S�n�r�n�n (N�S) 3 kat�ndan fazla (> 3 × N�S); bkz. B�l�m 4.3 ve 4.4) olan hastalarda ba�lat�lmamal�d�r.
Pediyatrik pop�lasyon:
Masitentan�n �ocuklardaki g�venlili�i ve etkilili�i hen�z belirlenmemi�tir. Bu sebeple 18 ya� alt�ndaki �ocuklarda kullan�lmamal�d�r.
Geriyatrik pop�lasyon:
65 ya� �zeri hastalarda doz ayarlamas� gerekli de�ildir (bkz. B�l�m 5.2).
4.3. Kontrendikasyonlar
Etkin madde
4.4. �zel kullan�m uyar�lar� ve �nlemleri
WHO Fonksiyonel S�n�f� (FS) I olan pulmoner arteriyel hipertansiyon hastalar�nda masitentan�n fayda/risk dengesi belirlenmemi�tir.
Karaci�er fonksiyonu
Karaci�er aminotransferazlar�ndaki (AST, ALT) art��lar, PAH ve endotelin resept�r antagonistleri (ERA) ile ili�kilendirilmi�tir. OPSUM�T �iddetli karaci�er yetmezli�i veya artm�� aminotransferaz d�zeyleri (> 3 × N�S) (bkz. B�l�m 4.2 ve 4.3) olan hastalarda ba�lat�lmamal�d�r ve orta derece karaci�er yetmezli�i olan hastalarda �nerilmemektedir. OPSUM�T ba�lat�lmadan �nce karaci�er enzim testleri yap�lmal�d�r.
Hastalar karaci�er hasar� belirtileri a��s�ndan izlenmelidir ve ayl�k ALT ve AST izlenmesi �nerilmektedir. Uzun s�ren, a��klanamayan, klinik olarak ilgili aminotransferaz art��lar� meydana gelirse veya bu art��lar bilirubin d�zeyinde > 2 × N�S art��la veya klinik karaci�er hasar� semptomlar�yla (�r. sar�l�k) birlikte izlenirse OPSUM�T tedavisi sonland�r�lmal�d�r.
Karaci�er hasar�na ili�kin klinik semptomlar� olmayan hastalarda karaci�er enzim d�zeyleri normal aral��a geri d�nd�kten sonra OPSUM�T tedavisinin yeniden ba�lat�lmas� d���n�lebilir. Bir hepatolo�a dan���lmas� �nerilmektedir.
Hemoglobin konsantrasyonu
Di�er ERA'larda oldu�u gibi, masitentan tedavisi de hemoglobin konsantrasyonunda d���� ile ili�kilendirilmi�tir (bkz. B�l�m 4.8). Plasebo kontroll� �al��malarda, hemoglobin konsantrasyonunda masitentana ba�l� d����ler progresif olmay�p, tedavinin ilk 4-12 haftas�ndan sonra stabilize olmu� ve kronik tedavi boyunca stabil kalm��t�r. Masitentan ve di�er ERA'lar ile kan h�cresi transf�zyonu gerektiren anemi vakalar� bildirilmi�tir. �iddetli anemisi olan hastalarda OPSUM�T'in ba�lat�lmas� �nerilmemektedir. Tedavi ba�lat�lmadan �nce hemoglobin konsantrasyonlar�n�n �l��lmesi ve tedavi s�ras�nda klinik olarak endike oldu�unda testlerin tekrarlanmas� �nerilmektedir.
Pulmoner veno-okl�zif hastal�k
Vazodilat�rlerin (a��rl�kl� olarak prostasiklinler) pulmoner veno-okl�zif hastal��� olan hastalarda kullan�lmas� sonucunda pulmoner �dem vakalar� bildirilmi�tir. Sonu� olarak, masitentan PAH hastalar�na uygulan�rken pulmoner �dem belirtileri meydana gelirse pulmoner veno-okl�zif hastal�k olas�l��� de�erlendirilmelidir.
�ocuk do�urma potansiyeli olan kad�nlarda kullan�m
�ocuk do�urma potansiyeli olan kad�nlarda OPSUM�T tedavisi yaln�zca gebelik olmad��� do�ruland�ktan, do�um kontrol�ne ili�kin uygun �neri verildikten ve g�venilir bir do�um kontrol y�ntemi uyguland�ktan sonra ba�lat�lmal�d�r (bkz. B�l�m 4.3 ve 4.6). Kad�nlar, OPSUM�T tedavisi sonland�r�ld�ktan sonra 1 ay boyunca gebe kalmamal�d�r. Gebeli�in erken tespit edilmesi i�in OPSUM�T tedavisi s�ras�nda her ay gebelik testi yap�lmas� �nerilmektedir.
G��l� CYP3A4 ind�kleyicileri ile e� zamanl� kullan�m
G��l� CYP3A4 ind�kleyicilerinin varl���nda masitentan�n etkilili�inde azalma s�z konusu olabilir. Masitentan ile g��l� CYP3A4 ind�kleyicilerinin (�r. rifampisin, sar�
kantaron, karbamazepin ve fenitoin) kombinasyonundan ka��n�lmal�d�r (bkz. B�l�m 4.5). G��l� CYP3A4 inhibit�rleri ile e� zamanl� kullan�m
Masitentan g��l� CYP3A4 inhibit�rleri (�r. itrakonazol, ketokonazol, vorikonazol, klaritromisin, telitromisin, nefazodon, ritonavir ve sakinavir) ile birlikte uyguland���nda dikkatli olunmal�d�r (bkz. B�l�m 4.5).
Orta dereceli ikili veya kombine CYP3A4 ve CYP2C9 inhibit�rleri ile e� zamanl� kullan�m
Masitentan orta dereceli ikili CYP3A4 ve CYP2C9 inhibit�rleri (�r. flukonazol ve amiodaron) ile birlikte uyguland���nda dikkatli olunmal�d�r (bkz. B�l�m 4.5).
Masitentan orta dereceli CYP3A4 inhibit�r� (�r. siprofloksasin, siklosporin, diltiazem, eritromisin, verapamil) ve orta dereceli CYP2C9 inhibit�r� (�r. mikonazol, piperin) ile birlikte uyguland���nda da dikkatli olunmal�d�r (bkz. B�l�m 4.5).
B�brek yetmezli�i olan hastalar
B�brek yetmezli�i olan hastalar�n masitentan tedavisi s�ras�nda hipotansiyon ve anemi ya�ama riski y�ksek olabilir. Bu nedenle, kan bas�nc� ve hemoglobin izlemesi d���n�lmelidir. Masitentan�n �iddetli b�brek yetmezli�i olan PAH hastalar�nda kullan�m�na ili�kin klinik deneyim yoktur. Bu pop�lasyonda dikkatli olunmas� �nerilmektedir. Masitentan�n diyalize giren hastalarda kullan�m�na ili�kin deneyim yoktur, bu nedenle OPSUM�T bu pop�lasyonda �nerilmemektedir (bkz. B�l�m 4.2 ve 5.2).
Yard�mc� maddeler
OPSUM�T tablet laktoz i�erir. Nadir kal�t�msal galaktoz intolerans�, Lapp laktaz yetmezli�i ya da glukoz-galaktoz malabsorpsiyon problemi olan hastalar�n bu ilac� kullanmamalar� gerekir.
OPSUM�T tablet soyadan elde edilen lesitin i�erir. Soyaya a��r� duyarl�l��� olan hastalar OPSUM�T kullanmamal�d�r (bkz. B�l�m 4.3).
4.5. Di�er t�bbi �r�nler ile etkile�imler ve di�er etkile�im �ekilleri
�n vitro �al��malar
Sitokrom P450 CYP3A4 enzimi, CYP2C8, CYP2C9 ve CYP2C19 enzimlerinin min�r katk�s� ile masitentan metabolizmas�nda ve aktif metabolitinin olu�umunda rol oynayan ana enzimdir (bkz. B�l�m 5.2). Masitentan ve aktif metabolitinin sitokrom P450 enzimleri �zerinde klinik olarak ili�kili inhibe edici veya ind�kleyici etkisi yoktur.
Masitentan ve aktif metaboliti, organik anyon ta��y�c� polipeptitler de dahil olmak �zere (OATP1B1 ve OATP1B3), klinik olarak uygulanan konsantrasyonlarda karaci�er veya b�brek al�m ta��y�c�lar�n�n inhibit�rleri de�ildir. Masitentan ve aktif metaboliti, OATP1B1 ve OATP1B3'�n ilgili substratlar� olmamakla birlikte, pasif dif�zyonla karaci�ere girer.
Masitentan ve aktif metaboliti, �oklu ila� direnci proteini (P-gp, MDR-1) ve �oklu ila� ve toksin ekstr�zyon ta��y�c�lar� da (MATE1 ve MATE2-K) dahil olmak �zere, klinik olarak ilgili konsantrasyonlarda karaci�er veya b�brek ak�� pompalar�n�n inhibit�rleri de�ildir. Masitentan, P-gp/MDR-1'in substrat� de�ildir.
Masitentan ve aktif metaboliti, klinik olarak ilgili konsantrasyonlarda, karaci�er safra tuzu transportunda yer alan proteinlerle, yani safra tuzu eksport pompas� (BSEP) ve sodyuma ba�l� taurokolat kotransport polipeptidi (NTCP) ile etkile�ime girmez.
�n vivo �al��malar
Yaln�zca yeti�kinlerde etkile�im �al��malar� ger�ekle�tirilmi�tir.
Flukonazol: PBPK modeline g�re, g�nl�k 400 mg flukonazol (orta dereceli ikili CYP3A4 ve CYP2C9 inhibit�r�) varl���nda masitentana maruziyet yakla��k 3,8 kat artabilir. Ancak masitentan�n aktif metabolitine maruziyette klinik olarak anlaml� de�i�iklik g�zlenmemi�tir. Bu t�r bir modelin belirsizlikleri g�z �n�nde bulundurulmal�d�r. Masitentan orta dereceli ikili CYP3A4 ve CYP2C9 inhibit�rleri (�r. flukonazol ve amiodaron) ile birlikte uyguland���nda dikkatli olunmal�d�r (bkz. B�l�m 4.4).
Masitentan orta dereceli CYP3A4 inhibit�r� (�r. siprofloksasin, siklosporin, diltiazem, eritromisin, verapamil) ve orta dereceli CYP2C9 inhibit�r� (�r. mikonazol, piperin) ile birlikte uyguland���nda da dikkatli olunmal�d�r (bkz. B�l�m 4.4).
Varfarin:
G�nde bir kez 10 mg'l�k �oklu dozlar halinde verilen masitentan�n, 25 mg'l�k tek varfarin dozundan sonra S-varfarin (CYP2C9 substrat�) veya R-varfarine (CYP3A4 substrat�) maruziyet �zerinde etkisi olmam��t�r. Masitentan, varfarinin Uluslararas� Normalize Edilmi� Oran (INR) �zerindeki farmakodinamik etkisini etkilememi�tir. Varfarin, masitentan ve aktif metabolitinin farmakokinetiklerini etkilememi�tir.
Sildenafil:
G�nde bir kez 10 mg masitentan uygulamas� s�ras�nda, kararl� durumda, g�nde �� kez 20 mg sildenafile maruziyet %15 oran�nda artm��t�r. Bir CYP3A4 substrat� olan sildenafil masitentan�n farmakokinetiklerini etkilemezken, masitentan�n aktif metabolitine maruziyette %15 oran�nda azalma meydana gelmi�tir. Bu de�i�iklikler klinik olarak anlaml� kabul edilmemektedir. PAH hastalar�yla yap�lan plasebo kontroll� bir �al��mada, sildenafil ile kombinasyon halinde masitentan�n etkilili�i ve g�venlili�i kan�tlanm��t�r.
Ketokonazol:
G��l� bir CYP3A4 inhibit�r� olan ketokonazolun g�nde bir kez 400 mg dozunda uygulanmas�, masitentana maruziyetini yakla��k 2 kat art�rm��t�r. G�nde iki kez 200 mg ketokonazol uygulamas�nda, fizyolojik tabanl� farmakokinetik (PBPK) modelleme kullan�larak tahmin edilen art�� yakla��k olarak 3 katt�r. Bu modellemedeki belirsizlikler dikkate al�nmal�d�r. Masitentan�n aktif metabolitine maruziyet %26 oran�nda azalm��t�r. Masitentan g��l� CYP3A4 inhibit�rleri ile birlikte uyguland���nda dikkatli olunmal�d�r (bkz. B�l�m 4.4).
Siklosporin A:
Kombine CYP3A4 ve OATP inhibit�r� olan siklosporin A (g�nde iki kez 100 mg) ile e� zamanl� tedavi, masitentan ve aktif metabolitine kararl� durumda maruziyeti klinik olarak anlaml� �l��de de�i�tirmemi�tir.
G��l� CYP3A4 ind�kleyicileri:
G��l� bir CYP3A4 ind�kleyicisi olan rifampisin (g�nde bir kez 600 mg) ile e� zamanl� tedavi, masitentana kararl� durumda maruziyeti %79 oran�nda azalt�rken, aktif metabolite maruziyeti etkilememi�tir. Rifampisin gibi g��l� bir CYP3A4 ind�kleyicisinin varl���nda
masitentan�n etkilili�inin azald��� dikkate al�nmal�d�r. Masitentan ile g��l� CYP3A4 ind�kleyicilerinin kombinasyonundan ka��n�lmal�d�r (bkz. B�l�m 4.4).
Meme kanseri diren� proteini (BCRP) substrat ila�lar�: G�nde bir kez 10 mg masitentan bir BCRP substrat ilac�n�n farmakokineti�ini (1 mg riosiguat; 10 mg rosuvastatin) etkilememi�tir.
Hormonal kontraseptifler: G�nde bir kez 10 mg masitentan oral kontraseptif farmakokineti�ini (1 mg noretisteron ve 35 mikrogram etinil �stradiol) etkilememi�tir.
�zel pop�lasyonlara ili�kin ek bilgiler Pediyatrik pop�lasyon:
Etkile�im �al��malar� yaln�zca yeti�kinlerde ger�ekle�tirilmi�tir.
4.6. Gebelik ve laktasyon
Gebelik kategorisi: X
�ocuk do�urma potansiyeli bulunan kad�nlar/Do�um kontrol� (Kontrasepsiyon)
�ocuk do�urma potansiyeli olan kad�nlarda OPSUM�T tedavisi yaln�zca gebelik olmad��� do�ruland�ktan, do�um kontrol�ne ili�kin uygun �neri verildikten ve g�venilir bir do�um kontrol y�ntemi uyguland�ktan sonra ba�lat�lmal�d�r (bkz. B�l�m 4.3 ve 4.4). Kad�nlar, OPSUM�T tedavisi sonland�r�ld�ktan sonra 1 ay boyunca gebe kalmamal�d�r. Gebeli�in erken tespit edilmesi i�in OPSUM�T tedavisi s�ras�nda her ay gebelik testi yap�lmas� �nerilmektedir.
Gebelik d�nemi
Masitentan�n gebe kad�nlarda kullan�m�na ili�kin veri yoktur. Klinik olmayan verilere g�re, masitentan�n gebelik d�neminde uyguland��� takdirde ciddi do�um kusurlar�na yol a�t���ndan ��phelenilmektedir. Hayvan �al��malar� �reme toksisitesi g�stermi�tir (bkz. B�l�m 5.3). �nsanlara y�nelik potansiyel risk halen bilinmemektedir. OPSUM�T gebelik s�ras�nda ve g�venilir bir do�um kontrol y�ntemi kullanmayan �ocuk do�urma potansiyeli olan kad�nlarda kontrendikedir (bkz. B�l�m 4.3). �ocuk do�urma potansiyeli olan kad�nlar tedavi s�resince (ve tedavinin ard�ndan 1 aya kadar) etkili do�um kontrol� uygulamak zorundad�rlar.
Laktasyon d�nemi
Masitentan�n anne s�t�ne ge�ip ge�medi�i bilinmemektedir. S��anlarda, masitentan ve metabolitleri emzirme s�ras�nda s�te ge�mektedir (bkz. B�l�m 5.3). Emzirilen �ocu�a y�nelik risk g�z ard� edilemez. OPSUM�T emzirme s�ras�nda kontrendikedir (bkz. B�l�m 4.3).
�reme yetene�i/Fertilite
Masitentan tedavisinden sonra erkek hayvanlarda testik�ler t�b�ler atrofi geli�imi g�zlemlenmi�tir (bkz. B�l�m 5.3). ERA alan hastalarda sperm say�s�nda azalmalar g�zlenmi�tir. Masitentan, di�er ERA'lar gibi, erkeklerde spermatogenez �zerinde olumsuz bir etkiye sahip olabilir.
4.7. Ara� ve makine kullan�m� �zerindeki etkiler
Masitentan�n ara� ve makine kullanma yetene�i �zerinde hafif etkisi olabilir. Hastan�n ara� ve makine kullanma yetene�i de�erlendirilirken, hastan�n klinik durumu ve masitentan�n advers reaksiyon profili (ba� a�r�s�, hipotansiyon gibi) g�z �n�nde bulundurulmal�d�r (bkz. B�l�m 4.8).
4.8. �stenmeyen etkiler
G�venlilik profili �zeti
En s�k bildirilen advers ila� reaksiyonlar� nazofarenjit (%14), ba� a�r�s� (%13,6) ve anemidir (%13,2, bkz. B�l�m 4.4). Advers reaksiyonlar�n b�y�k k�sm� hafif ile orta �iddettedir.
Advers reaksiyonlar�n tablo halinde listesi
Masitentan�n g�venlili�i semptomatik PAH'� olan 742 hastay� i�eren uzun s�reli, plasebo kontroll� bir �al��mada de�erlendirilmi�tir (SERAPHIN �al��mas�). Ortalama tedavi s�resi masitentan 10 mg grubunda 103,9 hafta ve plasebo grubunda 85,3 haftad�r. Bu klinik �al��mada masitentan ile ili�kili olarak g�zlemlenen advers reaksiyonlar a�a��daki tabloda verilmektedir. Pazarlama sonras� advers reaksiyonlar da dahil edilmektedir.
A�a��daki terminolojik terimler istenmeyen etkilerin olu�umunu s�n�fland�rmak i�in kullan�lm��t�r:
�ok yayg�n (1/10); yayg�n (1/100 ila <1/10); yayg�n olmayan (1/1.000 ila <1/100); seyrek (1/10.000 ila <1/1.000); �ok seyrek (<1/10.000), bilinmiyor (eldeki verilerden hareketle tahmin edilemiyor).
MedDRA Sistem Organ S�n�flamas� | S�kl�k | Advers reaksiyon |
Enfeksiyonlar ve enfestasyonlar | �ok yayg�n | Nazofarenjit |
�ok yayg�n | Bron�it | |
Yayg�n | Farenjit | |
Yayg�n | Grip | |
Yayg�n | �drar yolu enfeksiyonu | |
Kan ve lenf sistemi hastal�klar� | �ok yayg�n | Anemi, hemoglobin azalmas� |
Yayg�n | L�kopeni | |
Yayg�n | Trombositopeni | |
Ba����kl�k sistemi hastal�klar� | Yayg�n olmayan | A��r� duyarl�l�k reaksiyonlar� (�rn. Anjiyo�dem, ka��nt�, k�zar�kl�k) |
Sinir sistemi hastal�klar� | �ok yayg�n | Ba� a�r�s� |
Vask�ler hastal�klar | Yayg�n | Hipotansiyon, k�zarma |
Solunum, g���s hastal�klar� ve mediastinal hastal�klar | Yayg�n | Nazal konjesyon |
Hepatobiliyer hastal�klar | Yayg�n | Aminotransferaz y�ksekli�i |
Genel bozukluklar ve uygulama b�lgesine ili�kin hastal�klar | �ok yayg�n | �dem, s�v� tutulumu |
Se�ili advers reaksiyonlar�n a��klamas�
Laboratuvar anomalileri
PAH hastalar�yla yap�lan �ift k�r bir �al��mada, > 3 × N�S d�zeyinde aminotransferaz (ALT/AST) art��� insidans� masitentan 10 mg ile %3,4 ve placebo ile %4,5 oran�nda g�zlemlenmi�tir. > 5 x N�S d�zeyindeki art��lar masitentan 10 mg grubundaki hastalar�n
%2,5'inde meydana gelirken, plasebo grubundaki hastalar�n %2'sinde meydana gelmi�tir.
PAH hastalar�yla yap�lan �ift k�r bir �al��mada, masitentan 10 mg plaseboya k�yasla hemoglobinde 1 g/dL'lik ortalama azalma ile ili�kilendirilmi�tir. Masitentan 10 mg ile tedavi edilen hastalar�n %8,7'sinde ve plasebo ile tedavi edilen hastalar�n %3,4'�nde hemoglobin konsantrasyonunda ba�lang�ca g�re 10 g/dL'nin alt�na d��en azalma bildirilmi�tir.
PAH hastalar�yla yap�lan �ift k�r bir �al��mada, masitentan 10 mg ortalama l�kosit say�s�nda ba�lang�ca g�re 0,7 × 10/L'lik azalma ile ili�kilendirilirken, plasebo ile tedavi edilen hastalarda de�i�iklik g�r�lmemi�tir.
PAH hastalar�yla yap�lan �ift k�r bir �al��mada, masitentan 10 mg ortalama trombosit
say�s�nda 17 × 10 /L'lik azalma ile ili�kilendirilirken, plasebo ile tedavi edilen hastalarda
ortalama azalma 11 × 10/L olmu�tur.
Uzun s�reli g�venlilik
Pivot SERAPHIN �ift k�r �al��mas�na kat�lan 742 hastadan 550'si uzun s�reli a��k etiketli (OL) bir uzatma �al��mas�na girmi�tir. (OL kohortu, masitentan 10 mg'a devam eden 182 hastay� ve plasebo veya masitentan 3 mg alan ve masitentan 10 mg'a ge�en 368 hastay� i�ermi�tir.)
Bu 550 hastan�n medyan 3,3 y�ll�k maruziyet ve maksimum 10,9 y�ll�k maruziyet i�in uzun
s�reli takibi, SERAPHIN �ift k�r faz� s�ras�nda yukar�da tarif edildi�i gibi tutarl� bir g�venlilik profili g�stermi�tir.
Pediyatrik pop�lasyon:
Masitentan�n �ocuklarda ve 18 ya��n alt�ndaki ad�lesanlarda g�venlili�i hen�z belirlenmemi�tir.
��pheli advers olaylar�n raporlanmas�
Ruhsatland�rma sonras� ��pheli ila� advers reaksiyonlar�n�n raporlanmas� b�y�k �nem ta��maktad�r. Raporlama yap�lmas�, ilac�n yarar/risk dengesinin s�rekli olarak izlenmesine olanak sa�lar. Sa�l�k mesle�i mensuplar�n�n herhangi bir ��pheli advers reaksiyonu T�rkiye Farmakovijilans Merkezi (T�FAM)'ne bildirmeleri gerekmektedir (www.titck.gov.tr; e- posta: tufam@titck.gov.tr; tel: 0 800 314 00 08; faks; 0 312 218 35 99).
4.9. Doz a��m� ve tedavisi
OPSUM�T, sa�l�kl� g�n�ll�lere 600 mg'a kadar tekli dozlarda uygulanm��t�r. Ba� a�r�s�, mide bulant�s� ve kusmay� i�eren advers reaksiyonlar g�zlemlenmi�tir. A��r� doz durumunda, gerekirse standart destekleyici �nlemler al�nmal�d�r. Masitentan�n y�ksek protein ba�lanma derecesi nedeniyle, diyalizin etkili olma olas�l��� d���kt�r.
5. FARMAKOLOJ�K �ZELL�KLER
5.1. Farmakodinamik �zellikler
Farmakoterap�tikgrup: Di�er antihipertansifler, pulmoner arteriyel hipertansiyon i�in antihipertansifler
ATC kodu: C02KX04
Etki mekanizmas�
Endotelin (ET)-1 ve resept�rleri (ETve ET) vazokonstriksiyon, fibroz, proliferasyon, hipertrofi ve enflamasyon gibi �e�itli etkilere arac�l�k eder. PAH gibi hastal�klarda lokal ET sistemi yukar� reg�le edilir (up-regulation) ve vask�ler hipertrofi ve organ hasar�nda rol oynar.
Masitentan hem EThem de ETresept�r� �zerinde etkin olan oral olarak aktif, g��l� bir endotelin resept�r antagonisti olup, ETi�in ET'ye g�re in vitro yakla��k 100 kat daha se�icidir. Masitentan insan pulmoner arteriyel d�z kas h�crelerinde ET resept�rleri i�in y�ksek afinite ve s�rekli ba�lanma g�sterir. Bu da vazokonstriksiyon ve d�z kas h�cresi proliferasyonuyla sonu�lanan ikinci haberci sistemlerin endotelin arac�l� aktivasyonunu �nler.
Klinik etkililik ve g�venlilik
Pulmoner Arteriyel Hipertansiyonu (PAH) olan hastalarda etkililik
Semptomatik PAH'� olan 742 hastada y�r�t�len �ok merkezli, �ift k�r, plasebo kontroll�, paralel gruplu, olay g�d�ml�, Faz 3 sonu� �al��mas�nda (AC-055-302/SERAPHIN), hastalar morbidite ve mortalite �zerindeki uzun s�reli etkiyi de�erlendirmek �zere �� tedavi grubuna randomize edilmi�tir (plasebo [N = 250], g�nde bir kez 3 mg [N = 250] ve 10 mg [N = 242] masitentan).
Ba�lang��ta, kaydedilen hastalar�n b�y�k k�sm�na (%64), oral fosfodiesteraz inhibit�rleri (%61) ve/veya inhale/oral prostanoidlerle (%6) PAH i�in stabil dozda spesifik bir tedavi uygulanmakta idi.
Primer sonlan�m noktas�, �ift k�r tedavinin sonuna kadar �l�m, atriyal septostomi ya da akci�er nakli, intraven�z (i.v.) ya da subk�tan�z (s.c.) prostanoidlere ba�lanmas� veya ‘di�er PAH k�t�le�mesi' olarak tan�mlanan ilk morbidite veya mortalite olay�n�n olu�umuna kadar ge�en s�re olarak belirlenmi�tir. ‘Di�er PAH k�t�le�mesi' �u �� bile�enin birlikte varl��� olarak tan�mlanm��t�r: 6 dakika y�r�me mesafesinde (6DYM) ba�lang�ca g�re en az %15 oran�nda s�rekli azalma, ve PAH semptomlar�n�n k�t�le�mesi (WHO fonksiyonel s�n�f�n�n veya sa� kalp yetmezli�inin k�t�le�mesi) ve PAH i�in yeni tedavi ihtiyac�. T�m olaylar, tedavi randomizasyonuna k�rle�tirilen ba��ms�z bir karar komitesi taraf�ndan do�rulanm��t�r.
T�m hastalar �al��man�n sonuna kadar hayati durumlar� a��s�ndan takip edilmi�tir. �al��ma sonu, �nceden belirlenen say�da primer sonlan�m noktas� olay�na ula��ld���nda bildirilmi�tir. Tedavi sonu ile �al��ma sonu aras�ndaki d�nemde, hastalar a��k etiketli masitentan 10 mg veya alternatif PAH tedavisi alabilmi�tir. Medyan �ift k�r tedavi s�resi 115 hafta olmu�tur (maksimum 188 hafta masitentan tedavisi).
T�m hastalar�n ortalama ya�� 46 olup (aral�k: 12-85 ya�; 20 hasta 18 ya� alt�, 706 hasta 18-74 aras� ve 16 hasta 75 ya� ve �zeri), g�n�ll�lerin b�y�k k�sm� beyaz �rk (%55) ve kad�nd�r (%77). Hastalar�n yakla��k %52, %46 ve %2'si s�ras�yla WHO fonksiyonel s�n�f II, III ve IV'tedir.
�al��ma pop�lasyonundaki en yayg�n etiyoloji idiyopatik veya kal�tsal PAH olup (%57), takip eden etiyolojiler ba� doku hastal�klar�na ba�l� PAH (%31), d�zeltilmi� basit konjenital kalp hastal��� ile ili�kili PAH (%8) ve di�er etiyolojilerle ili�kili PAH't�r (ila� ve toksinler [%3] ve HIV [%1]).
Sonlan�m noktalar�
Masitentan 10 mg tedavisi, tedavi sonuna kadar kompozit morbidite-mortalite sonlan�m noktas�nda plaseboya g�re %45 oran�nda risk azalmas� sa�lam��t�r (tehlike oran� [HR] 0,55;
%97,5 GA: 0,39 ile 0,76; logrank p < 0,0001) [�ekil 1 ve Tablo 1]. Tedavi etkisi erken ortaya ��km�� ve �al��ma boyunca s�rm��t�r.
Masitentan 10 mg'�n primer sonlan�m noktas� �zerindeki etkilili�i, monoterapi veya ba�ka bir PAH tedavisi ile kombinasyon durumunda, t�m WHO FS gruplar�nda (I/II ve III/IV) ve ya�, cinsiyet, etnik k�ken, co�rafi b�lge, ve etiyoloji alt gruplar� aras�nda tutarl� olmu�tur.
�ekil 1. SERAPHIN'de ilk morbidite-mortalite olay�na ili�kin Kaplan-Meier tahminleri
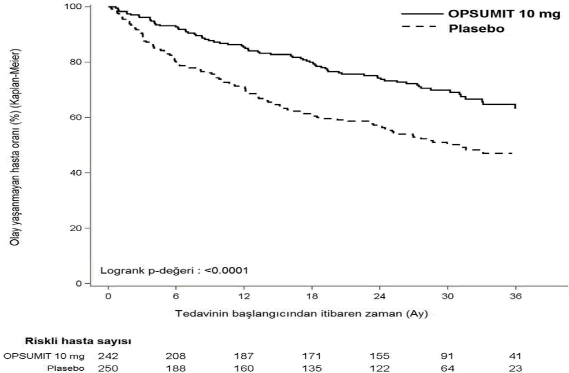
Tablo 1. Sonu� olaylar�n�n �zeti
Sonlan�m | Olay ya�ayan hastalar | Tedavi Kar��la�t�rmas�: Masitentan 10 mg ve Plasebo | ||||
noktas� ve �statistikler |
Plasebo (N = 250) |
Masitentan 10 mg (N = 242) |
Mutlak Risk Azalmas� |
Relatif Risk Azalmas� (%97,5 GA) | HR (%97,5GA) |
Logrank p de�eri |
Morbidite- mortalite olay� |
%53 |
%37 |
%16 | %45 (%24; %61) | 0,55 (0,39; 0,76) |
< 0,0001 |
�l�m n (%) |
19 (%7,6) |
14 (%5,8) |
%2 | %36 (−%42; %71) | 0,64 (0,29; 1,42) |
0,20 |
PAH K�t�le�mesi n (%) | 93 (%37,2) |
59 (%24,4) |
%13 |
%49 (%27, %65) |
0,51 (0,35; 0,73) |
< 0,0001 |
i.v./s.c. Prostanoide Ba�lama n (%) |
6 (%2,4) |
1 (%0,4) |
%2 | |||
�al��ma sonuna kadar t�m nedenlere ba�l� �l�m say�s� masitentan 10 mg grubunda 35 ve plasebo grubunda 44't�r (HR 0,77; %97,5 GA: 0,46 ile 1,28).
Tedavi sonuna kadar PAH'a ba�l� �l�m veya PAH nedeniyle hastaneye yatma riski, masitentan 10 mg (50 olay) alan hastalarda plaseboya g�re (84 olay) %50 oran�nda
azalm��t�r (HR 0,50; %97,5 GA: 0,34 ile 0,75; logrank p < 0,0001). 36 ayda, plasebo alan hastalar�n
%44,6's� ve masitentan 10 mg alan hastalar�n %29,4'� (Mutlak Risk Azalmas� = %15,2) PAH nedeniyle hastaneye yat�r�lm�� veya PAH'a ba�l� bir nedenden �lm��t�r.
Semptomatik sonlan�m noktalar�
Egzersiz kapasitesi sekonder sonlan�m noktas� olarak de�erlendirilmi�tir. Masitentan 10 mg tedavisi 6. ayda 6DYM'de 22 metrelik plaseboya g�re d�zeltilmi� ortalama art�� sa�lam��t�r (%97,5 GA: 3 ile 41; p = 0,0078). 6DYM'nin fonksiyonel s�n�fa g�re de�erlendirmesi, FS III/IV olan hastalarda ba�lang��tan 6. Aya kadar 37 metrelik plaseboya g�re d�zeltilmi� ortalama art��la (%97,5 GA: 5 ile 69) ve FS I/II olan hastalarda 12 metrelik art��la sonu�lanm��t�r (%97,5 GA: -8 ile 33). Masitentan ile elde edilen 6DYM art��� �al��ma s�resince korunmu�tur.
Plaseboya g�re 6. ayda WHO FS iyile�mesi olas�l���, masitentan 10 mg tedavisi ile %74 daha fazla bulunmu�tur (risk oran� 1,74; %97,5 GA: 1,10 ile 2,74; p = 0,0063).
Masitentan 10 mg, SF-36 anketiyle de�erlendirildi�i �zere ya�am kalitesini art�rm��t�r. Hemodinamik sonlan�m noktalar�
Hemodinamik parametreler 6 ayl�k tedaviden sonra bir hasta alt grubunda (plasebo [N = 67], masitentan 10 mg [N = 57]) de�erlendirilmi�tir. Masitentan 10 mg ile tedavi edilen hastalar plaseboya g�re, pulmoner vask�ler diren�te medyan %36,5 (%97,5 GA: %21,7 ile %49,2) azalma ve kardiyak indekste medyan 0,58 L/dk./m (%97,5 GA: 0,28 ile 0,93 L/dk./m) art�� elde etmi�tir.
Uzun s�reli PAH verileri
SERAPHIN �al��mas�n�n �ift k�r (DB) faz�nda masitentan 10 mg ile tedavi edilen ve 182'si a��k etiketli (OL) uzatma �al��mas�nda (SERAPHIN OL) masitentan ile devam eden (DB/OL kohortu) 242 hastan�n uzun s�reli takibinde, 1, 2, 5, 7 ve 9 y�l�n sonunda Kaplan-Meier
sa�kal�m tahminleri s�ras�yla %95, %89, %73, %63 ve %53't�r. Medyan takip s�resi 5,9 y�ld�r.
5.2. Farmakokinetik �zellikler
Genel �zelliklerMasitentan ve aktif metabolitinin farmakokinetikleri a��rl�kl� olarak sa�l�kl� g�n�ll�lerde belgelenmi�tir. PAH hastalar�nda masitentana maruziyet, sa�l�kl� g�n�ll�lere g�re yakla��k 1,2 kat daha y�ksektir. Hastalarda masitentana g�re yakla��k 5 kat daha az g��l� olan aktif metabolite maruziyet sa�l�kl� g�n�ll�lere g�re yakla��k 1,3 kat daha y�ksek olmu�tur. Masitentan�n PAH hastalar�ndaki farmakokinetikleri hastal���n �iddetinden etkilenmemi�tir.
Tekrarl� uygulamadan sonra masitentan farmakokinetikleri 30 mg'a kadar (30 mg dahil)
dozla orant�l�d�r.
Emilim
Masitentan�n maksimum plazma konsantrasyonlar�na uygulamadan yakla��k 8 saat sonra ula��l�r. Ard�ndan, masitentan ve aktif metabolitinin plazma konsantrasyonlar�, s�ras�yla yakla��k 16 saat ve 48 saatlik g�r�n�r eliminasyon yar�lanma �mr� ile, yava� yava� azal�r.
Sa�l�kl� g�n�ll�lerde, masitentan ve aktif metabolitine maruziyet g�da varl���nda de�i�memi�tir, dolay�s�yla masitentan yemekle birlikte veya yemekten ba��ms�z olarak al�nabilir.
Da��l�m
Masitentan ve aktif metaboliti temelde alb�min ve daha d���k �l��de alfa1-asit glikoprotein olmak �zere plazma proteinlerine y�ksek oranda ba�lan�r (> %99). Masitentan ve aktif metaboliti ACT-132577, masitentan ve ACT-132577 i�in s�ras�yla yakla��k 50 L ve 40 L olan g�r�n�r da��l�m hacminden (Vss/F) anla��ld��� �zere dokulara iyi bir �ekilde da��l�r.
Biyotransformasyon
Masitentan�n d�rt primer metabolik yola�� vard�r. S�lfamidin oksidatif depropilasyonu farmakolojik olarak aktif metaboliti verir. Bu reaksiyon, CYP2C8, CYP2C9 ve CYP2C19'un k���k katk�lar�yla birlikte a��rl�kl� olarak CYP3A4 (yakla��k %99) olmak �zere sitokrom P450 sistemine ba�l�d�r. Aktif metabolit insan plazmas�nda dola��ma girer ve farmakolojik etkiye katk�da bulunuyor olabilir. Di�er metabolik yolaklar farmakolojik aktivitesi olmayan �r�nler verir. Bu yolaklar i�in, CYP2C9 bask�n bir rol oynarken, CYP2C8, CYP2C19 ve CYP3A4 min�r katk� sa�lar.
Eliminasyon
Masitentan yaln�zca kapsaml� metabolizmadan sonra at�l�r. Ana at�l�m yolu idrar olup, dozun yakla��k %50'si idrarla at�l�r.
Hastalardaki karakteristik �zellikler:
�zel pop�lasyonlar
Ya�, cinsiyet veya etnik k�kenin masitentan ve aktif metabolitinin farmakokinetikleri �zerinde klinik olarak anlaml� bir etkisi yoktur.
B�brek yetmezli�i
�iddetli b�brek yetmezli�i olan hastalarda masitentan ve aktif metabolitine maruziyet, s�ras�yla, yakla��k 1,3 ve 1,6 kat artm��t�r. Bu art�� klinik olarak anlaml� kabul edilmemektedir (bkz. B�l�m 4.2 ve 4.4).
Karaci�er yetmezli�i
Hafif, orta derece ve �iddetli karaci�er yetmezli�i olan hastalarda masitentana maruziyet s�ras�yla %21, %34 ve %6 oran�nda azal�rken, aktif metabolitine maruziyet s�ras�yla
%20, %25 ve %25 oran�nda azalm��t�r. Bu azalma klinik olarak ilgili kabul edilmemektedir (bkz. B�l�m 4.2 ve 4.4).
5.3. Klinik �ncesi g�venlilik verileri
Masitentan, k�peklerde terap�tik insan maruziyetine benzer maruziyetlerde kan bas�nc�n� d���rm��t�r. 4-39 haftal�k tedaviden sonra insan maruziyetinin 17 kat� olan d�zeylerde koroner arterlerde intimal kal�nla�ma g�zlemlenmi�tir. T�re �zg� hassasiyet ve g�venlik marj�na ba�l� olarak, bu bulgu insanla ilgisiz kabul edilmi�tir.
Fare, s��an ve k�peklerde masitentan tedavisinden sonra karaci�er a��rl���nda art�� ve hepatosel�ler hipertrofi g�zlemlenmi�tir. Bu de�i�iklikler b�y�k oranda tersinir olup, karaci�erin artan metabolik talebe olumsuz olmayan adaptasyonu olarak kabul edilmi�tir.
Masitentan, fare karsinojenisite �al��mas�nda t�m dozlarda nazal kavitenin submukozas�nda minimum ile hafif mukozal hiperplazi ve enflamatuvar infiltrasyona neden olmu�tur. 3 ayl�k fare toksisitesi �al��mas� veya s��an ve k�pek �al��malar�nda hi�bir nazal kavite bulgusu kaydedilmemi�tir.
Masitentan standart in vitro ve in vivo test bataryas�nda genotoksik bulunmam��t�r. Masitentan, insan maruziyetinin 24 kat�na kadar maruziyetlerde tek dozdan sonra in vivo fototoksik bulunmam��t�r. 2 y�l s�ren karsinojenisite �al��malar�, s��an ve farelerde insan maruziyetinin s�ras�yla 18 ve 116 kat� olan maruziyetlerde karsinojenik potansiyel ortaya koymam��t�r.
Erkek s��an ve k�peklerle yap�lan kronik toksisite �al��malar�nda, s�ras�yla 11,6 ve 5,8 g�venlik marj�yla testik�ler t�b�ler dilatasyon g�zlemlenmi�tir. T�b�ler dilatasyon tamamen tersinirdir. S��anlarda 2 y�ll�k tedaviden sonra insan maruziyetinin 4 kat� olan dozlarda testik�ler t�b�ler atrofi g�r�lm��t�r. S��anlarda �m�r boyu s�ren karsinojenisite �al��mas�nda ve k�peklerde tekrarl� doz toksisite �al��mas�nda, s��anlarda 9,7 ve k�peklerde 23 g�venlik marj� veren maruziyetlerde hipospermatogenez g�zlemlenmi�tir. Fertilite i�in g�venlik marjlar� erkek s��anlarda 18 ve di�i s��anlarda 44 olarak belirlenmi�tir. 2 y�la kadar s�ren tedaviden sonra farelerde herhangi bir testik�ler bulgu kaydedilmemi�tir.
Masitentan, tav�an ve s��anlarda test edilen t�m dozlarda teratojenik bulunmu�tur. Her iki t�rde kardiyovask�ler anomaliler ve mandibular ark f�zyon anomalileri tespit edilmi�tir.
Masitentan�n di�i s��anlara ge� gebelik d�neminden emzirme d�nemine kadar insan maruziyetinin 5 kat� olan maternal maruziyetlerde uygulanmas�, yavru sa�kal�m�nda azalmaya ve ge� intrauterin �mr� s�ras�nda ve emzirme d�neminde s�t arac�l���yla masitentana maruz kalan yavrunun �reme kabiliyetinde bozulmaya neden olmu�tur.
Juvenil s��anlara do�um sonras� 4. G�n ile 114. G�n aras�nda uygulanan tedavi, v�cut a��rl��� art���nda azalmaya neden olarak, geli�im �zerinde sekonder etkilere (testis inmesinde hafif gecikme, uzun kemik uzunlu�unda tersinir azalma, uzun s�reli �strus siklusu) yol a�m��t�r. �nsan maruziyetinin 7 kat� olan maruziyetlerde pre-implantasyon ve post-implantasyon kayb�nda hafif art��, ortalama yavru say�s�nda azalma, testis ve epididimis a��rl���nda azalma g�zlemlenmi�tir. Testik�ler t�b�ler atrofi ve �reme de�i�kenleri ile sperm morfolojisi �zerindeki minimum etkiler insan maruziyetinin 3,8 kat� olan maruziyetlerde kaydedilmi�tir.
6. FARMAS�T�K �ZELL�KLER
6.1. Yard�mc� maddelerin listesi
Tablet �ekirde�i
Laktoz monohidrat (s���r kaynakl�) Mikrokristal sel�loz (E460i) Sodyum ni�asta glikolat Tip A Povidon
Magnezyum stearat (E572) Polisorbat 80 (E433)
Film kaplama
Polivinil alkol (E1203) Titanyum dioksit (E171) Talk (E553b)
Lesitin [soya fasulyesi (E322)] Ksantan zamk� (E415)
6.2. Ge�imsizlikler
i
Ge�erli de�ildir.
6.3. Raf �mr�
60 ay
6.4. Saklamaya y�nelik �zel tedbirler
30°C'nin alt�ndaki oda s�cakl���nda saklay�n�z.
6.5. Ambalaj�n niteli�i ve i�eri�i
28 film kapl� tablet i�eren karton kutularda beyaz, opak PVC/PE/PVdC/Al�minyum folyo blister.
6.6. Be�eri t�bbi �r�nden arta kalan maddelerin imhas� ve di�er �zel �nlemler
Kullan�lmam�� olan �r�nler ya da at�k materyaller “T�bbi At�klar�n Kontrol� Y�netmeli�i” ve ‘Ambalaj At�klar�n�n Kontrol� Y�netmelik'lerine uygun olarak imha edilmelidir.
 Kalp Krizi
Kalbe giden kan ak��� durdu�unda kalp krizi meydana gelir.
Kalp Krizi
Kalbe giden kan ak��� durdu�unda kalp krizi meydana gelir. |
 Parkinson Hastal���
Hastal�k ilk kez 1817 de �ngiliz doktor James Parkinson taraf�ndan tan�mlanm�� ve Dr. Parkinson hastal��� “sallay�c� fel�” olarak kaleme alm��.
Parkinson Hastal���
Hastal�k ilk kez 1817 de �ngiliz doktor James Parkinson taraf�ndan tan�mlanm�� ve Dr. Parkinson hastal��� “sallay�c� fel�” olarak kaleme alm��. |
�LA� E�DE�ERLER�
| E�de�er �la� Ad� | Barkodu | �la� Fiyat� |
|---|---|---|
| MASILVA | 8699525099754 | 29,378.64TL |
| MASITERA10 | 8680760092440 | 30,847.65TL |
| OPSENTAN | 8699769090265 | 33,050.83TL |
| OPSUMIT | 8697542090051 | |
| Di�er E�de�er �la�lar |
 |
D�� Gebelik D�� gebelik, her 100 gebelikten birini etkileyen, s�k g�r�len ve �l�me sebep olabilecek bir durumdur. Bu, d�llenen yumurta, rahimin d���na yerle�irse, olu�an bir durumdur. Gebelik ilerledik�e, a�r�ya ve kanamalara sebep olur. |
 |
S�rt A�r�s� S�rt a�r�s� birden bire ortaya ��k�p �iddetli (akut) olabilir veya zamanla geli�ip daha uzun s�reli sorunlara (kronik) neden olabilir. |
 |
A��z Kanseri A��z kanserinin en yayg�n t�rleri, dudak, dil, di�etidir. Nadiren yanak i�i veya damak b�lgelerini de i�ine al�r. |
�LA� GENEL B�LG�LER�
Actelion �la� Tic. Ltd. �ti.
| Geri �deme Kodu | A15804 |
| Sat�� Fiyat� | 18759.43 TL [ 10 Jul 2023 ] |
| �nceki Sat�� Fiyat� | 18418.35 TL [ 3 Jul 2023 ] |
| Original / Jenerik | Original �la� |
| Re�ete Durumu | Normal Re�eteli bir ila�d�r. |
| Barkodu | 8697542090051 |
| Etkin Madde | Masitentan |
| ATC Kodu | C02KX04 |
| Birim Miktar | 10 |
| Birim Cinsi | MG |
| Ambalaj Miktar� | 28 |
| Kalp Damar Sistemi > Di�er Antihipertansifler |
| �thal ( ref. �lke : Isvicre ) ve Be�eri bir ila�d�r. |