OPDIVO 40 mg/4ML IV inf. ��z. kons. i�eren 1 flakon K�sa �r�n Bilgisi
{ Nivolumab }
1. BE�ER� TIBB� �R�N�N ADI
OPDIVO® 40 mg/4 mL IV inf�zyonluk ��zelti konsantresi i�eren flakon Steril
2. KAL�TAT�F VE KANT�TAT�F B�LE��M
Etkin madde
Her 1 mL konsantre 10 mg nivolumab i�erir.
4 mL konsantre i�eren 1 flakon 40 mg nivolumab i�erir.
Nivolumab, rekombinant DNA teknolojisi ile �in hamsteri over h�crelerinde �retilen tamamen insana �zg� bir anti-PD-1 monoklonal antikordur (IgG4).
Yard�mc� maddeler
Sodyum sitrat dihidrat Sodyum klor�r
Sodyum hidroksit (pH ayarlamas� i�in)
Her 1 mL konsantre 0,1 mmol (veya 2,5 mg) sodyum i�erir. Yard�mc� maddeler i�in B�l�m 6.1'e bak�n�z.
3. FARMAS�T�K FORMU
�nf�zyonluk ��zelti konsantresi (steril konsantre)
Az say�da partik�l i�erebilen, berrak ila opak, renksiz ila a��k sar� likittir. ��zeltinin pH de�eri yakla��k 6 ve ozmolaritesi yakla��k 340 mOsm/kg'd�r.
4. KL�N�K �ZELL�KLER
4.1. Terap�tik endikasyonlar
Adjuvan Melanom
OPDIVO, monoterapi olarak tam rezeksiyon uygulanm�� ve lenf d���m� tutulumu olan yeti�kinlerde adjuvan tedavi i�in endikedir. OPDIVO ile tedavi edilmi� hastalar, hastal�k progresyonu halinde PD-1, PDL-1 ve CTLA-4 inhibit�r� kullanamazlar. Tedavi s�resi 12 ay ile s�n�rl�d�r. (bkz. B�l�m 5.1)
Melanom
OPDIVO monoterapi veya ipilimumab ile kombinasyon halinde ECOG performans durumu 0-1 olan yeti�kinlerde ileri evre (rezeke edilemeyen veya metastatik) melanom tedavisinde endikedir.
Renal H�creli Karsinom (RHK)
OPDIVO, berrak h�creli kanser i�eren renal kanserli ileri evre yeti�kin hastalarda endikedir. Hastalar�n karnofsky performans stat�s� en az 70 olmal�d�r. Daha �nce bir veya iki basamak antianjiojenik tedavi ve en fazla 3 basamak sistemik tedavi uygulanm�� olmas� ve hastal�k progresyonu g�r�lm�� olmal�d�r.
OPDIVO, ipilimumab ile kombinasyon halinde IMDC risk kategorisi orta/k�t� riskli, Karnofsky Performans Durumu 70 ve �zerinde olan ve 65 ya� ve alt�ndaki ileri evre renal h�creli karsinomlu yeti�kin hastalar�n birinci basamak tedavisinde endikedir (bkz. B�l�m 5.1).
Klasik Hodgkin Lenfoma (cHL)
OPDIVO, n�ks veya refrakter klasik Hodgkin Lenfoma g�r�len yeti�kin hastalarda; otolog k�k h�cre nakli (OKHN) ve brentuksimab vedotin tedavisinden sonra, veya OKHN de dahil olmak �zere en az 3 basamak sistemik tedavi sonras�nda monoterapi olarak endikedir.
K���k H�creli D��� Akci�er Kanseri (KHDAK)
OPDIVO, ipilimumab ve 2 k�r platin bazl� kemoterapi ile kombinasyon halinde, EGFR mutasyonu veya ALK translokasyonu bulunmayan metastatik k���k h�creli d��� akci�er kanserli ECOG performans skoru 0-1 olan yeti�kin hastalar�n birinci basamak tedavisinde endikedir.
OPDIVO, performans durumu ECOG 0-1 olan, ve bilinen EGFR, ALK, ROS mutasyonu ve/veya semptomatik beyin metastaz� olmayan, lokal ileri/metastatik k���k h�creli d��� akci�er kanseri (KHDAK) olup, daha �nce bir basamak kemoterapi kullan�m�ndan sonra progresyon geli�en hastalar�n tedavisinde, tekrar progresyona kadar kullan�m� endikedir. (Bu hastalar�n tedavisinde tedavi �ncesi veya sonras�nda ba�ka bir PD-1/PD-L1 inhibit�r� kullan�lamaz.)
Malign Plevral Mezotelyoma (MPM)
OPDIVO, ipilimumab ile kombinasyon halinde, rezeke edilemeyen malign plevral mezotelyomas� olan yeti�kin hastalar�n birinci basamak tedavisinde endikedir.
Skuam�z H�creli Ba� ve Boyun Kanseri (SHBBK)
Opere edilemeyen lokal ileri evre kemoradyoterapi sonras� n�ks geli�en veya metastatik ba� boyun (oral kavite, farenks, larenks) yass� epitel h�creli kanserlerde birinci basamak platin temelli kemoterapi sonras� ilk 6 ay i�erisinde n�ks geli�en hastalar�n tedavisinde progresyona kadar kullan�m� uygundur.
Mikrosatellit �nstabilitesi Y�ksek (MSI-H) veya Uyumsuzluk Onar�m Eksikli�i (dMMR) olan Metastatik Kolorektal Kanser (mKRK)
Nivolumab, monoterapi olarak, bir fluoropirimidin, oksaliplatin ve irinotekan ile tedaviyi takiben progresyon g�steren mikrosatellit instabilitesi y�ksek (MSI-H) ya da uyumsuzluk onar�m eksikli�i (dMMR) olan metastatik kolorektal kanseri (mKRK) olan yeti�kin hastalar�n tedavisinde endikedir.
�zofagus Skuam�z H�creli Karsinom (�SHK)
OPDIVO, metastatik veya k�ratif tedaviye uygun olmayan lokal ileri �zofagus skuam�z h�creli karsinomu bulunan yeti�kin hastalar�n tedavisinde floropirimidin ve platin bazl� kombinasyon kemoterapisine progresyon geli�en hastalarda monoterapi olarak endikedir.
�zofagus Kanseri (�K) veya Gastro�zofageal Bile�ke Kanserinin (GEJC=GBK) Adjuvan Tedavisi
OPDIVO monoterapi olarak, �nceki neoadjuvan kemoradyoterapi ve k�ratif cerrahi tedavileri sonras�nda patolojik rezid�el hastal��� bulunan �zofagus veya gastro�zofageal bile�ke kanseri olan yeti�kin hastalar�n adjuvan tedavisinde n�kse kadar veya maksimum 1 y�l s�reyle endikedir. (bkz. B�l�m 5.1).
Mide Adenokanseri (MK), Gastro�zofageal Bile�ke (GEJ=GBK) Kanseri veya �zofagus Adenokarsinom (�AK)
OPDIVO, fluoropirimidin ve platin i�eren kemoterapi rejimi ile kombinasyon halinde, PD-L1 kombine pozitif skoru (CPS) ≥ 5 olup, HER2-negatif, ECOG 0-1, rezeke edilemeyen ileri evre/metastatik mide kanseri, gastro�zofageal bile�ke kanseri veya �zofagus adenokarsinomu olan yeti�kin hastalar�n birinci basamak tedavisi i�in endikedir. Hastalar e�er neoadjuvan/adjuvan tedavi ald�larsa en az 6 ayl�k hastal�ks�z s�re ge�mi� olmal�d�r.
4.2. Pozoloji ve uygulama �ekli
Tedavi, kanser tedavisinde deneyimli uzman doktorlar taraf�ndan ba�lat�lmal� ve kontrol edilmelidir.
PD-L1 testi
E�er endikasyonda belirtilmi�se, OPDIVO tedavisi i�in hasta se�imi PD-L1'in t�m�r ekspresyonuna dayal� olarak, valide edilmi� bir testle do�rulanmal�d�r (bkz. B�l�m 4.1, 4.4 ve 5.1).
Pozoloji/uygulama s�kl��� ve s�resi
OPDIVO'nun monoterapi olarak �nerilen dozu 2 haftada bir 60 dakikal�k intraven�z inf�zyonla verilen 3 mg/kg'dir. Tedavi, klinik yarar g�zlendi�i s�rece veya tedavi hasta taraf�ndan art�k tolere edilemeyinceye kadar s�rd�r�lmelidir.
MSI-H/dMMR mKRK i�in, monoterapi olarak �nerilen OPDIVO dozu, hastal�k progresyonu veya kabul edilemez toksisiteye kadar 30 dakika s�reyle intraven�z inf�zyon olarak 2 haftada bir uygulanan 240 mg'd�r.
�zofagus Skuam�z H�creli Karsinom (�SHK) i�in, monoterapi olarak �nerilen OPDIVO dozu, 2 haftada bir 30 dakika s�reyle intraven�z inf�zyon olarak uygulanan 240 mg veya 2 haftada bir 60 dakikal�k intraven�z inf�zyon olarak uygulanan 3 mg/kg'dir.
Adjuvan tedavi i�in OPDIVO ile tedavi s�resi maksimum 12 ayd�r.
�pilimumab ile kombinasyon halinde OPDIVO Melanom
�nerilen doz, ilk 4 doz i�in 3 haftada bir intraven�z yoldan uygulanan 3 mg/kg ipilimumab ile kombinasyon halinde 1 mg/kg nivolumab �eklindedir. Tablo 1'de g�sterildi�i �zere, bunu, her 2 haftada bir 240 mg veya her 4 haftada bir 480 mg dozda intraven�z yoldan uygulanan nivolumab monoterapisi faz� takip eder. Monoterapi faz�nda, ilk nivolumab dozu a�a��da g�sterilen �ekillerde uygulanmal�d�r;
Her iki haftada bir 240 mg uygulan�yor ise, nivolumab ve ipilimumab kombinasyonunun son dozundan 3 hafta sonra ya da
4.3. Kontrendikasyonlar
Etkin madde
OPDIVO 18 ya��n alt�ndaki hastalarda kullan�lmamal�d�r.
4.4. �zel kullan�m uyar�lar� ve �nlemleri
PD-L1 durumunun de�erlendirilmesi
T�m�r�n PD-L1 durumunu de�erlendirirken, iyi valide edilmi� ve g��l� bir metodolojinin kullan�lmas� �nemlidir.
Imm�n ili�kili advers reaksiyonlar
Nivolumab kombinasyon halinde uyguland���nda, tedavinin ba�lang�c�ndan �nce di�er kombinasyon tedavisi bile�enlerinin K�sa �r�n Bilgisi'ne bak�n�z. �mm�n ili�kili advers reaksiyonlar, monoterapi olarak nivolumaba k�yasla ipilimumab ile kombinasyon halinde nivolumab tedavisi ile daha fazla meydana gelmi�tir. �mm�n ili�kili advers reaksiyonlar�n bir�o�u kortikosteroid tedavisinin ba�lat�lmas� ve tedavi de�i�iklikleri dahil olmak �zere uygun y�netim ad�mlar� ile iyile�mi� ya da ��z�lm��t�r (bkz. B�l�m 4.2).
V�cutta birden fazla sistemi etkileyen ba����kl�kla ilgili advers reaksiyonlar ayn� anda meydana gelebilir.
Kombinasyon tedavisinde pulmoner emboli dahil olmak �zere kardiyak ve pulmoner advers olaylar da bildirilmi�tir. Hastalar tedavi �ncesinde ve tedavi s�ras�nda periyodik olarak elektrolit bozukluklar�n�n ve dehidratasyonun g�stergesi olan klinik bulgular, semptomlar ve laboratuvar anormalliklerinin yan� s�ra, kardiyak ve pulmoner advers reaksiyonlar i�in s�rekli izlenmelidir. �pilimumab ile kombinasyon halinde nivolumab uygulamas� ya�am� tehdit eden ya da tekrarlayan �iddetli kardiyak ve pulmoner advers reaksiyonlar�n meydana gelmesi halinde kesilmelidir (bkz. B�l�m 4.2).
Nivolumab, imm�n ili�kili advers reaksiyonlarla ili�kilendirilmi�tir.
Nivolumab tedavisi s�ras�nda veya tedaviden sonraki herhangi bir zamanda bir advers reaksiyon meydana gelebilece�inden, hastalar s�rekli olarak izlenmelidir (son dozu takiben en az 5 ay).
��pheli imm�n ili�kili advers reaksiyonlar i�in, etiyolojiyi do�rulamak veya di�er nedenleri d��lamak i�in uygun de�erlendirmeler yap�lmal�d�r. Advers reaksiyonun �iddetine dayanarak, nivolumab tedavisi kesilmeli ve kortikosteroidler uygulanmal�d�r. Bir advers reaksiyon nedeniyle uygulanan kortikosteroid, iyile�me sonras�nda en az 1 ayl�k s�rede azalt�larak kesilmelidir. Dozun k�sa s�rede kesilmesi advers reaksiyonun k�t�le�mesine veya tekrarlamas�na yol a�abilir. Kortikosteroid kullan�m�na ra�men k�t�le�me g�r�len veya iyile�me g�r�lmeyen hastalarda kortikosteroid d���nda bir imm�nosupresif tedavi eklenmelidir.
Hasta, imm�nosupresif kortikosteroid dozlar�n� ya da di�er imm�nos�presif tedavileri al�rken nivolumab monoterapisi veya ipilimumab ile kombinasyon halinde nivolumab tedavisi yeniden ba�lat�lmamal�d�r. �mm�nos�presif tedavi alan hastalarda f�rsat�� enfeksiyonlar�n �nlenmesi i�in profilaktif antibiyotikler kullan�lmal�d�r.
Herhangi bir �iddette imm�n ili�kili advers reaksiyonun tekrarlamas� veya ya�am� tehdit eden herhangi bir imm�n ili�kili reaksiyon g�r�lmesi durumunda, nivolumab monoterapisi veya ipilimumab ile kombinasyon halinde nivolumab tedavisi kal�c� olarak kesilmelidir.
�mm�n ili�kili pn�monit
Nivolumab monoterapisi veya ipilimumab ile kombinasyon halinde nivolumab tedavisi s�ras�nda �iddetli pn�monit veya �l�mc�l vakalar dahil olmak �zere interstisyel akci�er hastal��� g�zlenmi�tir (bkz. B�l�m 4.8). Hastalar radyografik de�i�iklikler (�rn., fokal buzlu cam opasiteleri ve yama tarz�nda filtratlar), dispne ve hipoksi gibi pn�monit i�aretleri ve semptomlar� a��s�ndan izlenmelidir. Enfeksiy�z ve hastal�kla ili�kili etiyolojiler d��lanmal�d�r.
Derece 3 veya 4 pn�monit i�in nivolumab monoterapisi veya ipilimumab ile kombinasyon halinde nivolumab tedavisi kal�c� olarak kesilmeli ve 2 ila 4 mg/kg/g�n metilprednizolon e�de�eri dozda kortikosteroid tedavisine ba�lanmal�d�r.
Derece 2 (semptomatik) pn�monit i�in, nivolumab monoterapisi veya ipilimumab ile kombinasyon halinde nivolumab tedavisine ara verilmeli ve 1 mg/kg/g�n metilprednizolon e�de�eri kortikosteroid tedavisine ba�lanmal�d�r. �yile�meden sonra, kortikosteroid tedavisinin kademeli olarak kesilmesini takiben nivolumab tedavisi yeniden ba�lat�labilir. Kortikosteroid tedavisine ba�lanmas�na ra�men k�t�le�me olursa veya iyile�me g�r�lmezse kortikosteroid dozu 2 ila 4 mg/kg/g�n metilprednizolon e�de�erine y�kseltilmeli ve nivolumab monoterapisi veya ipilimumab ile kombinasyon halinde nivolumab tedavisi kal�c� olarak kesilmelidir.
�mm�n ili�kili kolit
Nivolumab monoterapisi veya ipilimumab ile kombinasyon halinde nivolumab tedavisi ile �iddetli diyare ya da kolit g�zlenmi�tir (bkz. B�l�m 4.8). Hastalar diyare ya da kar�n a�r�s� ve d��k�da mukus veya kan gibi ilave kolit semptomlar� i�in izlenmelidir. Kortikosteroide yan�ts�z imm�n ili�kili kolit hastalar�nda sitomegalovir�s (CMV) enfeksiyonu/reaktivasyonu bildirilmi�tir. Enfeksiy�z ve hastal�kla ili�kili etiyolojiler d��lanmal�d�r, Bu nedenle uygun laboratuvar testleri ve ek incelemeler yap�lmal�d�r. E�er kortikosteroide yan�ts�z imm�n ili�kili kolit tan�s� do�rulanm��sa kortikosteroid tedavisine alternatif bir imm�nos�presif ila� eklenmesi ya da kortikosteroid tedavinin de�i�tirilmesi d���n�lmelidir.
Derece 4 diyare ya da kolit i�in, nivolumab monoterapisi veya ipilimumab ile kombinasyon halinde nivolumab tedavisi kal�c� olarak kesilmeli ve 1 ila 2 mg/kg/g�n metilprednizolon e�de�eri dozda kortikosteroid tedavisine ba�lanmal�d�r.
Derece 3 diyare ya da kolit i�in nivolumab monoterapi tedavisine ara verilmeli ve 1 ila 2 mg/kg/g�n metilprednizolon e�de�eri dozda kortikosteroid tedavisine ba�lanmal�d�r. �yile�meden sonra, kortikosteroid dozunun kademeli olarak kesilmesini takiben nivolumab tedavisi yeniden ba�lat�labilir. Kortikosteroid tedavisine ba�lanmas�na ra�men k�t�le�me olursa veya iyile�me g�r�lmezse, nivolumab monoterapi tedavisi kal�c� olarak kesilmelidir. Nivolumab monoterapisi ya da ipilimumab ile kombinasyon halinde nivolumab tedavisinde, tedavinin kal�c� olarak kesilmesini ve 1 ila 2 mg/kg/g�n metilprednizolon e�de�eri dozlarda kortikosteroidlerin ba�lat�lmas�n� gerektiren Derece 3 diyare ya da kolit g�zlemlenmi�tir.
Derece 2 diyare ya da kolit i�in, nivolumab monoterapisi veya ipilimumab ile kombinasyon halinde nivolumab tedavisine ara verilmelidir. Persistan diyare veya kolit i�in, 0,5 ila 1 mg/kg/g�n metilprednizolon e�de�eri dozda kortikosteroid tedavisi kullan�lmal�d�r. �yile�meden sonra, kortikosteroid tedavisinin kademeli olarak kesilmesini takiben gerekirse nivolumab monoterapisi veya ipilimumab ile kombinasyon halinde nivolumab tedavisi yeniden ba�lat�labilir. Kortikosteroid tedavisine ba�lanmas�na ra�men k�t�le�me olursa veya iyile�me g�r�lmezse kortikosteroid dozu 1 ila 2 mg/kg/g�n metilprednizolon e�de�erine y�kseltilmeli ve nivolumab monoterapisi veya ipilimumab ile kombinasyon halinde nivolumab tedavisi kal�c� olarak kesilmelidir.
�mm�n ili�kili hepatit
Nivolumab monoterapisi veya ipilimumab ile kombinasyon halinde nivolumab tedavisi ile �iddetli hepatit g�zlenmi�tir (bkz. B�l�m 4.8). Hastalar, transaminaz ve toplam bilirubin d�zeylerinde y�kselme gibi hepatit belirti ve semptomlar� i�in izlenmelidir. Enfeksiy�z ve hastal�kla ili�kili etiyolojiler d��lanmal�d�r.
Transaminaz ve toplam bilirubin d�zeylerinde Derece 3 veya 4 art�� durumunda, nivolumab monoterapisi veya ipilimumab ile kombinasyon halinde nivolumab tedavisi kal�c� olarak kesilmeli ve 1 ila 2 mg/kg/g�n metilprednizolon e�de�eri dozda kortikosteroid tedavisine ba�lanmal�d�r.
Derece 2 transaminaz veya toplam bilirubin art��� durumunda, nivolumab monoterapisi veya ipilimumab ile kombinasyon halinde nivolumab tedavisine ara verilmelidir. Bu laboratuvar de�erlerinde persistan art�� i�in, 0,5 ila 1 mg/kg/g�n metilprednizolon e�de�eri dozda kortikosteroid tedavisi kullan�lmal�d�r. �yile�meden sonra, kortikosteroid dozunun kademeli olarak kesilmesini takiben gerekirse nivolumab monoterapisi veya ipilimumab ile kombinasyon halinde nivolumab tedavisi yeniden ba�lat�labilir. Kortikosteroid tedavisine ba�lanmas�na ra�men k�t�le�me olursa veya iyile�me g�r�lmezse kortikosteroid dozu 1 ila 2 mg/kg/g�n metilprednizolon e�de�erine y�kseltilmeli ve nivolumab monoterapisi veya ipilimumab ile kombinasyon halinde nivolumab tedavisi kal�c� olarak kesilmelidir.
�mm�n ili�kili nefrit ve renal fonksiyon bozuklu�u
Nivolumab monoterapisi veya ipilimumab ile kombinasyon halinde nivolumab tedavisi ile �iddetli nefrit veya b�brek fonksiyon bozuklu�u g�zlenmi�tir (bkz. B�l�m 4.8). Hastalar, nefrit ve b�brek fonksiyon bozuklu�u belirti ve semptomlar� i�in izlenmelidir. Hastalar�n �o�unda herhangi bir semptom olmadan serum kreatininde art�� g�zlenmi�tir. Hastal�kla ili�kili etiyolojiler d��lanmal�d�r.
Derece 4 serum kreatinin art��lar� i�in, nivolumab monoterapisi veya ipilimumab ile kombinasyon halinde nivolumab tedavisi kal�c� olarak kesilmeli ve 1 ila 2 mg/kg/g�n metilprednizolon e�de�eri dozunda kortikosteroid tedavisine ba�lanmal�d�r.
Derece 2 veya 3 serum kreatinin art��� i�in, nivolumab monoterapisi veya ipilimumab ile kombinasyon halinde nivolumab tedavisine ara verilmeli ve 0,5 ila 1 mg/kg/g�n metilprednizolon e�de�eri dozda kortikosteroid tedavisine ba�lanmal�d�r. �yile�meden sonra, kortikosteroid dozunun kademeli olarak kesilmesini takiben nivolumab monoterapisi veya ipilimumab ile kombinasyon halinde nivolumab tedavisi yeniden ba�lat�labilir. Kortikosteroid tedavisine ba�lanmas�na ra�men k�t�le�me olursa veya iyile�me g�r�lmezse kortikosteroid dozu 1 ila 2 mg/kg/g�n metilprednizolon e�de�erine y�kseltilmeli ve nivolumab monoterapisi veya ipilimumab ile kombinasyon halinde nivolumab tedavisi kal�c� olarak kesilmelidir.
�mm�n ili�kili endokrinopatiler
Nivolumab monoterapisi veya ipilimumab ile kombinasyon halinde nivolumab tedavisi ile hipotiroidizm, hipertiroidizm, adrenal yetmezlik (sekonder adrenokortikal yetmezlik dahil), hipofizit (hipopit�itarizm dahil), diabetes mellitus ve diyabetik ketoasidoz dahil �iddetli endokrinopatiler g�zlenmi�tir (bkz. B�l�m 4.8).
Hastalar endokrinopatilerin klinik belirti ve semptomlar�, hiperglisemi ve tiroid fonksiyonundaki de�i�iklikler a��s�ndan dikkatli �ekilde izlenmelidir (tedavinin ba��nda, tedavi s�ras�nda periyodik olarak ve klinik de�erlendirmeye dayanarak gerekli oldu�unda). Hastalarda yorgunluk, ba� a�r�s�, mental durum de�i�iklikleri, kar�n a�r�s�, ola�and��� ba��rsak al��kanl�klar� ve hipotansiyon veya beyin metastazlar� ya da altta yatan hastal�k gibi di�er nedenlere benzeyen, spesifik olmayan semptomlar g�r�lebilir. Alternatif etiyoloji belirlenene dek, endokrinopati belirti ve semptomlar�n�n imm�n ili�kili oldu�u kabul edilmelidir.
Semptomatik hipotiroidizm i�in, nivolumab monoterapisi veya ipilimumab ile kombinasyon halinde nivolumab tedavisine ara verilmeli ve gerekti�i �ekilde tiroid hormon replasman�na ba�lanmal�d�r. Semptomatik hipertiroidizm i�in, nivolumab monoterapisi veya ipilimumab ile kombinasyon halinde nivolumab tedavisine ara verilmeli ve gerekti�i �ekilde antitiroid ila� tedavisine ba�lanmal�d�r. Akut tiroid enflamasyonundan ��pheleniliyorsa, 1 ila 2 mg/kg/g�n metilprednizolon e�de�eri dozda kortikosteroid tedavisine ba�lanmal�d�r. �yile�meden sonra, kortikosteroid dozunun kademeli olarak kesilmesini takiben gerekirse nivolumab monoterapisi veya ipilimumab ile kombinasyon halinde nivolumab tedavisi yeniden
ba�lat�labilir. Uygun hormon replasman�n�n kullan�ld���ndan emin olmak i�in tiroid fonksiyonu s�rekli �ekilde izlenmelidir.Ya�am� tehdit eden hipertiroidizm veya hipotiroidizm durumunda nivolumab monoterapisi veya ipilimumab ile kombinasyon halinde nivolumab tedavisine kal�c� olarak son verilmelidir.
Semptomatik Derece 2 adrenal yetmezlik i�in, nivolumab monoterapisi veya ipilimumab ile kombinasyon halinde nivolumab tedavisine ara verilmeli ve gerekti�i �ekilde fizyolojik kortikosteroid replasman�na ba�lanmal�d�r. Ciddi (Derece 3) veya ya�am� tehdit eden (Derece 4) adrenal yetmezlik durumunda, nivolumab monoterapisi veya ipilimumab ile kombinasyon halinde nivolumab tedavisi kal�c� olarak kesilmelidir. Uygun kortikosteroid replasman�n�n kullan�ld���ndan emin olmak i�in adrenal fonksiyon ve hormon d�zeyleri s�rekli �ekilde izlenmelidir.
Semptomatik Derece 2 veya 3 hipofizit i�in, nivolumab monoterapisi veya ipilimumab ile kombinasyon halinde nivolumab tedavisine ara verilmeli ve gerekti�i �ekilde hormon replasman�na ba�lanmal�d�r. Akut hipofiz bezi enflamasyonundan ��pheleniliyorsa, 1 ila 2 mg/kg/g�n metilprednizolon e�de�eri dozda kortikosteroid tedavisine ba�lanmal�d�r. �yile�meden sonra, kortikosteroid dozunun kademeli olarak kesilmesini takiben gerekirse nivolumab monoterapisi veya ipilimumab ile kombinasyon halinde nivolumab tedavisi yeniden ba�lat�labilir. Ya�am� tehdit eden (Derece 4) hipofizit durumunda, nivolumab monoterapisi veya ipilimumab ile kombinasyon halinde nivolumab tedavisi kal�c� olarak kesilmelidir. Uygun hormon replasman�n�n kullan�ld���ndan emin olmak i�in hipofiz fonksiyonu ve hormon d�zeyleri s�rekli �ekilde izlenmelidir.
Semptomatik diyabet i�in, nivolumab monoterapisi veya ipilimumab ile kombinasyon halinde nivolumab tedavisine ara verilmeli ve gerekti�i �ekilde ins�lin replasman�na ba�lanmal�d�r. Uygun ins�lin replasman�n�n kullan�ld���ndan emin olmak i�in kan �ekeri s�rekli �ekilde izlenmelidir. Ya�am� tehdit eden diyabet durumunda, nivolumab monoterapisi veya ipilimumab ile kombinasyon halinde nivolumab tedavisi kal�c� olarak kesilmelidir.
�mm�n ili�kili deri advers reaksiyonlar�
�pilimumab ile kombinasyon halinde nivolumab tedavisi ile ve daha seyrek olarak nivolumab monoterapisi ile imm�n ili�kili olabilen �iddetli d�k�nt� g�zlenmi�tir (bkz. B�l�m 4.8). Derece 3 d�k�nt� g�r�l�rse OPDIVO dozuna ara verilmeli, Derece 4 d�k�nt�de nivolumab monoterapisi veya ipilimumab ile kombinasyon halinde nivolumab kesilmelidir. �iddetli d�k�nt� i�in, 1 ila 2 mg/kg/g�n metilprednizolon e�de�eri dozda y�ksek doz kortikosteroid tedavisi kullan�lmal�d�r.
Baz�lar� fatal sonu� g�steren seyrek SJS ve TEN olgular� g�zlenmi�tir. SJS veya TEN belirti veya bulgular� geli�irse, nivolumab monoterapisi veya ipilimumab ile kombinasyon halinde nivolumab tedavisi kesilmelidir ve hasta de�erlendirme ve tedavi i�in uzman bir �niteye y�nlendirilmelidir. Hastada nivolumab monoterapisi veya ipilimumab ile kombinasyon halinde nivolumab kullan�m�na ba�l� SJS veya TEN geli�mi�se, nivolumab�n kal�c� olarak kesilmesi �nerilir. (bkz. B�l�m 4.2)
Di�er imm�n stim�lat�r antikanser ila�lar� ile �nceki tedavi s�ras�nda ciddi veya ya�am� tehdit eden advers cilt reaksiyonlar� ya�ayan bir hastada nivolumab kullan�lmas� d���n�l�rken dikkatli olunmal�d�r.
Di�er imm�n ili�kili advers reaksiyonlar
A�a��daki imm�n ili�kili advers reaksiyonlar �e�itli dozlarda ve t�m�r tiplerinde yap�lan klinik �al��malarda nivolumab monoterapisi veya ipilimumab ile kombinasyon halinde nivolumab ile tedavi edilen hastalar�n %1'inden az�nda bildirilmi�tir: pankreatit, �veit,
demiyelinasyon, otoimm�n n�ropati (fasiyal ve abdusens sinir parezisi dahil), Guillain-Barré sendromu, miyastenia gravis, miyastenik sendrom, aseptik menenjit, ensefalit, gastrit, sarkoidoz, duodenit, miyozit, miyokardit ve rabdomiyoliz. Pazarlama sonras�nda Vogt- Koyanagi-Harada sendromu, hipoparatiroidizm ve infektif olmayan sistit vakalar� bildirilmi�tir (bkz. B�l�m 4.2 ve 4.8).
��pheli imm�n ili�kili advers reaksiyonlar i�in etiyolojiyi do�rulamak veya di�er nedenleri d��lamak i�in uygun de�erlendirmeler yap�lmal�d�r. Advers reaksiyonun �iddetine dayanarak, nivolumab monoterapisi veya ipilimumab ile kombinasyon halinde nivolumab tedavisi kesilmeli ve kortikosteroidler uygulanmal�d�r. �yile�meden sonra, kortikosteroid dozunun kademeli olarak kesilmesini takiben nivolumab monoterapisi veya ipilimumab ile kombinasyon halinde nivolumab tedavisi yeniden ba�lat�labilir. Herhangi bir �iddetli imm�n ili�kili advers reaksiyonun tekrarlamas� veya ya�am� tehdit eden herhangi bir imm�n ili�kili reaksiyon g�r�lmesi durumunda nivolumab monoterapisi veya ipilimumab ile kombinasyon halinde nivolumab tedavisi kal�c� olarak kesilmelidir.
Nivolumab monoterapisi veya ipilimumab ile kombinasyon halinde nivolumab ile baz�lar� �l�mc�l olan nadir miyotoksisite (miyozit, miyokardit ve rabdomiyoliz) vakalar� bildirilmi�tir. Bir hastada miyotoksisite belirtileri ve semptomlar� geli�ti�i takdirde yak�n takip uygulanmal�d�r ve hasta gecikmeden de�erlendirme ve tedavi uygulanmas� i�in bir uzmana sevk edilmelidir. Miyotoksisitenin �iddetine ba�l� olarak, nivolumab monoterapisi veya ipilimumab ile kombinasyon halinde nivolumab tedavisi duraklat�lmal� veya kesilmelidir (bkz. B�l�m 4.2) ve uygun tedavi ba�lat�lmal�d�r.
Miyokardit tan�s�n�n konulabilmesi i�in kuvvetli ��phe gerekir. Kardiyak ya da kardiyopulmoner semptomlar� olan hastalar miyokardit olas�l��� a��s�ndan de�erlendirilmelidir. E�er miyokardit ��phesi varsa derhal y�ksek doz steroid ba�lanmal� (prednizon 1 - 2 mg/kg/g�n ya da metilprednizolon 1-2 mg/kg/g�n) ve derhal kardiyoloji kons�ltasyonu istenerek g�ncel klinik rehberlere g�re tan�sal testlere ba�lanmal�d�r. Miyokardit tan�s� konulmas�n� takiben nivolumab ile tedavi kesilmeli ya da tamamen b�rak�lmal�d�r (bkz. B�l�m 4.2).
Pazarlama sonras� PD-1 inhibit�rleriyle tedavi uygulanan hastalarda solid organ nakli reddi bildirilmi�tir. Solid organ nakli uygulanan ki�ilerde nivolumab tedavisi red riskini artt�rabilir. Bu hastalarda nivolumabla uygulanan tedavinin olas� organ transplantasyonu sonras�nda organ reddi riski kar��s�ndaki faydas� de�erlendirilmelidir.
Monoterapi olarak uygulanan nivolumab ve ipilimumabla kombinasyon halinde kullan�lan nivolumabla birlikte hemofagositik lenfohistiyositoz (HLH) g�zlenmi�tir. Nivolumab monoterapi olarak veya ipilimumabla kombinasyon halinde uygulan�rken dikkatli olunmal�d�r. HLH do�ruland��� takdirde nivolumab veya ipilimumabla kombinasyon halinde nivolumab uygulamas� durdurulmal�d�r ve HLH tedavisi ba�lat�lmal�d�r.
�nf�zyon reaksiyonlar�
Nivolumab veya ipilimumab ile kombinasyon halinde nivolumab ile yap�lan klinik �al��malarda ciddi veya ya�am� tehdit eden inf�zyon reaksiyonlar� bildirilmi�tir (bkz. B�l�m 4.8). Ciddi ya da ya�am� tehdit edici inf�zyon reaksiyonu durumunda, nivolumab monoterapisi veya ipilimumab ile kombinasyon halinde nivolumab inf�zyonu sonland�r�lmal� ve uygun t�bbi tedavi uygulanmal�d�r. Hafif veya orta �iddetli inf�zyon reaksiyonlar� g�r�len hastalara nivolumab monoterapisi veya ipilimumab ile kombinasyon halinde nivolumab yak�n g�zetim alt�nda ve inf�zyon reaksiyonlar�n�n profilaksisine y�nelik yerel tedavi k�lavuzlar� uyar�nca bir �n ila� kullan�larak uygulanabilir.
�zel pop�lasyonlar
Melanom
�lerlemi� melanom
Ba�lang�� performans skoru ≥ 2 olan, aktif beyin metastazlar� veya otoimm�n hastal�k g�r�len hastalar ve �al��maya girmeden �nce sistemik imm�nosupresif alan hastalar nivolumab monoterapisi veya ipilimumab ile kombinasyon halinde nivolumab klinik �al��malar�na al�nmam��t�r. Ok�ler/�veal melanomu olan hastalar melanom klinik �al��mas�na dahil edilmemi�tir. Ayr�ca, CA209037 �al��mas�na, anti-CTLA-4 tedavisi ile ili�kili Derece 4 advers reaksiyon ya�am�� olan hastalar dahil edilmemi�tir (bkz. B�l�m 5.1). Yeterli veri bulunmad���ndan, nivolumab, hastaya �zg� dikkatli bir yarar-risk de�erlendirmesinin ard�ndan dikkatli �ekilde kullan�lmal�d�r. Ba�lang��taki performans skoru 2 olan, tedavi edilmi� leptomenengeal metastazlar� olan, ok�ler/uveal melanomu olan, otoimm�n hastal��� olan hastalar ve �nceki anti-CTLA-4 tedavisine ba�l� olarak Derece 3-4 advers reaksiyon geli�mi� olan hastalar CA209172 �al��mas�na al�nm��t�r (bkz. B�l�m 5.1). �al��maya girmeden �nce sistemik imm�nos�presif tedavi alan hastalar ve aktif beyin ya da leptomenengeal metastazlar� olan hastalar hakk�nda veri bulunmamas� nedeniyle bu pop�lasyonda nivolumab�n olas� yarar�/riski bireysel bazda dikkatle de�erlendirdikten sonra kullan�lmas� gerekir.
Nivolumab monoterapisine k�yasla, nivolumab ve ipilimumab kombinasyonunda PFS art��� yaln�zca d���k t�m�r PD-L1 ekspresyonuna sahip hastalarda g�sterilmi�tir. OS'deki iyile�me y�ksek t�m�r PD-L1 ekspresyonuna (PD-L1 ≥ %1) sahip hastalarda ipilimumab ile kombinasyon halinde nivolumab ve nivolumab monoterapisi aras�nda benzer olmu�tur. Kombinasyon tedavisini ba�latmadan �nce, hekimlere nivolumab monoterapisine k�yasla kombinasyon tedavisinin g�zlemlenen yararlar�n� ve toksisitesini dikkate alarak hastay� ve t�m�r �zelliklerini bireysel olarak dikkatli bir bi�imde de�erlendirmeleri �nerilir (bkz. B�l�m 4.8 ve 5.1).
H�zla ilerleyen hastal��� bulunan melanom hastalar�nda nivolumab kullan�m�
H�zla ilerleyen hastal��� bulunan hastalarda tedaviye ba�lamadan �nce doktorlar nivolumab etkisinin gecikmeli ba�lang�c�n� dikkate almal�d�r (bkz. b�l�m 5.1).
Melanom adjuvan tedavisi
Daha �nce otoimm�n hastal�k ve kortikosteroidlerle (≥ 10 mg g�nl�k prednizon veya e�de�eri) veya di�er imm�nos�presif ila�larla sistemik tedavi gerektiren herhangi bir hastal�k g�r�len hastalar ve yan� s�ra daha �nce melanom i�in tedavi g�rm�� olan hastalar (randomizasyondan ≥ 6 ay �nce tamamlanm�� olmas� ko�uluyla daha �nce adjuvan interferon, cerrahi, merkezi sinir sistemi lezyonlar�n�n n�rocerrahiyle rezeksiyonu sonras� adjuvan radyoterapi uygulanm�� olan hastalar hari�), anti-PD-1, anti-PD-L1, anti-PD-L2, anti-CD137 veya anti-CTLA-4 antikoru (ipilimumab veya spesifik olarak T-h�cre kostimulasyonu veya kontrol noktas� mekanizmalar�n� hedef alan ba�ka herhangi bir antikor veya ila� dahil) ile daha �nce tedavi uygulanm�� hastalar ve 18 ya��n alt�ndaki g�n�ll�ler adjuvan melanom tedavisine ili�kin pivot �al��maya dahil edilmemi�tir (bkz. B�l�m 4.5 ve 5.1). Veri mevcut olmad���ndan nivolumab bu pop�lasyonlarda ki�i baz�nda potansiyel yarar/risk de�erlendirmesi yap�lmas�n�n ard�ndan dikkatli �ekilde kullan�lmal�d�r.
H�zl� ilerleyen hastal���n g�r�ld��� melanom hastalar�nda OPDIVO kullan�m�
Doktorlar hastal���n h�zl� �ekilde ilerledi�i hastalarda tedavi ba�lamadan �nce nivolumab�n ge� etki ba�lang�c�n� g�z �n�nde bulundurmal�d�r (bkz. B�l�m 5.1).
K���k H�creli D��� Akci�er Kanseri KHDAK'nin birinci basamak tedavisi
Aktif otoimm�n hastal���, semptomatik interstisyel akci�er hastal���, sistemik
imm�nosupresyon gerektiren t�bbi ko�ullar�, aktif (tedavi edilmemi�) beyin metastaz� olan, ilerlemi� hastal�k i�in daha �nce sistemik tedavi g�rm�� veya EGFR mutasyonlar� veya ALK translokasyonlar� olan hastalar, KHDAK'nin birinci basamak tedavisini ara�t�ran k�lavuz �al��malara dahil edilmemi�tir (bkz. B�l�m 4.5 ve 5.1). Ya�l� hastalarda (≥ 75 ya�) s�n�rl� veri mevcuttur (bkz. B�l�m 5.1). Bu hastalarda, ipilimumab ve kemoterapi ile kombinasyon halinde nivolumab, ki�i baz�nda potansiyel yarar/risk de�erlendirmesi yap�lmas�n�n ard�ndan dikkatli �ekilde kullan�lmal�d�r.
Kemoterapiden sonra KHDAK
Ba�lang�� performans skoru ≥ 2 olan, aktif beyin metastazlar� veya otoimm�n hastal�k g�r�len, semptomatik interstisyel akci�er hastal��� olan ve �al��maya girmeden �nce sistemik imm�nosupresan tedaviler alan hastalar KHDAK klinik �al��malar�na al�nmam��t�r (bkz. B�l�m 4.5 ve 5.1). Ba�lang��taki performans skoru 2 olan hastalar CA209171 �al��mas�na al�nm��t�r (bak�n�z B�l�m 5.1). Otoimm�n hastal��� olan, semptomatik interstisyel akci�er hastal��� olan, aktif beyin metastazlar� olan hastalar ve �al��maya girmeden �nce sistemik imm�nos�presif tedavi alan hastalar, veri bulunmamas� nedeniyle bu pop�lasyonda nivolumab�n olas� yarar�/riski bireysel bazda dikkatle de�erlendirdikten sonra kullan�lmas� gerekir.
Doktorlar nispeten k�t� prognostik �zelliklere ve/veya agresif hastal��a sahip hastalarda tedavi ba�latmadan �nce nivolumab�n ge� etki ba�lang�c�n� g�z �n�nde bulundurmal�d�r. Non-skuam�z KHDAK'de dosetaksele k�yasla nivolumabla 3 ay i�inde daha y�ksek say�da �l�m g�zlenmi�tir. Daha k�t� prognostik fakt�rler ve/veya daha agresif hastal�k ile birlikte t�m�r PD-L1 ekspresyonunun d���k olmas� veya hi� olmamas� erken �l�mlerle ili�kili fakt�rler olmu�tur (bkz. B�l�m 5.1).
Malign plevral mezotelyoma
Primitif peritoneal, perikardiyal, testis veya tunika vajinalis mezotelyomas�, interstisyel akci�er hastal���, aktif otoimm�n hastal���, sistemik imm�nosupresyon gerektiren t�bbi ko�ullar� ve beyin metastaz� olan hastalar (cerrahi olarak rezeke edilmedik�e veya stereotaksik radyoterapi ile tedavi edilmedik�e ve tedaviye dahil edilmeden �nceki 3 ay i�inde herhangi bir geli�me olmad�k�a) MPM'nin birinci basamak tedavisini ara�t�ran k�lavuz �al��malara dahil edilmemi�tir (bkz. B�l�m 4.5 ve 5.1). Veri bulunmad���ndan, ipilimumab ile kombinasyon halinde nivolumab bu pop�lasyonlarda ki�i baz�nda potansiyel yarar/risk de�erlendirmesi yap�lmas�n�n ard�ndan dikkatli �ekilde kullan�lmal�d�r.
Renal H�creli Karsinom
E� zamanl� beyin metastaz� varl��� ya da beyin metastaz� �yk�s� olan, aktif otoimm�n hastal��� ya da sistemik imm�nosupresyon gerektiren t�bbi durumlar� olan hastalar, pivot RHK �al��malar�na dahil edilmemi�tir (bkz. B�l�m 4.5 ve 5.1). Verilerin olmad��� durumlarda nivolumab monoterapisi veya ipilimumab ile kombinasyon halinde nivolumab, bu pop�lasyonlarda her hasta i�in bireysel olarak potansiyel risk-yarar�n dikkatli de�erlendirilmesinden sonra dikkatle kullan�lmal�d�r.
Klasik Hodgkin Lenfoma
Aktif otoimm�n hastal��a ve semptomatik interstisyal akci�er hastal���na sahip hastalar,
Klasik Hodgkin lenfoma klinik �al��malar�n�n d���nda b�rak�lm��t�r (bkz. B�l�m 5.1). �lgili
veri mevcut olmad���ndan OPDIVO bu pop�lasyonlarda dikkatli bir �ekilde, potansiyel fayda/risk oran� bireysel bazda de�erlendirildikten sonra kullan�lmal�d�r.
Klasik Hodgkin Lenfomada allojenik Hematopoietik K�k H�cre Naklinin (HKHN) Komplikasyonlar�
Nivolumaba maruz kal�m�n ard�ndan allojenik HKHN uygulanan hastalar�n izleminden elde edilen �n bulgular, akut greft-versus-host hastal��� (aGVHD) ve transplantla ili�kili mortalite (TRM) vakalar�n�n say�s�n�n beklenenin �zerinde oldu�unu g�stermi�tir. �lave veri elde edilene kadar HKHN'nin potansiyel faydalar� ve transplantla ili�kili komplikasyonlarda art�� ortaya ��kmas� potansyeli �zerinde vaka baz�nda dikkatli bir �ekilde durulmal�d�r (bkz. B�l�m 4.8).
Allojenik HKHN sonras� nivolumab ile tedavi edilen hastalarda, pazarlama sonras� d�nemde baz�lar� �l�mle sonu�lanm�� olan h�zl� ba�lang��l� ve ciddi GVHD bildirilmi�tir. Nivolumab ile tedavi, �zellikle daha �nce GVHD �yk�s� olanlar olmak �zere �nceden allojenik HKHN ge�irmi� olan hastalarda ciddi GVHD ve �l�m riskini art�rabilir. Bu hastalarda nivolumab ile tedavinin yarar�na kar��l�k muhtemel riskleri g�z �n�nde bulundurulmal�d�r (bkz. B�l�m 4.8).
Ba� ve Boyun Kanseri
Ba�lang�� performans skoru ≥2 olan, aktif beyin metastazlar�na veya leptomeninjel metastazlara sahip olan, aktif otoimm�n hastal�k, sistemik imm�nosupresyon gerektiren t�bbi sorunlar g�r�len veya primer t�m�r b�lgeleri nazofarenks ya da t�k�r�k bezi karsinomu olan ki�iler SHBBK klinik �al��mas� d���nda b�rak�lm��t�r (bkz. B�l�m 4.5 ve 5.1). Veri mevcut olmad���ndan nivolumab bu pop�lasyonlarda ki�i baz�nda potansiyel yarar/risk de�erlendirmesi yap�lmas�n�n ard�ndan dikkatli �ekilde kullan�lmal�d�r.
Doktorlar daha k�t� prognostik �zelliklere ve/veya agresif hastal��a sahip hastalarda tedaviye ba�lamadan �nce nivolumab etkisinin ge� ba�lang�c�n� g�z �n�nde bulundurmal�d�r. Ba� ve boyun kanserinde dosetaksele k�yasla nivolumabla 3 ay i�inde daha y�ksek say�da �l�m g�zlenmi�tir. Erken �l�mlerle ili�kili fakt�rlerin ECOG performans durumu, �nceki platin tedavisi s�ras�nda h�zl� progresyon sergileyen hastal�k ve y�ksek t�m�r y�k� oldu�u belirlenmi�tir.
dMMR veya MSI-H Metastatik Kolorektal Kanser
Bazal performans skoru ≥ 2, aktif beyin metastazlar�, aktif otoimm�n hastal��� veya sistemik imm�nos�presyon gerektiren t�bbi rahats�zl�klar� olan hastalar, dMMR veya MSI-H mKRK i�in yap�lan klinik �al��malara dahil edilmemi�tir (Bkz. B�l�m 4.5 ve 5.1). Veri bulunmad��� durumlarda, nivolumab bu pop�lasyonlarda potansiyel yarar/riskin bireysel olarak dikkatli bir �ekilde ele al�nmas�ndan sonra dikkatli bir �ekilde kullan�lmal�d�r.
�zofagus Skuam�z H�creli Karsinom
�zofagus skuam�z h�creli karsinomla ilgili mevcut klinik verilerin �o�unlu�u Asya k�kenli hastalardan elde edilmektedir (bkz. B�l�m 5.1).
Ba�lang�� performans skoru ≥ 2 olan, semptomatik veya tedavi gerektiren beyin metastazlar�, yemek borusuna biti�ik organlarda (�rn. aort veya solunum yolu) belirgin t�m�r invazyonu, aktif otoimm�n hastal��� veya sistemik imm�nos�presyon gerektiren t�bbi durumlar� bulunan hastalar �SHK hakk�ndaki klinik �al��man�n d���nda b�rak�lm��t�r (bkz. B�l�m 4.5 ve 5.1). Veri bulunmad���ndan, nivolumab bu pop�lasyonlarda ki�i baz�nda potansiyel yarar/risk de�erlendirmesi yap�lmas�n�n ard�ndan dikkatli �ekilde kullan�lmal�d�r.
Doktorlar �SHK'li hastalarda tedaviye ba�lamadan �nce nivolumab�n ge� etki ba�lang�c�n� g�z �n�nde bulundurmal�d�r. Kemoterapiye k�yasla, nivolumab ile randomizasyondan sonraki
2,5 ay i�inde daha y�ksek say�da �l�m g�zlenmi�tir. Erken �l�mlerle ilgili hi�bir spesifik fakt�r belirlenememi�tir (bkz. B�l�m 5.1).
Bir talidomid analo�u ve deksametazona OPDIVO eklendi�inde multipl miyelom hastalar�nda artan mortalite
Multipl miyelom hastalar� �zerinde ger�ekle�tirilen randomize klinik �al��malarda PD-1 veya PD-L1 bloke edici antikorun endike olmad��� bir kullan�m olan talidomid analo�u + deksametazona, OPDIVO'nun da aralar�nda oldu�u bir PD-1 bloke edici antikorun eklenmesi mortalitede art��la sonu�lanm��t�r. Multipl miyelom hastalar�na bir talidomid analo�u + deksametazonla kombinasyon halinde bir PD-1 veya PD-L1 bloke edici antikorla tedavi uygulanmas� kontroll� klinik �al��malar d���nda �nerilmemektedir.
Di�er t�m terap�tik proteinlerde oldu�u gibi OPDIVO i�in de potansiyel immunojenesite riski s�z konusudur. Biyolojik t�bbi �r�nlerin takip edilebilirli�inin sa�lanmas� i�in uygulanan �r�n�n ticari ismi ve seri numaras� mutlaka hasta dosyas�na kaydedilmelidir.
�zofagus veya gastro�zofageal bile�ke kanserinin adjuvan tedavisi
Ba�lang�� performans skoru ≥ 2 olup, cerrahi �ncesinde e�zamanl� kemoradyoterapi (KRT) almam��, IV. evre rezeke edilebilir hastal���, aktif otoimm�n hastal��� ya da sistemik imm�nos�presyon gerektiren t�bbi durumlar� olan hastalar �zofagus ve gastro�zofageal bile�ke kanseri i�in yap�lan klinik �al��maya dahil edilmemi�tir (bkz. B�l�m 4.5 ve 5.1). Veri bulunmad���nda, nivolumab bu pop�lasyonlarda potansiyel fayda-risk oran�n�n bireysel olarak ele al�nmas�ndan sonra dikkatli bir �ekilde kullan�lmal�d�r.
Mide, gastro�zofageal bile�ke ya da �zofagus adenokarsinom
Ba�lang�� ECOG performans skoru ≥ 2 olup, tedavi edilmemi� merkezi sinir sistemi metastazlar� olan, aktif, bilinen ya da ��phelenilen otoimm�n hastal��� bulunan veya sistemik imm�nos�presyon gerektiren t�bbi durumlar� mevcut hastalar, mide, GBK ya da �zofagus adenokarsinomu i�in yap�lan klinik �al��maya dahil edilmemi�tir (bkz. B�l�m 4.5 ve 5.1). Veri bulunmad���nda, kemoterapi ile kombinasyon halindeki nivolumab bu pop�lasyonlarda potansiyel fayda-risk oran�n�n bireysel olarak ele al�nmas�ndan sonra dikkatli bir �ekilde kullan�lmal�d�r.
�al��ma CA209649'da, bilinen HER-2 pozitif durumu olan hastalar hari� tutulmu�tur. Belirsiz durumdaki hastalar�n �al��maya kat�lmas�na izin verilmi� olup; hastalar�n %40,3'�n� temsil ediyorlard� (bkz. B�l�m 5.1).
Kontroll� sodyum diyetindeki hastalar
Her 1 mL m�stahzar 0,1 mmol (veya 2,5 mg) sodyum i�erir. Kontroll� sodyum diyetinde olan hastalar� tedavi ederken bu durum dikkate al�nmal�d�r.
Hasta Uyar� Kart�
OPDIVO re�eteleyen t�m uzmanlar Doktorlara Y�nelik Bilgi ve Y�netim K�lavuzlar� konusunda bilgi sahibi olmal�d�r. Re�eteyi yazan uzman OPDIVO tedavisinin riskleri konusunda hasta ile konu�mal�d�r. Hastaya her re�ete ile birlikte Hasta Uyar� Kart� verilecektir.
�zlenebilirlik
Biyolojik t�bbi �r�nlerin izlenebilirli�ini artt�rmak i�in uygulanan �r�n�n ad� ve seri numaras� a��k �ekilde kaydedilmelidir.
4.5. Di�er t�bbi �r�nler ile etkile�imler ve di�er etkile�im �ekilleri
Nivolumab insana �zg� bir monoklonal antikor oldu�undan, farmakokinetik etkile�im �al��malar� ger�ekle�tirilmemi�tir. Monoklonal antikorlar sitokrom P450 (CYP) enzimleri veya di�er ila� metabolize eden enzimler taraf�ndan metabolize edilmedi�inden, e�zamanl� uygulanan ila�larla bu enzimlerin inhibisyonu veya ind�ksiyonunun nivolumab�n farmakokineti�ini etkilemesi beklenmez.
Di�er etkile�im formlar�
Sistemik imm�nos�presyon
Farmakodinamik aktiviteyle etkile�im potansiyeli nedeniyle nivolumaba ba�lamadan �nce, ba�lang��ta sistemik kortikosteroidlerin ve di�er imm�nosupresanlar�n kullan�m�ndan ka��n�lmal�d�r. Yine de, imm�n ili�kili advers reaksiyonlar�n tedavi edilmesi i�in nivolumaba ba�land�ktan sonra sistemik kortikosteroidler veya di�er imm�nos�presanlar kullan�labilir. Ba�lang��ta al�nan sonu�lar, OPDIVO tedavisine ba�land�ktan sonra sistemik imm�nos�presyon kullan�m�n�n, nivolumaba verilen yan�t� bozmad���n� g�stermektedir.
�zel pop�lasyonlara ili�kin ek bilgiler
Hi�bir etkile�im �al��mas� yap�lmam��t�r.
Pediyatrik pop�lasyon
Hi�bir etkile�im �al��mas� yap�lmam��t�r.
4.6. Gebelik ve laktasyon
Genel tavsiyeGebelik kategorisi: D
�ocuk do�urma potansiyeli bulunan kad�nlar /Do�um kontrol� (kontrasepsiyon)
Klinik yararlar� olas� risklerinden fazla olmad�k�a etkili bir do�um kontrol y�ntemi kullanmayan �ocuk do�urma potansiyeline sahip kad�nlarda nivolumab kullan�m� �nerilmemektedir. Kad�nlara nivolumab�n son dozunu takip eden en az 5 ay s�resince etkili bir do�um kontrol y�ntemi kullanmalar� �nerilmelidir.
Gebelik d�nemi
Gebe kad�nlarda nivolumab kullan�m�na ili�kin herhangi bir veri mevcut de�ildir. Hayvanlarda yap�lan �al��malar embriyofetal toksisite kan�t� g�stermi�tir (bkz. B�l�m 5.3). �nsan IgG4'�n�n plasenta bariyerini ge�ti�i bilinmektedir ve nivolumab bir IgG4 oldu�undan; nivolumab�n anneden geli�mekte olan fetusa ta��nma potansiyeli vard�r. Nivolumab, klinik yararlar� olas� risklerinden fazla olmad�k�a, gebelik s�ras�nda kullan�lmamal�d�r.
Laktasyon d�nemi
Nivolumab�n anne s�t�ne ge�ip ge�medi�i bilinmemektedir. Antikorlar dahil olmak �zere bir�ok t�bbi �r�n anne s�t�ne ge�ti�inden, yeni do�anda/bebekte olu�abilecek risk g�z ard� edilemez. Emzirmenin bebe�e ve tedavinin anneye yarar� dikkate al�narak, emzirmenin veya nivolumab tedavisinin kesilmesi konusunda bir karar verilmelidir.
�reme yetene�i/Fertilite
Nivolumab�n fertilite �zerindeki etkilerini de�erlendiren �al��malar yap�lmam��t�r. Bu durumda, nivolumab�n erkek ve di�i fertilitesi �zerindeki etkisi bilinmemektedir.
4.7. Ara� ve makine kullan�m� �zerindeki etkiler
5.1. Farmakodinamik �zellikler
ine dayanarak, nivolumab�n ara� ve makine kullanma becerisini etkilemesi beklenmez. Yorgunluk gibi potansiyel advers reaksiyonlara yol a�abilmesi nedeniyle (bkz. B�l�m 4.8), hastalara OPDIVO'nun kendilerini ters bir �ekilde etkilemedi�inden emin olana dek ara� veya makine kullanmalar� konusunda dikkatli olmalar� �nerilmelidir.
4.8. �stenmeyen etkiler
Monoterapi olarak nivolumab (bkz. B�l�m 4.2)
G�venlilik profilinin �zeti
�e�itli t�m�r tiplerinde nivolumab monoterapisi ile yap�lan �al��malar�n (n = 4122) birle�tirilmi� veri setinde minimum takip aral��� 2,3 ila 28 ay olup, en yayg�n (≥ %10) yan etkiler yorgunluk (%45), kas iskelet a�r�s� (%31), diyare (%26), bulant� (%23), �ks�r�k
(%24), d�k�nt� (%24), dispne (%17), ka��nt� (%19), i�tahs�zl�k (%18), kab�zl�k (%17), kar�n
a�r�s� (%16), �st solunum yolu enfeksiyonu (%16), artralji (%14), pireksi (%14), kusma (%14), ba� a�r�s� (%13) ve �dem (%10) olmu�tur. . Advers reaksiyonlar�n �o�u hafif ila orta �iddetliydi (Derece 1 veya 2). KHDAK'de minimum 63 ayl�k bir izlemle herhangi yeni bir g�venlilik sinyali tespit edilmemi�tir.
Yan etkilerin �zeti
Nivolumab monoterapisi ile tedavi edilen hastalar i�in (n = 4122) birle�tirilmi� veri setinde bildirilen advers reaksiyonlar Tablo 4'te listelenmi�tir. Bu reaksiyonlar, sistem organ s�n�f� ve s�kl�k kategorilerine g�re sunulmu�tur. S�kl�k terimleri a�a��daki �ekilde tan�mlanmaktad�r: �ok yayg�n (≥ 1/10); yayg�n (≥ 1/100 ila <1/10); yayg�n olmayan (≥1/1.000 ila <1/100); seyrek (≥1/10.000 ila <1/1.000); �ok seyrek (<1/10.000), bilinmiyor (eldeki verilerden hareketle tahmin edilemiyor). Her s�kl�k derecesi grubunda advers reaksiyonlar azalan ciddiyet s�ras�nda g�re sunulmaktad�r.
Tablo 4: Nivolumab monoterapisi ile g�zlenen advers reaksiyonlar
Enfeksiyonlar ve enfestasyonlar | |
�ok yayg�n: | �st solunum yolu enfeksiyonu |
Yayg�n: | Pn�moni, bron�it |
Seyrek | Aseptik menenjit |
(Kist ve polipler de dahil olmak �zere) iyi huylu, k�t� huylu ve belirlenemeyen neoplazma | |
Seyrek: | Histositik nekrotizan lenfadenit (Kikuchi lenfadenit) |
Kan ve lenf sistemi hastal�klar� | |
�ok Yayg�n: | Lenfopeni , anemi, l�kopeni, n�tropeni, trombositopeni |
Yayg�n olmayan | Eozinofili |
Bilinmiyor: | Hemofagositik lenfohistiyositoz |
Ba����kl�k sistemi hastal�klar� | |
Yayg�n: | �nf�zyonla ili�kili reaksiyon, a��r� duyarl�l�k (anafilaktik reaksiyonu i�eren) |
Yayg�n olmayan: | Sarkoidozis |
Bilinmiyor: | Solid organ nakli reddi |
Endokrin hastal�klar� | |
Yayg�n: | Hipotiroidizm, hipertiroidizm, tiroidit |
Yayg�n olmayan: | Adrenal yetmezlik, hipopituitarizm, hipofizit, diyabet mellitus |
Seyrek | Diyabetik ketoasidoz, hipoparatiroidi |
Metabolizma ve beslenme hastal�klar� | |
�ok yayg�n: | ��tah azalmas�, hiperglisemi, hipoglisemi |
Yayg�n: | Dehidratasyon, kilo kayb� |
Yayg�n olmayan: | Metabolik asidoz |
Bilinmiyor: | T�m�r lizis sendromu |
Sinir sistemi hastal�klar� | |
�ok yayg�n: | Ba� a�r�s� |
Yayg�n: | Periferik n�ropati, sersemlik |
Yayg�n olmayan: | Polin�ropati, otoimm�n n�ropati (fasiyal ve ok�ler sinir parezisi dahil) |
Seyrek: | Guillain-Barré sendromu, demiyelinizasyon, miyastenik sendrom, ensefalit |
G�z hastal�klar� | |
Yayg�n: | Bulan�k g�rme, g�z kurulu�u |
Yayg�n olmayan: | �veit |
Bilinmiyor: | Vogt-Koyanagi-Harada sendromu |
Kardiyak hastal�klar | |
Yayg�n: | Ta�ikardi, atriyal fibrilasyon |
Yayg�n olmayan: | Miyokardit, perikardiyal bozukluklar, aritmi (ventrik�ler aritmi dahil) |
Vask�ler hastal�klar | |
Yayg�n: | Hipertansiyon |
Seyrek: | Vask�lit |
Solunum, g���s bozukluklar� ve mediastinal hastal�klar | |
�ok yayg�n: | Dispne, �ks�r�k |
Yayg�n: | Pn�moni, plevral ef�zyon |
Yayg�n olmayan | Akci�er infiltrasyonu |
Gastrointestinal hastal�klar | |
�ok yayg�n: | Diyare, kusma, bulant�, kar�n a�r�s�, kab�zl�k |
Yayg�n: | Kolit, stomatit, a��z kurulu�u |
Yayg�n olmayan: | Pankreatit, gastrit |
Seyrek: | Duodenal �lser |
Hepatobiliyer hastal�klar | |
Yayg�n olmayan: | Hepatit, kolestazis |
Deri ve deri alt� doku hastal�klar� | |
�ok yayg�n: | D�k�nt�, ka��nt� |
Yayg�n: | Vitiligo, kuru cilt, eritem, alopesi, �rtiker |
Yayg�n olmayan: | Eritema multiforme, psoriasis, rosacea |
Seyrek: | Toksik epidermal nekroliz , Stevens-Johnson sendromu |
Bilinmiyor: | Liken sklerozus, di�er liken bozukluklar� |
Kas iskelet bozukluklar� ve ba� doku hastal�klar� | |
�ok yayg�n: | Kas iskelet a�r�s�, artralji |
Yayg�n: | Artrit |
Yayg�n olmayan: | Polimyalji romatika |
Seyrek: | Sjogren's sendrom, miyopati, miyozit (polimiyozit dahil), rabdomiyoliz, |
B�brek ve idrar yolu hastal�klar� | |
Yayg�n: | B�brek yetmezli�i (akut b�brek hasar� dahil) |
Seyrek: | Tubulointerstisyel nefrit, infektif olmayan sistit |
Genel bozukluklar ve uygulama b�lgesine ili�kin hastal�klar | |
�ok yayg�n: | Yorgunluk, pireksi, �dem |
Yayg�n | A�r�, g���s a�r�s� |
Ara�t�rmalar | |
�ok yayg�n: | AST art���, hiponatermi, hipoalbuminemi, alkalen fosfataz art���, kreatinin art���, ALT art���, lipaz art���, hiperkalemi, amilaz art���, hipokalsemi, hipomagnezemi, hipokalemi, hiperkalsemi |
Yayg�n: | Toplam bilirubin art���, hipernatremi, hipermagnezemi |
Tablo 4'te sunulan advers reaksiyon s�kl�klar�, tam olarak tek ba��na nivolumaba ba�lanamaz, ancak altta yatan hastal��a katk�da bulunabilir.
Tamamlanm�� veya devam eden klinik �al��malarda fatal olgular bildirilmi�tir.
4.9. Doz a��m� ve tedavisi
Klinik �al��malarda doz a��m� vakas� bildirilmemi�tir. Doz a��m� halinde, hastan�n advers reaksiyon bulgu ve semptomlar� a��s�ndan yak�ndan g�zlemlenmesi ve uygun semptomatik tedaviye ba�lanmas� �nerilir.
5. FARMAKOLOJ�K �ZELL�KLER
5.1. Farmakodinamik �zellikler
ine dayanarak, nivolumab�n ara� ve makine kullanma becerisini etkilemesi beklenmez. Yorgunluk gibi potansiyel advers reaksiyonlara yol a�abilmesi nedeniyle (bkz. B�l�m 4.8), hastalara OPDIVO'nun kendilerini ters bir �ekilde etkilemedi�inden emin olana dek ara� veya makine kullanmalar� konusunda dikkatli olmalar� �nerilmelidir.
Farmakoterap�tik grup: Antineoplastik ajanlar, monoklonal antikorlar,antikor ila� ATC kodu: L01FF01.
Etki mekanizmas�
Nivolumab, programlanm�� �l�m-1 (PD-1) resept�r�ne ba�lanan ve PD-L1 ve PD-L2 ile etkile�imi bloke eden insan imm�noglobulin G4 (IgG4) monoklonal antikorudur (HuMAb).
PD-1 resept�r�, T-h�cre imm�n yan�tlar�n�n kontrol�ne kat�ld��� g�sterilmi� olan, T-h�cre aktivitesinin negatif bir d�zenleyicisidir. PD-1'in, antijen sunucu h�creler taraf�ndan ve belki de t�m�r veya t�m�r mikro�evresindeki di�er h�creler taraf�ndan da eksprese edilebilen PD-L1 ve PD-L2 ligandlar�yla ba�lanmas�, T-h�cre proliferasyonunun ve sitokin sal�m�n�n
inhibisyonu ile sonu�lan�r. Nivolumab, PD-1'in PD-L1 ve PD-L2 ligandlar�na ba�lanmas�n� bloke ederek, anti-t�m�r yan�tlar dahil, T-h�cresi yan�tlar�n� artt�r�r. Genetik olarak �zde� fare modellerinde, bloke edici PD-1 aktivitesi, t�m�r b�y�mesinin azalmas� ile sonu�lanm��t�r.
Klinik etkililik ve g�venlilik
Doz/maruziyet etkililik ve g�venlilik ili�kilerinin modellenmesine dayanarak, her 2 haftada bir 240 mg veya her 2 haftada bir 3 mg/kg nivolumab aras�nda etkililik ve g�venlilik a��s�ndan klinik olarak anlaml� bir fark bulunmamaktad�r. Ek olarak, bu ili�kilere dayanarak, RHK'de 4 haftada bir 480 mg veya her 2 haftada bir 3 mg/kg nivolumab dozu aras�nda klinik olarak anlaml� bir fark g�r�lmemi�tir.
Melanom
�lerlemi� melanom tedavisi
Dakarbazin kar��s�nda randomize faz 3 �al��ma (CA209066)
Nivolumab 3 mg/kg'�n ilerlemi� (rezeke edilemeyen veya metastatik) melanom tedavisi i�in g�venlili�i ve etkilili�i bir faz 3, randomize, �ift k�r �al��mada (CA209066) de�erlendirilmi�tir. �al��maya do�rulanm��, tedavi uygulanmam��, Evre III veya IV BRAF vah�i tip melanomu olan ve ECOG performans durumu 0 veya 1 olan yeti�kin hastalar (18 ya� ve �zeri) dahil edilmi�tir. Aktif otoimm�n hastal���, ok�ler melanomu veya aktif beyin ya da leptomeningeal metastazlar� bulunan hastalar �al��maya al�nmam��t�r.
Toplam 418 hasta her 2 haftada bir 60 dakika s�reyle intraven�z yoldan uygulanan 3 mg/kg dozunda nivolumab (n = 210) veya her 3 haftada bir 1000 mg/m2 dozunda dakarbazin (n = 208) almak �zere randomize edilmi�tir. Randomizasyon, t�m�r PD-L1 durumu ve M evresi (M1c kar��s�nda M0/M1a/M1b) ile basamakland�r�lm��t�r. Tedavi, klinik yarar g�zlendi�i s�rece veya tedavi hasta taraf�ndan art�k tolere edilemeyinceye kadar s�rd�r�lm��t�r. Hastal�k progresyonundan sonra tedaviye, ara�t�rmac� taraf�ndan belirlendi�i gibi klinik yarar g�ren ve �al��ma ilac� ile �nemli bir advers olay ya�amam�� olan hastalarda izin verilmi�tir. T�m�r de�erlendirmeleri, randomizasyondan 9 hafta sonra, ard�ndan ilk y�l her 6 haftada bir ve bunu takip eden y�llarda her 12 haftada bir, Solid T�m�rlerde Yan�t De�erlendirme Kriterleri (RECIST), versiyon 1.1 uyar�nca ger�ekle�tirilmi�tir. Primer etkililik sonlan�m noktas� genel sa�kal�md� (OS). Kilit sekonder etkililik sonlan�m noktas� �l��mleri, ara�t�rmac� taraf�ndan de�erlendirilen progresyonsuz sa�kal�m (PFS) ve objektif yan�t oran� (ORR) idi.
�ki grup aras�nda ba�lang�� �zellikleri dengelenmi�ti. Ya� ortalamas� 65 olup (aral�k: 18 - 87)
%59'u erkek ve %99,5'i beyazd�. Ba�lang�� ECOG performans durumu puan� 0 (%64) veya 1 (%34) idi. Hastalar�n %61'i, �al��maya giri�te evre M1c hastal��a sahipti. %74'� kutan�z melanom, %11'i mukozal melanom; %35'i ise PD-L1 pozitif melanoma sahipti (>%5 t�m�r h�cresi membran ekspresyonu). Hastalar�n %16's�, daha �nce adjuvan tedavi g�rm�� olup en yayg�n kullan�lan adjuvan tedavi interferondu (%9). Hastalar�n %4'�nde �al��ma giri�inde beyin metastaz�, %37'sinde ise ULN'den y�ksek LDH d�zeyi mevcuttu.
OS i�in Kaplan-Meier e�rileri �ekil 1'de g�sterilmektedir.
Progresyonsuz sa�kal�m
�ekil 1. Kaplan-Meier OS e�rileri (CA209066)
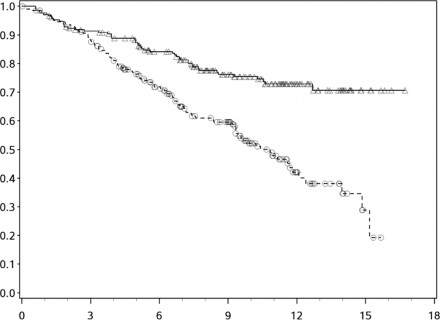
Genel Sa�kal�m (Ay)
Riskli g�n�ll�lerin say�s� | ||||||
Nivolumab | ||||||
210 | 185 | 150 | 105 | 45 | 8 | 0 |
Dakarbazin | ||||||
208 | 177 | 123 | 82 | 22 | 3 | 0 |
─∆─── Nivolumab (olaylar: 50/210), medyan ve %95 GA: ge�erli de�il.
- - -- - - Dakarbazin (olaylar: 96/208), medyan ve %95 GA: 10,84 (9,33 - 12,09)
G�zlenen OS yarar�, ba�lang�� ECOG performans durumu, M evresi, beyin metastaz �yk�s� ve ba�lang�� LDH d�zeyi dahil hasta alt gruplar�nda tutarl� �ekilde g�sterilmi�tir.
T�m�rlerin PD-L1 negatif veya PD-L1 pozitif olarak s�n�fland�r�lmas�ndan ba��ms�z olarak sa�kal�m yarar� g�zlenmi�tir (%5 veya %10'luk t�m�r membran� ekspresyonu e�ik de�eri).
Elde edilen veriler, nivolumab�n ge� etki ba�lang�c�na sahip oldu�unu ve kemoterapiden sonra nivolumab yarar�n�n ortaya ��kmas�n�n 2-3 ay s�rebilece�ini g�stermi�tir.
Yan�t oranlar�, yan�ta kadar ge�en s�re ve yan�t s�releri Tablo 9'da g�sterilmektedir.
Tablo 9: Etkililik Sonu�lar� (CA209066)
| nivolumab (n = 210) | dakarbazin (n = 208) |
Genel sa�kal�m |
| |
Olaylar | 50 (%23,8) | 96 (%46,2) |
Risk oran� | 0,42 | |
%99,79 GA | (0,25 - 0,73) | |
%95 GA | (0,3 - 0,6) | |
p-de�eri | < 0,0001 | |
Medyan (%95 GA) | Eri�ilmedi | 10,8 (9,33 - 12,09) |
Oran (%95 GA) |
| |
6. ayda | 84,1 (78,3 - 88,5) | 71,8 (64,9 - 77,6) |
12. ayda | 72,9 (65,5 - 78,9) | 42,1 (33 - 50,9) |
Progresyonsuz sa�kal�m |
| |
Olaylar | 108 (%51,4) | 163 (%78,4) |
Risk oran� | 0,43 | |
%95 GA | (0,34 - 0,56) | |
p-de�eri | < 0,0001 | |
Medyan (%95 GA) | 5,1 (3,48 - 10,81) | 22 (2,1 - 2,4) |
Oran (%95 GA) |
| |
6. ayda | 48 (40,8 - 54,9) | 18,5 (13,1 - 24,6) |
12. ayda | 41,8 (34 - 49,3) | NA |
Objektif yan�t | 84 (%40) | 29 (%13,9) |
(%95 GA) | (33,3 - 47) | (9,5 - 19,4) |
Olas�l�k oran� (%95 GA) | 4,06 (2,52 - 6,54) |
|
p-de�eri | < 0,0001 |
|
Tam yan�t (CR) | 16 (%7,6) | 2 (%1) |
K�smi yan�t (PR) | 68 (%32,4) | 27 (%13) |
Stabil hastal�k (SD) | 35 (%16,7) | 46 (%22,1) |
Medyan yan�t s�resi |
| |
Ay (aral�k) | Eri�ilmedi (0 - 12,5) | 6 (1,1 - 10) |
Yan�ta kadar medyan s�re |
| |
Ay (aral�k) | 2,1 (1,2 - 7,6) | 2,1 (1,8 - 3,6) |
“” gizlenen bir g�zlemi g�sterir.
Kemoterapi kar��s�nda randomize faz 3 �al��ma (CA209037)
Nivolumab 3 mg/kg'�n ilerlemi� (rezeke edilemeyen veya metastatik) melanom tedavisi i�in g�venlili�i ve etkilili�i bir faz 3, randomize, a��k etiketli �al��mada (CA209037) de�erlendirilmi�tir. �al��ma ipilimumab tedavisi s�ras�nda veya sonras�nda progresyon g�r�len ve (BRAF V600 mutasyonu pozitif ise) BRAF kinaz inhibit�r� tedavisi s�ras�nda veya sonras�nda progresyon g�r�len hastalar� i�ermi�tir.
Aktif otoimm�n hastal��� ve ok�ler melanomu, aktif beyin veya leptomeningeal metastazlar� olanlar veya iyile�mi� bulant�, yorgunluk, inf�zyon reaksiyonlar� veya endokrinopatiler hari� �nceden ipilimumab ile ili�kili y�ksek dereceli (CTCAE v4.0 uyar�nca Derece 4) advers reaksiyon ya�ayan hastalar �al��maya dahil edilmemi�tir.
Toplam 405 hasta her 2 haftada bir 60 dakika s�reyle intraven�z yoldan uygulanan 3 mg/kg dozunda nivolumab (n = 272) veya ara�t�rmac�n�n karar�na g�re dakarbazin (her 3 haftada bir 1000 mg/m2) veya karboplatin (her 3 haftada EAA 6) ve paklitaksel (her 3 haftada bir
175 mg/m2) i�eren kemoterapi (n = 133) almak �zere randomize edilmi�tir. Randomizasyon, BRAF ve t�m�r PD L1 durumu ve �nceki ipilimumab tedavisine verilen en iyi yan�ta g�re basamakland�r�lm��t�r.
Yard�mc� primer etkililik sonu� �l��mleri, nivolumab tedavisi g�ren ilk 120 g�n�ll�de RECIST versiyon 1.1 kullan�larak ba��ms�z bir radyolojik inceleme komitesi (IRRC) taraf�ndan �l��ld��� gibi do�rulanm�� ORR ve nivolumab ile elde edilen OS'nin kemoterapi ile kar��la�t�r�lmas�n� i�ermi�tir. �lave sonu� �l��mleri, yan�t s�resi ve zaman�yd�.
Hastalar�n medyan ya�� 60 idi (aral�k: 23 - 88). Hastalar�n y�zde %64'� erkekti ve %98'i beyazd�. ECOG performans skorlar� hastalar�n %61'i i�in 0 ve %39'u i�in 1 idi. Hastalar�n �o�unlu�u (%75) �al��maya giri�te evre M1c hastal��a sahipti. Hastalar�n %73'� kutan�z melanom ve %10'u mukozal melanom idi.
�nceden al�nan sistemik tedavi say�s� hastalar�n %27'sinde 1, %51'inde 2 ve %21'inde
> 2 idi. Hastalar�n %22'sinin BRAF mutasyonu pozitifti ve %50'si PD-L1 pozitifti. Hastalar�n
%64'�, �nceki ipilimumab tedavisinden klinik yarar (CR/PR ya da SD) g�rmemi�tir.
Ba�lang�� �zellikleri, beyin metastaz� olan hastalar�n oran� (nivolumab grubu ve kemoterapi grubunda s�ras�yla %19 ve %13) ve ba�lang�� LDH d�zeyi ULN'den y�ksek olan hastalar�n oran� (s�ras�yla %51 ve %35) hari�, gruplar aras�nda dengeliydi.
Bu nihai ORR analizi d�neminde, en az 6 ay takip edilen nivolumab alan 120 hastadan ve kemoterapi alan 47 hastadan al�nan sonu�lar analiz edilmi�tir. Etkililik sonu�lar� Tablo 10'da sunulmu�tur.
Tablo 10: En iyi genel yan�t, zaman ve yan�t s�resi (CA209037)
| nivolumab (n = 120) | kemoterapi (n = 47) |
Objektif yan�t (IRRC) |
38 (%31,7) |
5 (%10,6) |
(%95 GA) | (23,5 - 40,8) | (3,5 - 23,1) |
Tam yan�t (CR) | 4 (%3,3) | 0 |
K�smi yan�t (PR) | 34 (%28,3) | 5 (%10,6) |
Stabil hastal�k (SD) | 28 (%23,3) | 16 (%34) |
Medyan Yan�t S�resi |
| |
Ay (aral�k) | Eri�ilmedi | 3,6 (Mevcut de�ildir) |
Yan�ta kadar medyan s�re |
| |
Ay (aral�k) | 2,1 (1,6 - 7,4) | 3,5 (2,1 - 6,1) |
Elde edilen veriler, nivolumab�n ge� etki ba�lang�c�na sahip oldu�unu ve kemoterapiden sonra nivolumab yarar�n�n ortaya ��kmas�n�n 2-3 ay s�rebilece�ini g�stermi�tir.
G�ncellenmi� analiz (24 ayl�k izlem)
Randomize edilmi� t�m hastalarda ORR nivolumab grubunda %27,2 (%95 GA: 22 – 32,9),
kemoterapi grubunda ise %9,8 (%95 GA: 5,3 – 16,1) olarak belirlenmi�tir. Medyan yan�t
s�resinin s�ras�yla 31,9 ay (aral�k: 1,4+ - 31,9) ve 12,8 ay (aral�k: 1,3+ - 13,6+) oldu�u tespit edilmi�tir. Nivolumab – kemoterapi kar��la�t�rmas�na ili�kin PFS HR de�erinin 1,03 (%95
GA: 0,78 – 1,36) oldu�u belirlenmi�tir. ORR ve PFS, IRRC taraf�ndan RECIST versiyon 1.1 ile de�erlendirilmi�tir.
Nihai OS analizinde nivolumab ile kemoterapi aras�nda istatistiksel a��dan anlaml� fark g�zlenmemi�tir. Primer OS analizi, takip eden tedaviler hesaba kat�lacak �ekilde ayarlanmam��t�r ve kemoterapi kolundaki hastalar�n 54'� (%40,6) bir anti-PD1 tedavisi g�rm��t�r. Tedaviyi b�rakanlar, sonraki tedavilerin dengesizli�i ve ba�lang�� fakt�rlerindeki farkl�l�klar OS'de kar���kl��a neden olmu� olabilir. Kemoterapi kolundakilere k�yasla nivolumab kolunda bulunan daha fazla hastan�n k�t� prognostik fakt�rlere (y�ksek LDH ve beyin metastazlar�) sahip oldu�u belirlenmi�tir.
BRAF durumuna g�re etkililik:
BRAF mutasyonu-pozitif melanom g�r�len ve g�r�lmeyen hastalarda nivolumaba objektif yan�tlar (e� primer sonlan�m noktas� tan�mlamas�na g�re) g�zlenmi�tir. ORR'ler BRAF mutasyonu-pozitif alt grupta nivolumab i�in %17 (%95 GA: 8,4 – 29) kemoterapi i�in %11
(%95 GA: 2,4 – 29,2), BRAF yaban�l tip alt grupta ise s�ras�yla %30 (%95 GA: 24 – 36,7) ve
%9 (%95 GA: 4,6 – 16,7) olarak belirlenmi�tir.
Nivolumab-kemoterapi kar��la�t�rmas�na ili�kin PFS HR de�erleri BRAF mutasyonu-pozitif hastalar i�in 1,58 (%95 GA: 0,87 – 2,87), BRAF yaban�l tip hastalar i�inse 0,82 (%95 GA: 0,6 – 1,12) olarak belirlenmi�tir. Nivolumab-kemoterapi kar��la�t�rmas�na ili�kin OS HR de�erleri BRAF mutasyonu-pozitif hastalar i�in 1,32 (%95 GA: 0,75 – 2,32), BRAF yaban�l
tip hastalar i�inse 0,83 (%95 GA: 0,62 – 1,11) olarak belirlenmi�tir.
T�m�r PD-L1 ekspresyonuna g�re etkililik:
T�m�r PD-L1 ekspresyonundan ba��ms�z �ekilde nivolumaba objektif yan�tlar g�zlenmi�tir. Bununla birlikte, bu biyobelirtecin (t�m�r PD-L1 ekspresyonu) rol� tam olarak a��kl��a kavu�turulmam��t�r.
T�m�r PD-L1 ekspresyonu ≥%1 olan hastalarda ORR nivolumab i�in %33,5 (n=179; %95 GA: 26,7 - 40,9) kemoterapi i�inse %13,5 (n=74; %95 GA: 6,7 - 23,5) olarak belirlenmi�tir. T�m�r PD-L1 ekspresyonu <%1 olan hastalarda IRRC'ye g�re ORR s�ras�yla %13 (n=69;
%95 GA: 6,1 – 23,3) ve %12 (n=25; %95 GA: 2,5 – 31,2) olarak belirlenmi�tir.
Nivolumab-kemoterapi kar��la�t�rmas�na ili�kin PFS HR de�erleri t�m�r PD-L1 ekspresyonu
≥%1 olan hastalarda 0,76 (%95 GA: 0,54 – 1,07), t�m�r PD-L1 ekspresyonu <%1 olan
hastalarda ise 1,92 (%95 GA: 1,05 – 3,5) olarak belirlenmi�tir.
Nivolumab-kemoterapi kar��la�t�rmas�na ili�kin OS HR de�erleri t�m�r PD-L1 ekspresyonu
≥%1 olan hastalarda 0,69 (%95 GA: 0,49 – 0,96), t�m�r PD-L1 ekspresyonu <%1 olan
hastalarda ise 1,52 (%95 GA: 0,89 – 2,57) olarak belirlenmi�tir.
Alt gruplar�n k���k boyutu ve randomize edilmi� olan t�m pop�lasyonda OS'de istatistiksel a��dan anlaml� fark bulunmad��� g�z �n�nde bulunduruldu�unda, bu alt grup analizleri dikkatli �ekilde yorumlanmal�d�r.
A��k etiketli faz 1 doz y�kseltme �al��mas� (MDX1106-03)
Nivolumab�n g�venlili�i ve etkilili�i, malign melanom dahil �e�itli t�m�r tiplerinde yap�lan bir faz 1, a��k etiketli, doz y�kseltme �al��mas�nda de�erlendirilmi�tir. �al��maya al�nan daha �nceden tedavi g�rm�� 306 hastan�n 107'si melanom idi ve en fazla 2 y�l s�reyle 0,1 mg/kg, 0,3 mg/kg, 1 mg/kg, 3 mg/kg veya 10 mg/kg dozunda nivolumab alm��lard�r. Bu hasta pop�lasyonunda, medyan 22,9 ayl�k yan�t s�resi ile (%95 GA:17, NR) %9 (%95 GA: 2,6 -
22,1) 33 hastada (%31) objektif yan�t bildirilmi�tir. Medyan PFS s�resi 3,7 ayd� (%95 GA:
1,9 - 9,3). Medyan OS 17,3 ay (%95 GA: 12,5 – 37,8), tahmini OS oranlar� ise 3 y�lda %42
(%95 GA: 32 - 51), 4 y�lda %35 (%95 GA: 26 - 44), 5 y�lda ise %34 (%95 GA: 25 - 43) olarak
hesaplanm��t�r (minimum izlem 45 ay).
�pilimumab monoterapisine kar�� ipilimumabla kombinasyon halinde nivolumab ya da monoterapi olarak nivolumab ile randomize faz 3 �al��ma (CA209067)
�pilimumab 3 mg/kg monoterapisine kar�� ipilimumab ile kombinasyon halinde nivolumab 1 mg/kg veya nivolumab 3 mg/kg monoterapisinin ileri evre (rezeke edilemeyen ya da metastatik) melanom tedavisindeki g�venlili�i ve etkilili�i faz 3, randomize, �ift-k�r bir �al��mada de�erlendirilmi�tir (CA209067). Nivolumab i�eren iki grup aras�ndaki farklar tan�mlay�c� bir bi�imde de�erlendirilmi�tir. �al��ma, rezeke edilemeyen do�rulanm�� Evre III veya Evre IV melanomu olan yeti�kin hastalar� i�ermi�tir. Hastalar�n ECOG performans durumu puan�n�n 0 veya 1 olmas� gerekmi�tir. Rezeke edilemeyen veya metastatik melanom i�in daha �nce sistemik kanser tedavisi g�rmemi� olan hastalar �al��maya kaydedilmi�tir. Randomizasyondan en az 6 hafta �nce tamamland�ysa, �nceki adjuvan veya neoadjuvan tedaviye izin verilmi�tir. Aktif otoimm�n hastal���, ok�ler/�veal melanom veya aktif beyin veya leptomeningeal metastaz� olan hastalar �al��maya dahil edilmemi�tir.
Toplam 945 hasta; ipilimumab ile kombinasyon halinde nivolumab (n=314), nivolumab monoterapisi (n=316) ya da ipilimumab monoterapisi (n=315) almak �zere randomize edilmi�tir. Kombinasyon kolundaki hastalara ilk 4 doz boyunca her 3 haftada bir 60 dakika s�reyle nivolumab 1 mg/kg ve 90 dakika s�reyle ipilimumab 3 mg/kg uygulanm��, bunu takiben her iki haftada bir monoterapi olarak nivolumab 3 mg/kg verilmi�tir. Nivolumab monoterapi kolundaki hastalara her 2 haftada bir nivolumab 3 mg/kg uygulanm��t�r. Kar��la�t�rma kolundaki hastalara 4 doz boyunca her 3 haftada bir intraven�z yoldan ipilimumab 3 mg/kg ve nivolumabla e�le�tirilmi� plasebo uygulanm��, bunu her 2 haftada bir plasebo takip etmi�tir. Randomizasyon PD-L1 ekspresyonu (≥% 5'e kar��l�k <% 5 t�m�r h�cre membran� ekspresyonu), BRAF durumu ve Amerikan Ortak Kanser Komitesi (AJCC) evreleme sistemine g�re a�ama M'ye g�re basamakland�r�lm��t�r. Tedaviye klinik yarar g�zlenene veya tedavi art�k tolere edilemeyene kadar devam edilmi�tir. T�m�r de�erlendirmeleri randomizasyondan 12 hafta sonra, ard�ndan ilk y�l i�in her 6 haftada bir ve daha sonra her 12 haftada bir yap�lm��t�r. Yard�mc� primer sonu� �l��mleri progresyonsuz sa�kal�m ve OS idi. ORR ve yan�t s�resi de de�erlendirilmi�tir.
Ba�lang�� �zellikleri �� tedavi grubu aras�nda dengelenmi�tir. Medyan ya� 61 y�l olup (aral�k: 18 - 90), hastalar�n %65'i erkek ve %97'si beyazd�. ECOG performans durumu puan� 0 (%73) veya 1'di (%27). Hastalar�n �o�unda AJCC Evre IV hastal�k (%93); �al��maya giri�te
%58'inde M1c hastal�k mevcuttu. Hastalar�n %22'si daha once adjuvan tedavi alm��t�. Hastalar�n %32'sinde BRAF mutasyonu pozitif melanom; %26,5'inde PD-L1 ≥ %5 t�m�r h�cre membran� ekspresyonu mevcuttu. Hastalar�n %4'� beyin metastaz� �yk�s�ne ve hastalar�n %36's� �al��maya giri�te ULN'den daha y�ksek bir ba�lang�� LDH seviyesine sahipti. �l��lebilir t�m�r PD-L1 ekspresyonu olan hastalar aras�nda, hastalar�n da��l�m� �� tedavi grubunda dengelenmi�tir. T�m�r PD-L1 ekspresyonu, PD-L1 IHC 28-8 pharmDx tayini kullan�larak belirlenmi�tir.
Primer analizde (minimum takip 9 ay), nivolumab grubunda medyan PFS 6,9 ay iken ipilimumab grubunda 2,9 ayd� (HR = 0,57, %99,5 GA: 0,43, 0,76; p< 0,0001). �pilimumabla kombinasyon halindeki nivolumab grubunda medyan PFS 11,5 ay ile ipilimumab grubunda 2,9 ayd� (HR = 0,42, %99,5 GA: 0,31, 0,57; p < 0,0001)
PFS sonu�lar� (minimum 90 ayl�k takip s�resi ile) olarak �ekil 2'de (randomize edilmi� t�m pop�lasyon), �ekil 3'te (t�m�r PD-L1 %5 e�ik de�erinde) ve �ekil 4'te (t�m�r PD-L1 %1 e�ik de�erinde) g�sterilmektedir.
Progresyonsuz sa�kal�m olas�l���
�ekil 2: Progresyonsuz sa�kal�m (CA209067)
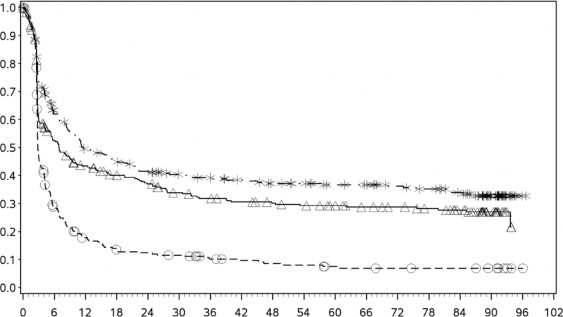
Progresyonsuz sa�kal�m (aylar)
Risk alt�ndaki g�n�ll�lerin say�s� | |||||||||||||||||
Nivolumab + ipilimumab | |||||||||||||||||
- - -* Nivolumab+ipilimumab (olaylar: 189/314), medyan ve %95 GA: 11,50 (8,90, 20,04).
12 ayda PFS oran� ve % 95 GA: %49 (44, 55), 60 ayda PFS oran� ve % 95 GA: %36 (32,
42), 90 ayda PFS oran� % 95 GA: %33 (27,39)
──∆─── Nivolumab (olaylar: 208/316), medyan ve %95 GA: 6,93 (5,13; 10,18)
12 ayda PFS oran� ve % 95 GA: %42 (36, 47), 60 ayda PFS oran� ve % 95 GA: %29 (24,
35), 90 ayda PFS oran� % 95 GA: %27 (22,33)
- - - �pilimumab (olaylar: 261/315), medyan ve %95 GA: 2,86 (2,79, 3,09).
12 ayda PFS oran� ve % 95 GA: %18 (14, 23), 60 ayda PFS oran� ve % 95 GA: %8 (5,
12), 90 ayda PFS oran� ve %95 GA CI: %7 (4,11)
�pilimumab kar��s�nda nivolumab+ipilimumab -tehlike oran� ve %95 GA: 0,42 (0,35, 0,51)
�pilimumab kar��s�nda nivolumab -tehlike oran� ve %95 GA: 0,53 (0,44, 0,64)
Nivolumab kar��s�nda nivolumab+ipilimumab - tehlike oran� ve %95 GA: 0,79 (0,65, 0,97)
�pilimumaba (primer analiz) kar�� Nivolumab+�pilimumab - HR (%99,5 GA): 0,42 (0,32-0,56); p- de�eri: < 0,0001
�pilimumaba kar�� Nivolumab (primer analiz) - HR (%99,5 GA): 0,55 (0,42-0,73); p-de�eri: < 0,0001 Nivolumaba kar�� Nivolumab+�pilimumab (tan�mlay�c� analiz) - HR (%95 GA): 0,76 (0,62-0,95)
�ekil 3: PD-L1 ekspresyonuna g�re progresyonsuz sa�kal�m: %5 e�ik (CA209067)
Progresyonsuz sa�kal�m olas�l���
PD L1 ekspresyonu < %5
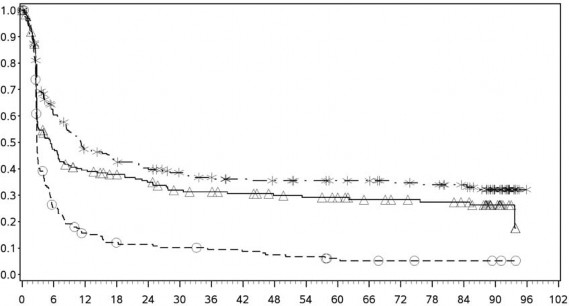
Progresyonsuz sa�kal�m (aylar)
Risk alt�ndaki g�n�ll�lerin say�s� |
Nivolumab + ipilimumab |
- - -*- - - - Nivolumab+ipilimumab (olaylar: 127/210), medyan ve %95 GA: 11,17 (7,98, 17,51)
──∆─── Nivolumab (olaylar: 139/208), medyan ve %95 GA: 5,39 (2,96, 7,13)
- - -- - - �pilimumab (olaylar: 171/202), ), medyan ve %95 GA: 2,79 (2,76, 3,02)
�pilimumab kar��s�nda nivolumab+ipilimumab tehlike oran� ve %95 GA: 0,42 (0,33, 0,53)
�pilimumab kar��s�nda nivolumab - tehlike oran� ve %95 GA: 0,54 (0,43, 0,68)
Nivolumab kar��s�nda nivolumab +ipilimumab tehlike oran� ve %95 GA: 0,77 (0,61, 0,98)
Progresyonsuz sa�kal�m olas�l���
PD-L1 ekspresyonu ≥ %5
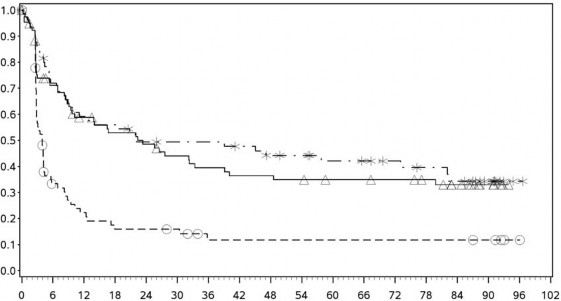
Progresyonsuz sa�kal�m (aylar)
Risk alt�ndaki g�n�ll�lerin say�s� | |||||||||||||||||
Nivolumab + ipilimumab |
|
|
|
|
|
|
|
|
|
|
|
|
|
| |||
- -* Nivolumab+ipilimumab (olaylar: 36/68), medyan ve %95 GA: 22,11 (9,72, 82,07)
──∆─── Nivolumab (olaylar: 48/80), medyan ve %95 GA: 22,34 (9,46, 39,13)
5.2. Farmakokinetik �zellikler
Genel �zelliklerEmilim:
Yeterli veri mevcut de�ildir.
Da��l�m:
Yeterli veri mevcut de�ildir.
Biyotransformasyon:
Nivolumab�n metabolik yola�� karakterize edilmemi�tir. Tamamen insan IgG4 monoklonal antikoru olan nivolumab�n, endojen IgG ile ayn� �ekilde katabolik yolaklar arac�l���yla k���k peptidlere ve amino asitlere bozunmas� beklenmektedir.
Eliminasyon:
Nivolumab�n klirensi (CL) zaman i�inde azalmaktad�r ve ba�lang�� de�erlerine g�re meydana gelen ortalama maksimal azalma (% varyasyon katsay�s� [%CV]) %26'd�r (%32,6) ve bu, metastatik t�m�rlere sahip hastalarda 7,91 mL/saatlik (%46) bir geometrik ortalama kararl� durum klirensi (CLss) (%CV) ortaya ��karmaktad�r; CLss'deki d���� klinik a��dan anlaml� kabul edilmemektedir. Kararl� durumda metastatik melanom hastalar�ndakine k�yasla melanomun tamamen rezeke edilmi� oldu�u hastalarda geometrik ortalama pop�lasyon klirensi %24 daha d���k oldu�undan, bu hastalarda nivolumab�n klirensi zaman i�inde azalmamaktad�r. Kararl� durumda geometrik ortalama da��l�m hacmi (Vd) (%CV) 6,6 L'dir (%24,4), geometrik ortalama eliminasyon yar� �mr� ise (t1/2) 25 g�nd�r (%55,4). 2 haftada bir 3 mg/kg dozunda uyguland���nda nivolumab�n kararl� durum konsantrasyonlar�na 12. haftada ula��lm��t�r ve sistemik birikim yakla��k 4 kat olmu�tur.
30 dakikal�k bir inf�zyonun ard�ndan �ng�r�len nivolumab maruziyeti 60 dakikal�k bir inf�zyonun ard�ndan g�zlenenle kar��la�t�r�labilir niteliktedir.
Nivolumab�n klirensi (CL) artan v�cut a��rl��� ile birlikte artm��t�r. V�cut a��rl���na g�re normalize edilmi� doz, geni� bir v�cut a��rl��� aral���nda (34-162 kg), a�a�� yukar� tek d�ze bir kararl� durum dip konsantrasyonu ortaya ��karm��t�r.
Do�rusall�k/Do�rusal Olmayan Durum:
Nivolumab�n farmakokineti�i 0,1 ila 10 mg/kg'l�k doz aral���nda do�rusald�r.
cHL hastalar�nda nivolumab CL, KHDAK'ne g�re yakla��k %32 daha d���k olmu�tur. Adjuvan Melanom hastalar�nda, ilerlemi� melanoma k�yasla nivolumab ba�lang�� CL yakla��k
%40 daha d���kt� ve kararl� durum CL yakla��k %20 daha d���kt�. Mevcut g�venlilik verilerine g�re, CL'deki bu azalmalar klinik olarak anlaml� de�ildi.
�pilimumab ile kombinasyon halinde OPDIVO:
Nivolumab 1 mg/kg, ipilimumab 3 mg/kg ile kombinasyon halinde uyguland���nda, nivolumab CL de�eri %29, ipilimumab CL de�eri %9 artm�� ve bu art�� klinik olarak anlaml� kabul edilmemi�tir. Nivolumab 3 mg/kg, ipilimumab 1 mg/kg ile kombinasyon halinde uyguland���nda, nivolumab CL de�eri %1 artm�� ve ipilimumab CL de�eri %1,5 azalm�� ve bu de�i�iklikler klinik olarak anlaml� g�r�lmemi�tir.
�pilimumab ile kombinasyon halinde uyguland���nda, nivolumab�n CL de�eri anti-nivolumab antikorlar�n�n varl���nda %20 artm�� ve ipilimumab�n CL de�eri anti-ipilimumab
antikorlar�n�n varl���nda %5,7 artm��t�r. Bu de�i�iklikler klinik olarak anlaml� kabul edilmemi�tir.
�pilimumab ve kemoterapi ile kombinasyon halinde OPDIVO:
3 haftada bir nivolumab 360 mg, 6 haftada bir ipilimumab 1 mg/kg ve 2 k�r kemoterapi ile kombinasyon halinde uyguland���nda, nivolumab CL de�eri yakla��k %10 d��m�� ve ipilimumab CL de�eri yakla��k %22 artm�� ve bu art�� klinik olarak anlaml� kabul edilmemi�tir.
Hastalardaki karakteristik �zellikler:
Pop�lasyon FK analizinde nivolumab CL'sinde ya�, cinsiyet, �rk, solid t�m�r tipi, t�m�r boyutu ve hepatik yetmezli�e dayanarak herhangi bir fark tespit edilmemi�tir. ECOG durumu, ba�lang�� glomer�ler filtrasyon h�z� (GFR), alb�min, kilo ve hafif karaci�er yetmezli�i nivolumab CL'sini etkilese de, bu etki klinik olarak anlaml� de�ildi.
Nivolumab�n klasik Hodgkin lenfoma hastalar�ndaki CL'sinin KHDAK'li hastalardakine k�yasla yakla��k %32 daha d���k oldu�u belirlenmi�tir. Mevcut g�venlilik verileri g�z �n�nde bulunduruldu�unda CL'deki bu azalma klinik a��dan anlaml� g�r�lmemi�tir.
B�brek yetmezli�i
Pop�lasyon FK analizlerinde b�brek yetmezli�inin nivolumab CL'si �zerindeki etkisi normal b�brek fonksiyonuna sahip olan hastalara k�yasla (GFR ≥ 90 mL/dakika/1,73 m2; n = 342) hafif (GFR < 90 ve ≥ 60 mL/min/1,73 m2; n = 379), orta (GFR < 60 ve ≥ 30 mL/min/1.73 m2; n = 179) veya �iddetli (GFR < 30 ve ≥ 15 mL/dak/1,73 m2; n = 2) b�brek yetmezli�i olan hastalarda de�erlendirilmi�tir. Hafif veya orta �iddetli b�brek yetmezli�i olan hastalarla normal b�brek fonksiyonuna sahip hastalar aras�nda nivolumab CL'sinde klinik olarak anlaml� farklar tespit edilmemi�tir. �iddetli b�brek yetmezli�i olan hastalardan elde edilen veriler, bu pop�lasyonla ilgili bir sonu� ��karamayacak kadar s�n�rl�d�r (bkz. B�l�m 4.2).
Karaci�er yetmezli�i
Bir pop�lasyon FK analizinde karaci�er yetmezli�inin nivolumab CL'si �zerindeki etkisi normal karaci�er fonksiyonuna sahip hastalara k�yasla (toplam bilirubin ve AST ≤ ULN; n = 804) hafif karaci�er yetmezli�i (Ulusal Kanser Enstit�s�n�n hepatik fonksiyon bozuklu�u kriterleri kullan�larak tan�mland��� �ekilde toplam bilirubin > 1 × ila 1,5 × ULN veya AST > ULN; n = 92) olan hastalarda de�erlendirilmi�tir. Hafif karaci�er yetmezli�i olan hastalarla normal karaci�er fonksiyonuna sahip hastalar aras�nda nivolumab CL'sinde klinik olarak anlaml� farklar tespit edilmemi�tir. Nivolumab, orta (toplam bilirubin > 1,5 × ila 3 × �st normal s�n�r [ULN] ve herhangi bir AST) veya �iddetli (toplam bilirubin > 3 × ULN ve herhangi bir AST) karaci�er yetmezli�i olan hastalarda ara�t�r�lmam��t�r (bkz. B�l�m 4.2).
5.3. Klinik �ncesi g�venlilik verileri
6. FARMAS�T�K �ZELL�KLER
6.1. Yard�mc� maddelerin listesi
Sodyum sitrat dihidrat Sodyum klor�r Mannitol (E421) Pentetik asit Polisorbat 80
Sodyum hidroksit (pH ayarlamas� i�in) Hidroklorik asit (pH ayarlamas� i�in) Enjeksiyonluk su
6.2. Ge�imsizlikler
Ge�imlilik �al��malar� yap�lmad���ndan, bu t�bbi �r�n di�er t�bbi �r�nlerle kar��t�r�lmamal�d�r. OPDIVO, di�er ajanlarla ayn� intraven�z hatta ayn� zamanda inf�ze edilmemelidir.
6.3. Raf �mr�
A��lmam�� flakon:
36 ay
A��ld�ktan sonra:
Mikrobiyolojik nedenlerle, a��lan t�bbi �r�n derhal inf�ze edilmeli ya da seyreltilerek inf�ze edilmelidir.
Hemen kullan�lmamas� halinde OPDIVO'nun ���ktan korundu�unda 2ºC ila 8ºC'de kimyasal ve fiziksel kullan�m i�i stabilitesinin 24 saat, oda ����� alt�nda 20°C-25°C'de ise en fazla 8 saat oldu�u g�sterilmi�tir (toplam 24 saatlik s�renin bu 8 saatlik periyoduna �r�n�n uyguland��� periyod dahildir).
6.4. Saklamaya y�nelik �zel tedbirler
Buzdolab�nda saklay�n�z (2°C - 8°C). Dondurmay�n�z.
I��ktan korumak i�in orijinal ambalaj�nda saklay�n�z.
Haz�rlanan ��zeltinin saklama ko�ullar� i�in b�l�m 6.3'e bak�n�z.
6.5. Ambalaj�n niteli�i ve i�eri�i
Bir t�pas� (b�til kau�uk) ve koyu mavi ge�me kapa�� (al�minyum) olan 10 mL flakonda (Tip 1 cam) 4 mL konsantre. Ambalaj boyutu 1 flakon.
6.6. Be�eri t�bbi �r�nden arta kalan maddelerin imhas� ve di�er �zel �nlemler
Kullan�lmam�� olan �r�nler ya da at�k materyaller “T�bbi At�klar�n Kontrol� Y�netmeli�i” ve “Ambalaj At�klar�n�n Kontrol� Y�netmelikleri”ne uygun olarak imha edilmelidir.
Haz�rlama a�amas�, �zellikle asepsi ile ilgili, iyi uygulamalara ili�kin kurallara uygun olarak, e�itimli personel taraf�ndan ger�ekle�tirilmelidir.
Haz�rlama ve uygulama Dozun hesaplanmas� Nivolumab monoterapisi:
Hasta i�in re�ete edilen doz mg/kg cinsinden verilir. Re�ete edilen bu doza dayan�larak uygulanacak toplam doz hesaplan�r. Hastaya tam doz uygulanabilmesi i�in birden fazla OPDIVO flakonu gerekli olabilir.
Mg olarak toplam OPDIVO dozu = kg olarak hastan�n a��rl��� x mg/kg olarak re�ete edilen doz.
 Ruh ve Ak�l Sa�l���m�z� Geli�tirmek
�yi ak�l ve ruh sa�l��� sahip olmaktan ziyade, yapt���n�z �eylerdir. Ak�l ve
ruhsal olarak sa�l�kl� olmak i�in kendinize de�er vermeli ve kendinizi kabul
etmelisiniz.
Ruh ve Ak�l Sa�l���m�z� Geli�tirmek
�yi ak�l ve ruh sa�l��� sahip olmaktan ziyade, yapt���n�z �eylerdir. Ak�l ve
ruhsal olarak sa�l�kl� olmak i�in kendinize de�er vermeli ve kendinizi kabul
etmelisiniz. |
 Deri Kanseri
Deri kanseri �ok rastlanan bir hastal�kt�r. �� ana t�r� bulunur ;genelde kemirici �lser olarak bilinen bazal h�creli karsinom, yass� h�creli karsinom ve k�t� huylu t�m�r.
Deri Kanseri
Deri kanseri �ok rastlanan bir hastal�kt�r. �� ana t�r� bulunur ;genelde kemirici �lser olarak bilinen bazal h�creli karsinom, yass� h�creli karsinom ve k�t� huylu t�m�r. |
 |
Do�um Sonras� Depresyonu Do�um sonras� depresyonu, do�umdan sonra her on kad�ndan biri taraf�ndan tecr�be edilen stresli bir durumdur. |
 |
Depresyonu Anlamak Depresyon farkl� ki�ileri farkl� bi�imlerde etkiler. Duygusal veya fiziksel olmak �zere geni� alanda belirtilere sebep olabilir.Depresyona neler sebep olur? |
 |
Parkinson Hastal��� Hastal�k ilk kez 1817 de �ngiliz doktor James Parkinson taraf�ndan tan�mlanm�� ve Dr. Parkinson hastal��� “sallay�c� fel�” olarak kaleme alm��. |
�LA� GENEL B�LG�LER�
Bristol-Myers Squibb �la�lar� Inc.
| Geri �deme Kodu | A16775 |
| Sat�� Fiyat� | 12322.69 TL [ 22 Apr 2024 ] |
| �nceki Sat�� Fiyat� | 12322.69 TL [ 15 Apr 2024 ] |
| Original / Jenerik | Original �la� |
| Re�ete Durumu | Normal Re�eteli bir ila�d�r. |
| Barkodu | 8699726765007 |
| Etkin Madde | Nivolumab |
| ATC Kodu | L01XC17 |
| Birim Miktar | 40/4 |
| Birim Cinsi | MG/ML |
| Ambalaj Miktar� | 1 |
| Antineoplastik ve �mm�nomod�lat�r Ajanlar > Di�er Kanser �la�lar� |
| �thal ( ref. �lke : Porto riko ) ve Be�eri bir ila�d�r. |