CLENID 80 mcg inhilasyon i�in �l��l� dozlu aerosol 120 doz K�sa �r�n Bilgisi
{ Siklesonid }
1. BE�ER� TIBB� �R�N�N ADI
CLEN�D 80 mcg inhalasyon i�in �l��l� dozlu aerosol
2. KAL�TAT�F VE KANT�TAT�F B�LE��M
Etkin madde
1 uygulama (a��z k�sm�ndan ��kan doz):
Siklesonid 80 mikrogram
Yard�mc� maddeler
Yard�mc� maddeler i�in B�l�m 6.1'e bak�n�z.
3. FARMAS�T�K FORMU
�nhalasyon i�in �l��l� dozlu aerosol.
Al�minyum inhaler kab� i�inde bas�n�l� propellant gaz ile doldurulmu� s�spansiyon. Al�minyum konteynere bir dozajlama valf eklidir.
�nhalasyon spreyinizi ba� parma��n�z a��zl���n alt�nda, inhalasyon spreyinizin taban�nda olacak �ekilde dik tutunuz.
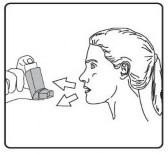
Kuru bir bez veya kuma� ile a��zl���n i�ini ve d���n� ve plastik g�vdeyi siliniz.
4. KL�N�K �ZELL�KLER
4.1. Terap�tik endikasyonlar
Ast�m�n t�m basamaklar�nda antienflamatuar, bronkodilat�r, semptom kontrol� ve oral steroid ihtiyac�n� azaltmak ama�l� kullan�l�r.
KOAH'ta tek ba��na kullan�lmas� �nerilmez.
4.2. Pozoloji ve uygulama �ekli
Pozoloji:Yeti�kinler:
CLEN�D'in �nerilen ba�lang�� dozu g�nde 1 kez uygulanan 160 mikrogramd�r. Bununla birlikte 12 haftal�k bir �al��mada, 640 mikrogram/g�n dozunun (g�nde iki kez 320 mikrogram) �iddetli ast�mlarda alevlenme s�kl���n� azaltt���, ancak akci�er fonksiyonlar�n� iyile�tirmedi�i g�r�lm��t�r (Bkz. B�l�m 5.1) Baz� hastalar i�in etkin idame dozu olarak g�nde 1 kez 80 mikrogram da tercih edilebilir.
Uygulama s�kl��� ve s�resi:
G�nde bir kez sabah veya ak�am kullan�l�r. Hastalar�n CLEN�D'i g�n�n hangi saatinde (ak�am ya da sabah) kullanacaklar� konusundaki son karar hekim taraf�ndan belirlenmelidir.
Hastal�k semptomlar� CLEN�D ile tedaviye ba�land�ktan sonraki ilk 24 saat i�inde d�zelmeye ba�lar. Ast�m kontrol alt�na al�nd�ktan sonra CLEN�D'in dozu hastan�n bireysel durumuna g�re �ekillendirilir ve hastal���n iyi bir �ekilde kontrol edilebilece�i minimum idame dozu tercih edilir.
Ast�m yak�nmalar� �iddetli olan hastalarda akut atak riski mevcut olup bu hastalar�n akci�er fonksiyon testleri de dahil olmak �zere muayenelerini d�zenli �ekilde s�rd�rmeleri gerekir. Ast�m semptomlar�n� gidermeye y�nelik k�sa etkili bronkodilat�r kullan�m�n�n art��� hastal���n
kontrol�nde bozulma oldu�una i�aret eder. K�sa etkili bronkodilat�r kullan�m�n�n hastaya sa�lad��� rahatlama azalm�� ise ya da eskisinden daha fazla say�da inhalasyona ihtiyac� s�z konusu olmaya ba�lad�ysa hekime ba�vurulmas� zorunludur.
Bu durumda hastan�n antiinflamatuar tedavinin artt�r�lmas� y�n�ndeki ihtiyac� g�z �n�nde bulundurularak tekrar de�erlendirilmesi gerekir (�rn. CLEN�D dozunun artt�r�lmas� ya da oral kortikosteroid tedavisine ge�ilmesi). Ciddi ast�m alevlenmeleri ola�an �ekilde tedavi edilmelidir.
Uygulama �ekli:
CLEN�D, sadece inhalasyon yolu ile uygulan�r.
�nhaler cihaz�n� aktive ederken e�zamanl� olarak nefes alma i�levini ayarlamada zorlanan hastalar�n ihtiya�lar� da g�z ard� edilmemelidir; bu gibi durumlarda CLEN�D uygun bir hava odac��� (spacer) yard�m� ile kullan�labilmektedir.
Kullan�m i�in �neriler:
�nhaler uygulamas�n� do�ru bir �ekilde yapabilmesi i�in hastan�n bu konuda bilgilendirilmeye ihtiyac� vard�r.
E�er CLEN�D kutusundan ilk kez ��kart�l�p kullan�lacaksa ya da 1 haftadan daha uzun bir s�redir hi� kullan�lmam��sa, a��z i�ine uygulama yapmadan �nce havaya do�ru 3 kez p�sk�rt�lmelidir. Sol�syon yap�da bir aerosol oldu�undan kullan�m �ncesinde �alkalanmas� gerekmez.
�nhalasyon s�ras�nda hastan�n tercihen oturmas� ya da ayakta durmas� gerekir; inhaler dik olarak tutulmal� ve ba�parmak ile a��zl�k k�sm�n�n alt�ndan kavranmal�d�r.
Hastaya cihaz�n a��zl�k k�sm�n�n kapa��n�n yerinden ��kart�lmas�, ard�ndan cihaz�n a��zl�k k�sm�n�n kendi a�z�na uygun �ekilde konumland�r�lmas� ve dudaklar taraf�ndan kavrand�ktan sonra yava��a ve derin bir �ekilde soluk almas� ��retilir. A��z yolundan ger�ekle�en soluk alma esnas�nda i�aret parma�� ile inhaler cihaz�n�n tepesinden 1 kez bas�l�r. Bu i�lemin ard�ndan hasta inhaler cihaz�n� a��zdan ��kart�r ancak alm�� oldu�u solu�u yakla��k 10 saniye boyunca d��ar� vermeden beklemesi gerekir. Akci�erlerdeki havan�n tekrar inhaler cihaz�na do�ru �flenmesi gerekmez. Hasta nefesini yava��a d��ar�ya vererek cihaz�n a��zl�k k�sm�n�n kapa��n� kapat�r.
Cihaz�n a��zl�k k�sm�n�n temizli�i kuru bir bez ile silmek suretiyle haftada 1 kez yap�lmal�d�r. �nhaler y�kanmamal� ve su ile temas ettirilmemelidir.
�zel pop�lasyonlara ili�kin ek bilgiler:
B�brek/Karaci�er yetmezli�i:
Karaci�er yetmezli�i olan hastalarda doz ayarlamas� gerekmez.
Ancak, a��r karaci�er yetmezli�i ve b�brek yetmezli�inde ila� dozuna ili�kin yeterli veri bulunmamaktad�r.
Pediyatrik pop�lasyon:
Siklesonidin 6 ya� alt�ndaki �ocuklar�n tedavisinde kullan�m�na ili�kin veriler yeterli olmad���ndan bu ya� grubuna �nerilmez. CLEN�D, 12 ya� alt�ndaki �ocuklarda kullan�lmamal�d�r.
Geriyatrik pop�lasyon:
Ya�l� hastalarda doz ayarlamas� gerekmez.
4.3. Kontrendikasyonlar
CLEN�D, siklesonide ve i�eri�indeki bile�enlerden herhangi birine kar�� a��r� duyarl�l��� oldu�u bilinen ki�ilerde kontrendikedir.
Di�er t�m inhale kortikosteroidler gibi, CLEN�D de, aktif veya semptomsuz akci�er t�berk�lozu olan ya da fungal, vir�tik veya bakteriyel enfeksiyonu bulunan hastalarda kontrendikedir.
4.4. �zel kullan�m uyar�lar� ve �nlemleri
Di�er t�m inhale kortikosteroidler gibi, CLEN�D de, status astmatikus ve di�er yo�un bak�m gerektiren acil durumlar�n tedavisinde endike de�ildir.
Di�er t�m inhale kortikosteroidler gibi, CLEN�D de, inhale k�sa etkili bir bronkodilat�r�n gerekli oldu�u akut ast�m semptomlar�n�n giderilmesi amac�yla kullan�lamaz. Hastalara bu gibi acil durumlara uygun ila�lar� haz�r bulundurmalar� gerekti�i konusunda bilgi verilmelidir.
�nhale kortikosteroidlerin �zellikle y�ksek dozda ve uzun s�reli kullan�mlar�nda sistemik etkileri ortaya ��kabilmektedir. Ancak, oral yoldan kullan�lan kortikosteroidlere k�yasla bu gibi durumlar�n meydana gelme ihtimali �ok daha azd�r. Olas� sistemik etkilerin aras�nda b�brek �st� bezi salg�s�nda azalma, �ocuk ve gen� ergenlerde b�y�me gerili�i, kemik mineral yo�unlu�unda azalma, katarakt ve glokom gibi durumlar yer almaktad�r. Bu y�zden inhale kortikosteroid dozunun ast�m kontrol�n� sa�layabilen en d���k etkin dozuna ayarlanm�� olmas� �nem ta��maktad�r.
�nhale kortikosteroidlerle uzun s�re tedavi olan �ocuklar�n ve ergenlik �a��ndaki hastalar�n boylar�n�n d�zenli olarak �l��lmesi �nerilir. E�er b�y�me yava�sa, inhale kortikosteroid dozunun ast�m� kontrol alt�na alabilecek etkili en d���k doza azalt�lmas� amac�yla tedavi tekrar d�zenlenmelidir.
Herhangi bir giri�im �ncesinde bu hastalar�n b�brek �st� bezi yetersizli�i a��s�ndan uzman g�zetimine al�nmas� gerekebilir. B�brek �st� bezindeki bozulman�n kal�nt�lar� olabilece�i g�z �n�ne al�narak t�bbi ya da cerrahi aciller veya stres olu�turan planl� giri�imler s�z konusu oldu�unda bu hastalara uygun kortikosteroid tedavisine ba�lanmal�d�r.
Oral kortikosteroid kullanan hastalarda inhale siklesonid tedavisine ge�ilmesi hakk�nda:
Oral steroid ba��ml� hastalar�n siklesonid tedavisine ge�ilmesi ve bu hastalar�n daha sonraki tedavileri �zel bak�m gerektirir; ��nk� uzun s�ren sistemik kortikosteroid kullan�m� nedeniyle b�brek �st� bezi fonksiyonlar�ndaki bozuklu�un iyile�mesi uzun zaman alabilir.
Uzun s�redir ya da y�ksek dozda sistemik steroid kullanm�� olan hastalar�n b�brek �st� bezi fonksiyonlar� bask�lanm�� olabilir. Bu hastalar�n b�brek �st� bezi fonksiyonlar� d�zenli olarak kontrol edilerek, kulland�klar� sistemik steroidin dozu dikkatle azalt�lmal�d�r.
Sistemik steroidin kademeli bir �ekilde b�rak�lmas� amac�yla mevcut doz her hafta 1 mg prednizolon veya di�er t�revlerin buna e�de�er olacak miktar� �eklinde hesaplanarak azaltma s�reci ba�lat�l�r. Prednizolon idame dozunun g�nl�k 10 mg'� a�t��� olgularda daha b�y�k dilimler halinde haftal�k azal��lar da uygun olabilir.
Baz� hastalar bu kademeli b�rakma a�amalar�nda solunum fonksiyonlar� de�i�medi�i ve hatta d�zeldi�i halde kendilerini bir �ekilde k�t� hissetmektedir. Bu gibi hastalar� e�er b�brek �st� bezi yetmezli�ine ait objektif bulgular� yoksa, inhale siklesonid kullanmaya ve de sistemik steroid tedavisini b�rakmaya azimle devam etmeleri konusunda cesaretlendirmek gerekir.
B�brek �st� fonksiyonlar� hala d�zelmemi� olan oral steroid tedaviden inhale siklesonid tedavisine ge�ilmi� hastalar�n stres d�nemlerinde (�rn. ast�m ataklar�n�n s�kla�mas�, torakal enfeksiyonlar, araya giren ciddi hastal�k, cerrahi giri�im, travma, vb.) ilave sistemik steroid kullanmalar�n�n gerekli oldu�unu belgeleyen uyar�/bilgi kartlar�n� ta��malar� gerekir.
Sistemik steroid tedavisinin yerine inhale tedavinin ba�lat�lmas� bazen alerjik rinit ya da egzama gibi evvelce sistemik ila� ile kontrol edilmi� bulunan alerjileri a���a ��karabilir.
�nhale kortikosteroid uygulamas�n�n hemen ard�ndan artan h�r�lt�l� solunum gibi paradoksal bronkospazm ve bronkospazm�n di�er semptomlar� genellikle h�zl� �ifa sa�layan inhale k�sa etkili bronkodilat�r ile tedavi edilmelidir. Hasta muayene edilip de�erlendirilmeli ve CLEN�D tedavisi ancak beklenen faydan�n olas� riski a�mas� halinde s�rd�r�lmelidir. Ast�m tablosunun ciddiyeti ile akut bron�iyal reaksiyonlar�n sebep oldu�u genel hassasiyet art��� aras�ndaki ilinti g�z �n�nde bulundurulmal�d�r (Bkz. B�l�m 4.8).
KOAH hastalar�nda pn�moni
Kortikosteroid i�eren inhale ila�lar� alan KOAH hastalar�nda, hastaneye yat�� gerektiren pn�moni dahil pn�moni insidans�nda art�� g�zlemlenmi�tir. Artan steroid dozu ile pn�moni riskinde art�� kan�tlar� bulunmaktad�r, ancak bu durum �al��malar�n tamam�nda kesin olarak g�sterilmemi�tir.
Kortikosteroid i�eren inhale ila�lar�n�n pn�moni riskinin b�y�kl��� konusunda s�n�f i�i farkl�l�k i�in kesin klinik kan�t bulunmamaktad�r.
Hekimler, KOAH hastalar�nda olas� pn�moni geli�imine kar��, enfeksiyonlar�n klinik �zellikleri ile KOAH semptomlar�n�n alevlenme durumunun kar��mas� ihtimali dolay�s�yla dikkatli olmal�d�rlar.
KOAH hastalar�ndaki pn�moni risk fakt�rleri aras�nda; sigara i�imi, ileri ya�, d���k v�cut kitle indeksi ve �iddetli KOAH bulunmaktad�r.
4.5. Di�er t�bbi �r�nler ile etkile�imler ve di�er etkile�im �ekilleri
CYP3A4, in vitro verilere g�re, siklesonidin aktif metaboliti olan M1'in metabolizmas�ndan sorumlu en �nemli enzimdir.
Siklesonid ve aktif metaboliti olan M1'in serum d�zeyleri d���kt�r. Ancak, CYP3A4 sisteminin g��l� inhibit�rlerinin (�rne�in itrakonazol, ritonavir ya da nelfinovir) e� zamanl� olarak kullan�m�, siklesonid/M1 d�zeylerinde artmaya neden olabilir. Klinik a��dan �nemli olabilecek istenmeyen etki riski g�zard� edilmemelidir.
4.6. Gebelik ve laktasyon
Gebelik kategorisi C.
�ocuk do�urma potansiyeli bulunan kad�nlar/Do�um kontrol� (Kontrasepsiyon)
Hen�z gebe kad�nlarda yap�lm�� yeterli ve iyi kontrol edilmi� �al��ma mevcut de�ildir.
Hayvan �al��malar�nda glukokortikoidlerin malformasyonlara sebep oldu�u g�sterilmi�tir.
(Bkz. B�l�m 5.3). Ancak, bu sonu�lar�n insanlara �nerilen dozlarda olu�abilmesi m�mk�n g�r�nmemektedir.
Di�er glukokortikoidler gibi, siklesonidi de gebelik s�ras�nda ancak fet�s i�in olan potansiyel riskinin anneye sa�lad��� potansiyel fayda taraf�ndan kar��lanmas� durumunda kullanmak gerekir. Yeterli ast�m kontrol�n� sa�layabilen en d���k etkin siklesonid dozu kullan�lmal�d�r. Gebeli�i s�ras�nda kortikosteroid kullanm�� olan annelerin bebekleri, hipoadrenalizm a��s�ndan dikkatle izlenmelidir.
Gebelik d�nemi
Di�er glukokortikoidler gibi, siklesonidi de gebelik s�ras�nda ancak fet�s i�in olan potansiyel riskinin anneye sa�lad��� potansiyel fayda taraf�ndan kar��lanmas� durumunda kullanmak gerekir. Yeterli ast�m kontrol�n� sa�layabilen en d���k etkin siklesonid dozu kullan�lmal�d�r.
Laktasyon d�nemi
�nhale siklesonidin anne s�t�ne ge�i�i hakk�nda bilgi mevcut de�ildir. Bebe�ini emziren annelere siklesonid tedavisine ancak anneye sa�layaca�� faydan�n bebe�e getirece�i olas� riski a�mas� durumunda ba�lanmal�d�r.
�reme yetene�i/Fertilite
Yeterli klinik veriye ula��lamamaktad�r.
4.7. Ara� ve makine kullan�m� �zerindeki etkiler
Siklesonid inhalasyonunun ara� ve makine kullanma yetene�i �zerinde etkisi yoktur ya da ihmal edilebilecek d�zeydedir.
4.8. �stenmeyen etkiler
Siklesonidin ve siklesonid ile tedavi edilen hastalarda bildirilen reaksiyonlar� i�eren istenmeyen etkilerin s�kl��� a�a��da listelenmi�tir. Siklesonid ile g�zlemlenen etkiler genellikle doz veya konsantrasyona ba�l�d�r.
�stenmeyen etkiler a�a��daki kategorilere g�re listelenmi�tir:
�ok yayg�n : ≥ 1/10
Yayg�n : ≥ 1/100 ila < 1/10
Yayg�n olmayan : ≥ 1/1.000 ila < 1/100 Seyrek : ≥ 1/10.000 ila < 1/1.000
�ok seyrek : < 1/10.000
Bilinmiyor : Eldeki verilerden hareketle tahmin edilemiyor.
Enfeksiyonlar ve enfestasyonlar
Yayg�n : Pn�moni (KOAH'l� hastalarda) Yayg�n olmayan : Oral mantar enfeksiyonlar�*
Ba����kl�k sistemi hastal�klar�
Seyrek: Anjiyo�dem, hipersensitivite
Psikiyatrik hastal�klar
Bilinmiyor : Psikomotor hiperaktivite, uyku bozukluklar�, anksiyete, depresyon, agresyon, davran�� de�i�iklikleri
Sinir sistemi hastal�klar�
Yayg�n olmayan : Ba� a�r�s�*
Kardiyak hastal�klar
Seyrek : Palpitasyonlar**
Vask�ler hastal�klar
Seyrek : Hipertansiyon
Solunum, g���s bozukluklar� ve mediastinal hastal�klar
Yayg�n olmayan : Paradoksikal bronkospazm*, inhalasyon sonras� �ks�r�k*, disfoni
Gastrointestinal hastal�klar
Yayg�n olmayan : Bulant�*, kusma*, k�t� tat Seyrek : Kar�n a�r�s�*, dispepsi*
Deri ve deri alt� doku hastal�klar�
Yayg�n olmayan : Egzama, d�k�nt�
Genel bozukluklar ve uygulama b�lgesine ili�kin hastal�klar
Yayg�n olmayan : Uygulama b�lgesinde reaksiyon ve kuruluk
(*) Plasebo ile kar��la�t�r�ld���nda benzer veya daha d���k insidans
(**) Klinik �al��malarda, �o�unlukla bilinen kardiyak etkileri olan ila�larla (�rn: teofilin veya salbutamol) birlikte kullan�ld��� durumlarda, hangisinden kaynakland��� belli olmayan palpitasyonlar meydana gelmi�tir.
Uygulamadan hemen sonra, t�m inhale ila�larda olan non-spesifik akut bir reaksiyon olarak, etkin madde, yard�mc� madde veya �l��l� doz inhalerlerde buhar so�umas�ndan kaynaklanabilen paradoksikal bronkospazm meydana gelebilir. Ciddi durumlarda CLEN�D tedavisinin durdurulmas� d���n�lmelidir.
�nhale kortikosteroidlere ba�l� sistemik etkiler �zellikle y�ksek dozda ve uzun s�reli kullan�m s�z konusu oldu�unda olu�abilmektedir. Olas� sistemik etkiler aras�nda Cushing sendromu, cushingoid �zellikler, adrenal supresyon, adolesanlarda b�y�mede gecikme, kemik mineral yo�unlu�unda azalma, katarakt, glokom say�labilir (Ayr�ca Bkz. B�l�m 4.4.).
��pheli advers reaksiyonlar�n raporlanmas�
Ruhsatland�rma sonras� ��pheli ila� advers reaksiyonlar�n�n raporlanmas� b�y�k �nem ta��maktad�r. Raporlama yap�lmas�, ilac�n yarar / risk dengesinin s�rekli olarak izlenmesine olanak sa�lar. Sa�l�k mesle�i mensuplar�n�n herhangi bir ��pheli advers reaksiyonu T�rkiye Farmakovijilans Merkezi (T�FAM)'ne bildirmeleri gerekmektedir. (www.titck.gov.tr; e-posta: tufam@titck.gov.tr; tel: 0800 314 0008; faks: 0312 218 35 99)
4.9. Doz a��m� ve tedavisi
Akut: Tek doz halinde 2880 mikrogram siklesonid inhale etmi� sa�l�kl� g�n�ll�ler taraf�ndan olduk�a iyi tolere edilmi�tir.
�nhale siklesonid a��r� dozunu takiben olu�abilecek akut toksik etki potansiyeli d���kt�r. Akut doz a��m� s�z konusu oldu�unda hastaya �zg�n bir tedavi uygulamak gerekli de�ildir.
Kronik: Siklesonidin 1280 mikrogram dozundaki uzun s�reli kullan�m�nda b�brek �st� bezinin bask�lanmas� ile ili�kili klinik bulgulara rastlanmam��t�r. Bununla birlikte, �nerilen dozun a��ld��� uzun s�reli kullan�mlarda b�brek �st� bezinin bir miktar bask�lanma ihtimali d��lanamaz. Bu durumda hastadaki b�brek �st� bezi rezervinin denetlenmesi gerekebilir.
A��zl��� di�lerinizin aras�na koyunuz ve dudaklar�n�z� s�k�ca kapat�n�z.
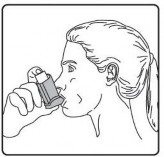
A��zl�k kapa��n� do�ru bir �ekilde yerle�tiriniz. Kapa�� yerle�tirmek i�in �ok fazla g�� uygulamay�n�z.
5. FARMAKOLOJ�K �ZELL�KLER
5.1. Farmakodinamik �zellikler
Farmakoterap�tik grup: Obstr�ktif solunum yolu hastal�klar�nda kullan�lan di�er ila�lar (inhalerler)/Glukokortikoidler
ATC kodu: R03BA08
Siklesonidin v�cuttaki glukokortikoid resept�rlerine ba�lanma afinitesi d���kt�r. A��zdan inhalasyon yoluyla uygulanan siklesonid akci�er dokusuna ula�t�ktan sonra enzim arac�l��� ile esas metaboliti olan C21-des-metilpropionil-siklesonide (M1) d�n���r. Siklesonidin aktif metaboliti olan C21-des-metilpropionil-siklesonid g��l� lokal antiinflamatuar etkinli�e sahiptir.
Klinik etkililik
Yap�lan klinik �al��malarda siklesonidin, yeti�kinlerde 640 mikrogram dozlarda maksimal etkilerin g�zlendi�i a��r� duyarl� hastalardaki adenozin monofosfat ve metakoline ba�l� havayolu duyarl�l���n� azaltt��� g�sterilmi�tir. Farkl� bir �al��mada ise 7 g�n s�reyle siklesonid uygulan�p ard�ndan inhale alerjen verilen grubun erken ve ge� d�nem havayolu reaksiyonlar�nda anlaml� azalma sa�land��� saptanm��t�r. �nhale siklesonid tedavisinin hastalar�n akci�er sekresyonlar�ndaki inflamatuar h�cre (total eozinofil) ve inflamatuar mediyat�r art���n� azaltt��� da g�sterilmi�tir.
26 eri�kin ast�ml� hastada yap�lan kontroll� �al��mada 7 g�n s�reyle siklesonid tedavisinden sonraki plazma kortizol EAA (konsantrasyon-zaman e�risi alt�ndaki alan) de�erlerinin 24 saatlik takipleri yap�lm��t�r. Plasebo ile k�yaslamal� olan bu �al��mada siklesonidin 320, 640 ve 1280 mikrogram/g�n gibi muhtelif dozlar� plazma kortizol d�zeyinin 24 saatlik ortalamalar�nda istatistiksel a��dan anlaml� d����e sebep olmad��� gibi, doza ba��ml� bir etki de g�zlenmemi�tir.
164 adet eri�kin erkek ve kad�n ast�ml� hastan�n kat�ld��� bir klinik �al��mada siklesonid 12 hafta s�reyle 320 ya da 640 mikrogram/g�n dozunda uygulanm��t�r. 12. haftan�n sonunda hastalara 1 ya da 250 mikrogram kosintropin uygulanm�� ve plasebo kullanan gruba k�yasla plazma kortizol d�zeylerinde anlaml� de�i�iklik g�zlenmemi�tir.
Eri�kin, ergen ve �ocuklarda, 12 hafta s�ren, �ift k�r ve plasebo kontroll� bir�ok �al��mada siklesonid ile tedavinin hastalar�n akci�er fonksiyonlar�nda sa�lad��� d�zelme �l��len FEVve doruk ekspiryum ak�m h�z� de�erleri ile g�sterilmi� olup ast�m semptomlar�n�n kontrol�ndeki geli�menin yan� s�ra hastalar�n inhale beta-agonist ihtiyac�nda azalma sa�lanm��t�r.
Daha �nce g�nde 500-1000 mikrogram flutikazon propiyonat veya e�de�eri verilen 680 �iddetli, 12 ya� ve �zeri ast�m hastas� ile yap�lan 12 haftal�k bir �al��mada, 160 veya 640 mikrogram siklesonid tedavisi s�ras�nda hastalar�n s�ras�yla %87,3 ve %93,3'�nde alevlenme g�r�lmemi�tir. 12 haftal�k �al��man�n sonu�lar�, ilk g�nden sonra, 160 mikrogram/g�n ve 640 mikrogram/g�n siklesonid doz uygulamalar� aras�nda alevlenme a��s�ndan istatistiksel olarak belirgin bir fark g�stermi�tir: 160 mikrogram/g�n verilen 339 hastan�n 43'�nde (%12,7) ve 640 mikrogram/g�n verilen 341 hastan�n 23'�nde (%6,7) alevlenme g�r�lm��t�r (Risk oran�: 0,523;
p:0,0134). Her iki doz, 12 hafta boyunca FEVde�erleri ile kar��la�t�r�lm��t�r. 160 veya 640 mikrogram/g�n siklesonid ile tedavi edilen hastalar�n s�ras�yla %3,8 ve %5'inde tedaviye ba�l� istenmeyen etki g�zlenmi�tir. �iddetli ast�m hastalar�nda yap�lan 160, 320 ve 640 mikrogram/g�n dozlar�n�n kar��la�t�r�ld��� bir �al��ma yoktur.
5.2. Farmakokinetik �zellikler
Genel �zelliklerFarmakokinetik karakterizasyon �o�unlukla M1 �zerinden yap�lm��t�r.
Emilim:
Radyoizotop ile i�aretlenmi� siklesonid kullanarak yap�lan oral ve intraven�z uygulamalarda oral emiliminin az oldu�u (%24,5) g�sterilmi�tir. Siklesonid ve aktif metabolitinin oral biyoyararlan�mlar� ihmal edilebilir d�zeydedir (siklesonid <%0,5; metabolit <%1). γ-sintigrafi y�ntemi ile yap�lan bir �l��m ile sa�l�kl� g�n�ll�lerin akci�er dokusundaki birikiminin, al�nan dozun %52'si oran�nda oldu�u g�sterilmi�tir. Siklesonidin �l��l� doz inhalasyon uygulamas� sonras�nda aktif metabolitin sistemik biyoyararlan�m� %50'nin �zerindedir. Aktif metabolitin oral biyoyararlan�m�n�n %1'in alt�nda olmas� nedeniyle inhale edilen siklesonidin a��zdan yutulan k�sm�n�n sistemik emilime herhangi bir katk�s� yoktur.
Da��l�m:
Sa�l�kl� g�n�ll�lere intraven�z yoldan uygulanan siklesonidin ba�lang�� da��l�m a�amas�n�n h�zl� oldu�u saptanm��t�r; bu durum, ilac�n y�ksek lipofilik �zelli�iyle de uyumludur. Da��l�m hacminin ortalama de�eri 2,9 L/kg'dir. Siklesonidin total serum klerensi ilac�n hepatik ekstraksiyonunun y�ksek oldu�una i�aret etmektedir (ortalama 2 L/sa/kg). Siklesonid ve aktif metaboliti neredeyse tamamen plazma proteinlerine ba�lanmaktad�r (%98-99).
Biyotransformasyon:
Siklesonid, akci�er dokusunda esteraz enzimleri arac�l���yla hidrolize edilerek biyolojik aktif metabolitine d�n��t�r�l�r. �nsan karaci�er mikrozomlar�nda u�rad��� daha ileri metabolizma a�amalar� enzimolojik olarak incelendi�inde, bu bile�i�in de daha sonra CYP3A4 taraf�ndan katalizlenen inaktif hidroksillenmi� metabolitlere d�n��t��� saptanm��t�r. Akci�erde ayr�ca aktif metabolite ait reversibl lipofilik ya� asidi ester bile�iklerinin varl��� da saptanm��t�r.
Eliminasyon:
Oral ve intraven�z uygulama sonras�nda siklesonidin v�cuttan esasen d��k� ile (%67) at�ld��� ve at�l�mdaki esas yolun safra sistemi oldu�u g�sterilmi�tir.
Do�rusall�k/Do�rusal olmayan durum:
Farmakokineti�i lineerdir. �nerilen tedavi dozlar�nda; sistemik maruziyeti dozla orant�l� art�� g�sterir.
Hastalardaki karakteristik �zellikler
B�brek yetmezli�i:
Aktif metabolitin b�brek yoluyla at�l�m� s�z konusu olmad���ndan, b�brek yetmezlikli hastalar ile �al��ma yap�lmam��t�r.
Karaci�er yetmezli�i:
Karaci�er fonksiyonundaki azalma kortikosteroidlerin v�cuttan at�l�m�n� etkileyebilir. Sirotik hastalar�n da kat�lm�� oldu�u bir �al��mada aktif metabolitin sistemik maruziyetinde art�� g�zlenmi�tir.
Geriyatrik pop�lasyon:
Geni� �apl� toplumsal �al��malarda saptanan farmakokinetik �zelliklerinden yola ��k�larak aktif metabolitin sistemik maruziyetinde ya� fakt�r�n�n etkisi bulunmad��� ortaya konmu�tur.
Di�er:
Siklesonidin hafif-orta d�zeyde ast�m hastalar�ndaki farmakokineti�i sa�l�kl� g�n�ll�lerde saptanm�� olan de�erlerden farkl� de�ildir.
5.3. Klinik �ncesi g�venlilik verileri
G�venilirlik farmakolojisi, kronik toksisite, genotoksisite ile karsinojenik potansiyel gibi geleneksel �al��malardan elde edilen preklinik veriler, siklesonid kullan�m�n�n insan i�in hi�bir �zel tehlikesi olmad���n� ortaya ��kartm��t�r.
�reme toksisitesi i�in yap�lan hayvan �al��malar�nda glukokortikosteroidlerin yar�k damak, iskelet malformasyonlar� gibi etkilerine rastlanm��t�r. Ancak, bu sonu�lar�n insanlara �nerilen dozlarda olu�abilmesi m�mk�n g�r�nmemektedir.
K�pekler ile yap�lan 12 ay s�ren iki �al��mada, en y�ksek dozlar�n yumurtal�klar �zerinde tedaviye ba�l� etkiler (atrofi) olu�turdu�u g�zlenmi�tir. Bu etkiler, 160 mikrograml�k g�nl�k dozun 5,27-8,34 kat�n�n sistemik maruziyeti sonucu meydana gelmi�tir. Bu bulgular�n insanlar ile ili�kisi bilinmemektedir.
Di�er glukokortikoid t�revleri ile yap�lan hayvan �al��malar�nda gebelik s�ras�nda ve farmakolojik dozlardaki kullan�mlar�nda glukokortikoidlerin intrauterin b�y�me gerili�i, eri�kinlikte kar��la��lan kalp-damar ve/veya metabolik hastal�k ile glukokortikoid resept�r yo�unlu�unda de�i�im, n�rotransmiter �retimi ve davran�� bozuklu�u gibi riskleri artt�rabildi�i g�sterilmi�tir. Bu verilerin insanlara inhalasyon yoluyla uygulanan siklesonid ile ilintisi hakk�nda bilgi mevcut de�ildir.
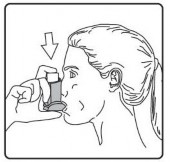
A�z�n�zdan yava� ve derin nefes al�n�z ve ayn� anda bir puf doz bo�altmak i�in inhalasyon spreyinizin �st k�sm�na bas�n�z.
6. FARMAS�T�K �ZELL�KLER
6.1. Yard�mc� maddelerin listesi
HFA 134a
Etil Alkol %99 Absolute
6.2. Ge�imsizlikler
Bilinen ge�imsizli�i yoktur.
6.3. Raf �mr�
24 ay
6.4. Saklamaya y�nelik �zel tedbirler
25°C alt�ndaki oda s�cakl���nda saklay�n�z. Direkt g�n �����ndan ve donmaktan koruyunuz. Aerosol kutusu delinmemeli, bo� olsa bile k�r�lmamal�, ate�ten uzak tutulmal�d�r.
6.5. Ambalaj�n niteli�i ve i�eri�i
CLEN�D 80 mikrogram inhalasyon i�in �l��l� dozlu aerosol, kutuda, �effaf PE-PET folyo i�inde, dozaj valfli konkav tabanl� alu t�pte, a��zl��� olan plastik uygulama aparat� ile kullanma talimat� ile beraber ambalajlan�r.
6.6. Be�eri t�bbi �r�nden arta kalan maddelerin imhas� ve di�er �zel �nlemler
Kullan�lmam�� olan �r�nler ya da at�k materyaller “T�bbi At�klar�n Kontrol� Y�netmeli�i” ve “Ambalaj At�klar�n�n Kontrol� Y�netmeli�i”ne uygun olarak imha edilmelidir.
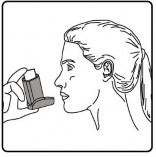
Nefesinizi yakla��k 10 saniye veya rahat�a tutabildi�iniz kadar tutunuz ve a��zl��� a�z�n�zdan ��kar�p parma��n�z� inhalasyon spreyinizin �st k�sm�ndan �ekiniz. Sonra yava��a a�z�n�zdan nefes veriniz. �nhalerin i�ine nefes vermekten ka��n�z.
4. basamak ile 6. basamak aras�nda anlat�lanlar� uygularken acele ETMEMEN�Z �nemlidir.
 L�semi Kan Kanseri
L�semi, kan kanseridir ve v�cudunun kan olu�turan dokular�n�n hastalanmas� anlam�na gelir. Bir�ok l�semi t�r� vard�r; baz� l�semi t�rleri �ocuklarda baz�lar� da yeti�kinlerde s�k g�r�l�r.
L�semi Kan Kanseri
L�semi, kan kanseridir ve v�cudunun kan olu�turan dokular�n�n hastalanmas� anlam�na gelir. Bir�ok l�semi t�r� vard�r; baz� l�semi t�rleri �ocuklarda baz�lar� da yeti�kinlerde s�k g�r�l�r. |
 Travma Sonras� Bunal�m�
Travmatik bir olay, g�nl�k ola�an olaylar�n d���nda olan ve ki�iyi derinden
rahats�z eden bir olayd�r.Bir�ok olay b�yle bir etki g�sterebilir.
Travma Sonras� Bunal�m�
Travmatik bir olay, g�nl�k ola�an olaylar�n d���nda olan ve ki�iyi derinden
rahats�z eden bir olayd�r.Bir�ok olay b�yle bir etki g�sterebilir. |
�LA� E�DE�ERLER�
| E�de�er �la� Ad� | Barkodu | �la� Fiyat� |
|---|---|---|
| ALVESCO | 8699456520143 | |
| CLENID | 8680741520924 | 395.25TL |
| FORLEX | ||
| LASECON | 8699525520180 | 333.27TL |
| OMNARIS | 8699456540028 | |
| Di�er E�de�er �la�lar |
 |
Ast�m Ast�ml� ki�ilerin akci�erlerindeki hava borular� (bron�lar) hassast�r. Bu ki�iler belirli tetikleyici fakt�rlere maruz kald�klar�nda, hava borular� nefes almalar�n� g��le�tirecek �ekilde daral�r. |
 |
Grip, So�uk Alg�nl��� ve �ks�r�k Grip ve so�uk alg�nl��� (nezle) semptomlar� aras�ndaki fark� bilmek �nemlidir. So�uk alg�nl��� gripten daha hafif belirtiler g�steren bir solunum yolu hastal���d�r. |
 |
Ast�m Ast�ml� ki�ilerin akci�erlerindeki hava borular� (bron�lar) hassast�r. Bu ki�iler belirli tetikleyici fakt�rlere maruz kald�klar�nda, hava borular� nefes almalar�n� g��le�tirecek �ekilde daral�r. |
�LA� GENEL B�LG�LER�
Neutec �la� San. Tic.A.�.
| Sat�� Fiyat� | 346.82 TL [ 15 Apr 2024 ] |
| �nceki Sat�� Fiyat� | 346.82 TL [ 5 Apr 2024 ] |
| Original / Jenerik | Jenerik �la� |
| Re�ete Durumu | Normal Re�eteli bir ila�d�r. |
| Barkodu | 8680741520917 |
| Etkin Madde | Siklesonid |
| ATC Kodu | R03BA08 |
| Birim Miktar | 80 |
| Birim Cinsi | MCG |
| Ambalaj Miktar� | 120 |
| Solunum Sistemi > Di�er �nhalanlar (solukla i�eri �ekilen ila�lar) > Siklesonid |
| Yerli ve Be�eri bir ila�d�r. |